名校
解题方法
1 . 下列实验方案能达到实验目的的是
| 实验方案 | 实验目的 | |
| A | 白铁皮(镀锌铁)出现刮痕后浸泡在食盐水中,一段时间后浸泡液中滴入几滴 | 探究上述过程铁是否发生腐蚀 |
| B | 将 (强氧化剂)固体溶于水后,加入浓盐酸 (强氧化剂)固体溶于水后,加入浓盐酸 | 证明 溶液存在平衡: 溶液存在平衡: + + ⇌ ⇌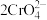 + + |
| C | 用两支试管各取 的 的 溶液,分别加入10滴 溶液,分别加入10滴 和 和 的草酸(H2C2O4)溶液,记录溶液褪色所需的时间 的草酸(H2C2O4)溶液,记录溶液褪色所需的时间 | 探究反应物浓度对反应速率的影响 |
| D | 分别在20℃、30℃下,向 溶液中依次加入 溶液中依次加入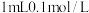 硫酸和2滴淀粉溶液 硫酸和2滴淀粉溶液 | 探究温度对4I-+O2+4H+=2I2+2H2O反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
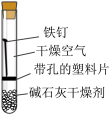
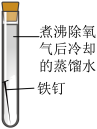
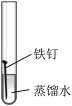
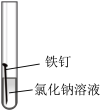
2 . 某小组同学对不同条件下铁钉的锈蚀进行了实验。
(1)一周后观察,铁钉被腐蚀程度最大的是___________ (填实验序号)。
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。___________ (填字母,下同)。
a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
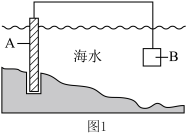
(3)电化学原理在保护海水中钢闸门中有广泛应用。______ 。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择______ 。
a.碳棒 b.锌板 c.铜板
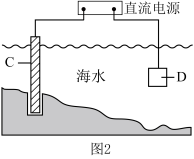
③图2中,钢闸门C应连接直流电源的___________ (填“正”或“负”)极。
| 序号 | ① | ② | ③ | ④ |
| 实验 |
|
|
|
|
(1)一周后观察,铁钉被腐蚀程度最大的是
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。

a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择
a.碳棒 b.锌板 c.铜板
③图2中,钢闸门C应连接直流电源的
您最近半年使用:0次
2023-12-25更新
|
159次组卷
|
2卷引用:北京市第十五中学2022-2023学年高二上学期期中考试 化学试题
解题方法
3 . 一定温度下,利用下列装置进行实验,能达到实验目的的是
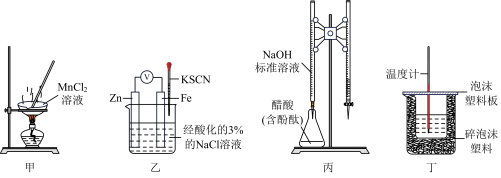

A.利用甲装置蒸干制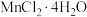 |
| B.利用乙装置验证牺牲阳极的阴极保护法 |
| C.利用丙装置测定醋酸溶液的浓度 |
| D.利用丁装置测定酸碱中和反应的反应热 |
您最近半年使用:0次
解题方法
4 . 化学与科技、生产、生活有密切的关系,下列叙述不正确的是
| A.在碳中和研究中,选择合适的催化剂将CO2氧化为甲酸等液体燃料 |
| B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| C.我国海洋开发走向“深蓝时代”,大型舰船的底部常镶嵌锌块做负极,防止船底腐蚀 |
| D.丝绸主要成分是高分子化合物蛋白质 |
您最近半年使用:0次
5 . 某兴趣小组探究金属腐蚀条件,设计了以下实验装置。下列说法不正确的是
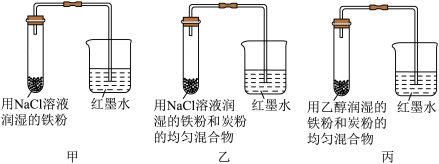

| A.铁粉腐蚀速率:乙>甲>丙 |
| B.甲、乙、丙三个装置均构成原电池,发生吸氧腐蚀 |
C.乙装置发生电化学腐蚀时正极反应式: |
| D.对比甲、乙、丙三个实验,金属放在有些有机溶剂中可防腐蚀 |
您最近半年使用:0次
名校
解题方法
6 . 下列图示装置或操作不能达到实验目的的是
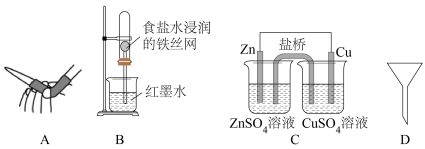

| A.图A碱式滴定管排气泡 | B.图B验证铁的吸氧腐蚀 |
| C.图C比较Zn与Cu金属性强弱 | D.图D提取碘水中的碘 |
您最近半年使用:0次
解题方法
7 . 化学与生活密切相关。下列说法中错误的是
| A.废旧电池随意丢弃会造成环境污染 |
| B.一次性保暖贴利用了铁被腐蚀时放热的原理 |
C.利用工业废气中的 合成 合成 是减少碳排放的一种方法 是减少碳排放的一种方法 |
D.常温常压下,利用新技术改变 的摩尔燃烧焓,使单位质量的 的摩尔燃烧焓,使单位质量的 燃烧时放热更多 燃烧时放热更多 |
您最近半年使用:0次
名校
解题方法
8 . 关于化学与生活、化学与生产,下列说法不正确的是
| A.燃烧热是评价燃料优劣的唯一标准 |
| B.在海轮外壳连接锌块保护外壳不受腐蚀,采用的是牺牲阳极的阴极保护法,属于原电池原理 |
| C.工业电解精炼铜用粗铜作阳极,纯铜作阴极 |
| D.为了延缓海水中钢闸门的腐蚀,常将钢闸门与直流电源的负极相连 |
您最近半年使用:0次
9 . 回答下列问题
(1)如图所示将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中。
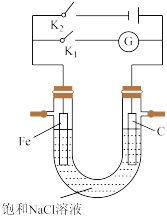
①K1闭合,铁电极的反应为___________ 。
②K2闭合,铁棒不会被腐蚀,属于___________ 保护法。
(2)氯碱工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂,氯气是制备系列含氯化合物的主要原料,可采用如图所示的装置来制取:
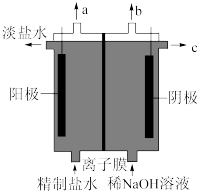
①写出电解饱和食盐水的化学方程式___________ ;氯气的逸出口是___________ 。
②该离子交换膜为___________ (填“阴”或“阳”)离子交换膜。
③电解产生1molCl2,理论上阳极室减少的离子数为___________ 。
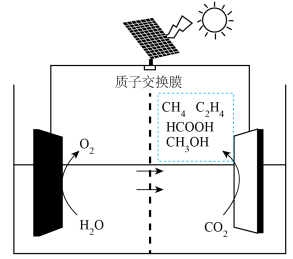
(3)目前,科研人员在研究CO2光电催化还原为甲醇的领域也取得了一定的进展,其原理如图所示,则生成甲醇的电极反应式为___________ 。
(1)如图所示将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中。

①K1闭合,铁电极的反应为
②K2闭合,铁棒不会被腐蚀,属于
(2)氯碱工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂,氯气是制备系列含氯化合物的主要原料,可采用如图所示的装置来制取:

①写出电解饱和食盐水的化学方程式
②该离子交换膜为
③电解产生1molCl2,理论上阳极室减少的离子数为
(3)目前,科研人员在研究CO2光电催化还原为甲醇的领域也取得了一定的进展,其原理如图所示,则生成甲醇的电极反应式为

您最近半年使用:0次
10 . 回答下列问题:
(1)以下合成材料制品中,属于塑料制品的是_______ ;属于橡胶制品的是_______ ;属于纤维制品的是_______ ;属于复合材料制品的是_______ 。
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子_______ (填“被氧化”或“被还原”),生成阳离子的过程;在海水中为防止钢铁巨轮被腐蚀,常在轮船水面下的船体上焊上_______ (填“锌块”或“铜块”)。
(1)以下合成材料制品中,属于塑料制品的是
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子
您最近半年使用:0次