名校
解题方法
1 . CH3OH、CO、CH4等都是重要的能源,也是重要的化工原料。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
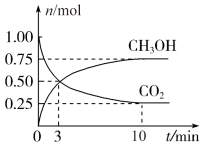
①从反应开始到平衡,CO2的平均反应速率v(CO2)=____ 。
②达到平衡时,H2的浓度为____ mol/L。
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是____ 。
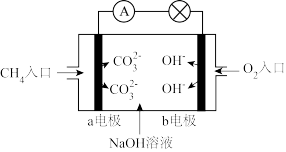
(3)某种甲烷燃料电池的工作原理如图所示氧气通入的一极为电源的____ 极,a电极反应式:____ ,b电极反应式:____ 。
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)____ L。
(1)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的浓度为
(2)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是| A.反应中CO与CH3OH的物质的量之比为1:1 |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH |
| D.CH3OH的质量分数在混合气体中保持不变 |
(4)当电路中累计有2 mol电子通过时,消耗的甲烷体积为(在标准状况下)

您最近一年使用:0次
2022-05-12更新
|
440次组卷
|
3卷引用:福建省福州第八中学2021-2022学年高一下学期期末考试化学试题
名校
2 . 电化学气敏传感器可用于监测环境中 的含量,其工作原理示意图如下。下列说法不正确的是
的含量,其工作原理示意图如下。下列说法不正确的是
 的含量,其工作原理示意图如下。下列说法不正确的是
的含量,其工作原理示意图如下。下列说法不正确的是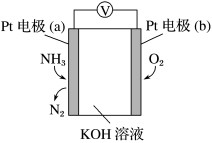
A. 在电极b上发生还原反应 在电极b上发生还原反应 |
B.溶液中 向电极a移动 向电极a移动 |
| C.电子流向:由负极经外电路流入正极,再通过内电路流回负极 |
D.负极的电极反应式为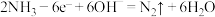 |
您最近一年使用:0次
2023-04-16更新
|
521次组卷
|
4卷引用:福建省福州第三中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
3 . 通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示,下列说法正确的是
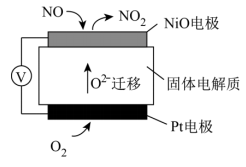
| A.Pt电极上发生的是氧化反应 |
| B.外电路中,电子从Pt电极流向NiO电极 |
| C.NiO电极上的电极反应方程式为NO+O2--2e-=NO2 |
| D.O2的电极反应产物是H2O |
您最近一年使用:0次
2022-06-01更新
|
316次组卷
|
3卷引用:福建省福州格致中学2023-2024学年高一下学期3月月考化学试卷
解题方法
4 . 如图是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源正极。
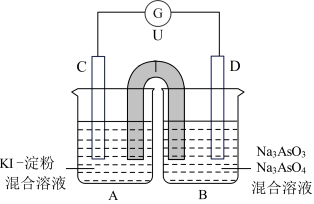
(1)As(砷)位于元素周期表中第四周期ⅤA族,则Na3AsO4溶液的pH____ 7(填“>”、“<”或“=”)。
(2)向B烧杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A烧杯中的主要实验现象是______ ,C电极上的电极反应式为:__ 。
(3)一段时间后,再向B烧杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总的离子方程式为I2+ +2OH-=2I-+
+2OH-=2I-+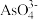 +H2O,此时D为
+H2O,此时D为____ 极,发生________ 反应。
(4)再过一段时间后,G的指针逐渐归零,此时实验装置中的化学反应已经达到化学平衡状态,该反应的化学平衡常数的表达式为:K=_____________ 。

(1)As(砷)位于元素周期表中第四周期ⅤA族,则Na3AsO4溶液的pH
(2)向B烧杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A烧杯中的主要实验现象是
(3)一段时间后,再向B烧杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总的离子方程式为I2+
 +2OH-=2I-+
+2OH-=2I-+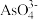 +H2O,此时D为
+H2O,此时D为(4)再过一段时间后,G的指针逐渐归零,此时实验装置中的化学反应已经达到化学平衡状态,该反应的化学平衡常数的表达式为:K=
您最近一年使用:0次



