名校
解题方法
1 . 下列关于四种装置的叙述不正确的是( )
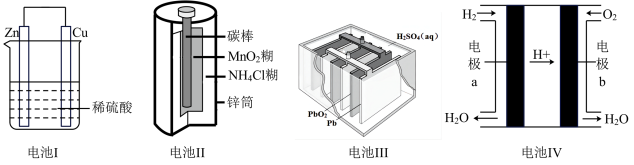

| A.电池Ⅰ:正极发生的反应为2H++2e﹣═H2↑ |
| B.电池Ⅱ:锌筒做负极,发生氧化反应 |
| C.电池Ⅲ:是最早使用的充电电池,又称为二次电池 |
| D.电池Ⅳ:外电路中电子由电极b通过导线流向电极a |
您最近一年使用:0次
2020-06-03更新
|
397次组卷
|
6卷引用:四川省成都南开为明学校2019-2020学年高一下学期期中考试化学试题
名校
2 . 利用金属镁和铝设计成如图所示的原电池。下列说法正确的是
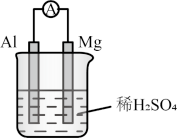
| A.铝作该原电池的负极 |
B.溶液中 向Mg电极移动 向Mg电极移动 |
C.若将稀 换成乙醇,则电流表的指针也能偏转 换成乙醇,则电流表的指针也能偏转 |
D.若将稀 换成 换成 溶液,则Al电极发生的电极反应为 溶液,则Al电极发生的电极反应为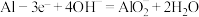 |
您最近一年使用:0次
2023-05-31更新
|
101次组卷
|
3卷引用:四川省眉山市部分名校2022-2023学年高一下学期5月期中大联考化学试题
四川省眉山市部分名校2022-2023学年高一下学期5月期中大联考化学试题甘肃省靖远县第一中学2022-2023学年高一下学期期末练习化学试题(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
3 . NO2和N2O4之间发生反应:N2O4 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
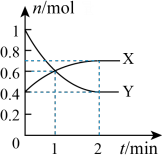
(1)曲线____________ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。在0到1min中内用X表示该反应的速率是________________ ,该反应达最大限度时Y的转化率_______ 。
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中y(N2O4)=0.2 mol·L-1·min-1,则__________ 中反应更快。
(3)下列描述能表示反应达平衡状态的是______________________ 。
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的平均相对分子质量不再改变
E.容器内气体的密度不再发生变化
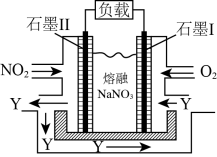
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如右图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是______________ (填“正极”或“负极”),石墨Ⅱ的电极反应式为_________________________________ 。
 2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题:
2NO2,一定温度下,体积为2L的密闭容器中,各物质的物质的量随时间变化的关系如图所示。请回答下列问题: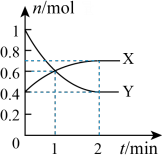
(1)曲线
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中 v(NO2)=0.3 mol·L-1·min-1,乙中y(N2O4)=0.2 mol·L-1·min-1,则
(3)下列描述能表示反应达平衡状态的是
A.容器中X与Y的物质的量相等
B.容器内气体的颜色不再改变
C.2v(X)=v(Y)
D.容器内气体的平均相对分子质量不再改变
E.容器内气体的密度不再发生变化
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如右图,该电池在使用过程中石墨Ⅱ电极上生成氧化物Y(N2O5),则石墨I电极是

您最近一年使用:0次
名校
解题方法
4 . 某兴趣小组设计的原电池如图所示,下列说法正确的是

| A.Cu电极为负极,发生氧化反应 |
| B.电池工作时,电子从Zn电极经电解质溶液流向Cu电极 |
| C.当Zn电极质量减少65g时,Cu电极生成22.4LH2 |
D.放电过程中, 从左向右移动 从左向右移动 |
您最近一年使用:0次
2023-07-06更新
|
101次组卷
|
2卷引用:四川省凉山州安宁河联盟2022-2023学年高一下学期期末联考化学试题
解题方法
5 . Ⅰ.依据氧化还原反应: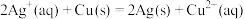 设计的原电池如下图所示,
设计的原电池如下图所示,
(1)电极X的材料是________ ;电解质溶液Y是________ ;
(2)银电极为原电池的_________ 极。(填“正”或“负”)
Ⅱ.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:______ ,若初始时两电极质量相等,当电路中有0.2mole-通过时,两电极的质量差为______ g。
(4)当电极a为 ,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为______ ,对比(3)和(4),说明原电池中相对活泼的金属做正极还是负极,除了与金属本身的还原性有关外,还与______ 有关。
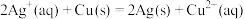 设计的原电池如下图所示,
设计的原电池如下图所示,
(1)电极X的材料是
(2)银电极为原电池的
Ⅱ.如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
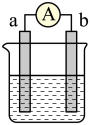
(4)当电极a为
 ,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
,电极b为Cu,电解质溶液为浓硝酸时,则电池的正极反应式为
您最近一年使用:0次
名校
解题方法
6 . 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是


A.Zn为正极,电极反应式为: |
B.电池工作时 向Cu电极移动 向Cu电极移动 |
| C.电子由Zn电极经稀硫酸溶液流向Cu电极 |
D.Zn电极质量每减少65g,则在该电极产生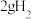 |
您最近一年使用:0次
2022-07-15更新
|
127次组卷
|
2卷引用:四川省凉山州2021-2022学年高一下学期期末考试化学试题
名校
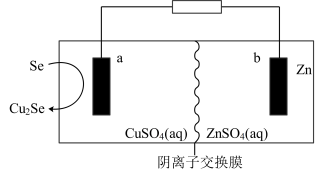
7 . 我国科学家最近开发出锌硒电池,工作原理如图所示。放电时,电池总反应为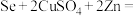
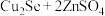 。下列说法正确的是
。下列说法正确的是
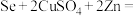
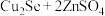 。下列说法正确的是
。下列说法正确的是
| A.放电时电能转化成化学能 |
B.a极的电极反应式为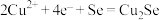 |
C.放电时,溶液中 向a极迁移 向a极迁移 |
| D.1mol Se完全反应时外电路中转移2mol电子 |
您最近一年使用:0次
名校
解题方法
8 . 如图为原电池装置示意图:
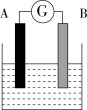
(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为________ 极(填正或负),写出电极反应式:正极_______________________ ,负极________________________ .总反应为:____________________ 。
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为________ 极(填正或负),写出电极反应式:正极_____________________________ ,负极________________________ .总反应为:_______________________________ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的________ 极(填正或负),该电池的总反应为:____________________

(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的
您最近一年使用:0次
2020-04-19更新
|
410次组卷
|
2卷引用:四川省遂宁市船山区第二中学校2019-2020学年高一下学期期中考试化学试题
解题方法
9 . 目前,第三代混合动力车已经投入市场,成为能源改革的典范。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:_____ 。
(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:_____ 。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH
 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:
您最近一年使用:0次
名校
解题方法
10 . 请根据所学知识,回答下列问题:
某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
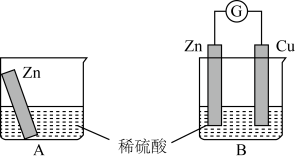
(1)B中Zn板是___________ 极,正极发生的电极反应是___________
(2)该小组同学反思原电池的原理,其中观点正确的是___________;
(3)在B中,当导线中有1 mol电子通过时,理论上的两极变化是___________。
(4)若将反应2Fe3++Cu=Cu2++2Fe2+设计成原电池,写出正极电极反应式___________ ;
(5)写出碱性氢氧燃料电池正极电极反应式___________
(6)写出酸性乙醇(C2H5OH)燃料电池负极电极反应式___________
(7)写出铜片和铝片插入浓硝酸溶液中的正极反应为:___________
某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
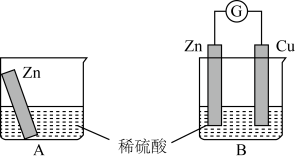
(1)B中Zn板是
(2)该小组同学反思原电池的原理,其中观点正确的是___________;
| A.原电池反应的过程中一定有电子转移 |
| B.电极一定不能参加反应 |
| C.原电池装置中的电子流向:负极→外线路→正极→电解质→负极 |
| D.氧化反应和还原反应可以拆开在两极发生 |
| A.锌片溶解32.5 g | B.锌片增重32.5 g |
| C.铜片上析出2 g H2 | D.铜片上析出1 mol H2 |
(5)写出碱性氢氧燃料电池正极电极反应式
(6)写出酸性乙醇(C2H5OH)燃料电池负极电极反应式
(7)写出铜片和铝片插入浓硝酸溶液中的正极反应为:
您最近一年使用:0次



