名校
1 . 完成下列问题。
(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
请回答下列问题。
①该可逆反应的化学方程式可表示为___________ 。
②从反应开始到2s末,A的转化率为___________ 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是___________ (填序号)
A.υB(消耗)= υC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.υA:υB:υC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是___________ 。
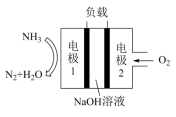
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为________ ;负极的电极反应式为________ 。
(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
aA(g)+bB(g)  cC(g) cC(g) | |
| 起始物质的量浓度/( mol∙L−1) | 1.5 1 0 |
| 2s末物质的量浓度/( mol∙L−1) | 0.9 0.8 0.4 |
①该可逆反应的化学方程式可表示为
②从反应开始到2s末,A的转化率为
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.υB(消耗)= υC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.υA:υB:υC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为

您最近一年使用:0次
解题方法
2 . 到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。
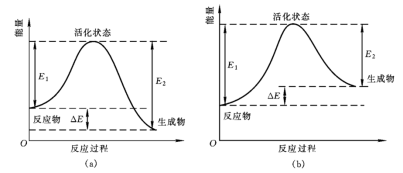
(1)从能量变化角度研究反应: 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是___________ (填字母)。
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
则生成 放出热量
放出热量___________ kJ。
(3)肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是___________ 。
(4)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
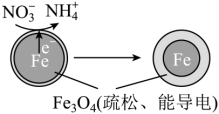
①作负极的物质是___________ 。
②正极的电极反应式是___________ 。
(1)从能量变化角度研究反应:
 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 放出热量
放出热量(3)肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是
(4)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
您最近一年使用:0次
名校
3 . 我国科学家设计的“海泥电池”,既可用于深海水下仪器的电源补给,又有利于海洋环境污染治理,其中微生物代谢产物显酸性,电池工作原理如图所示。下列说法错误的是
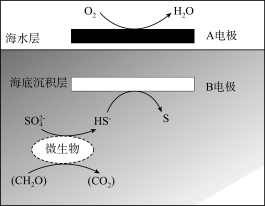
| A.A电极为正极 |
| B.质子从海底沉积层通过交接面向海水层移动 |
| C.负极的电极反应式为CH2O-4e-+H2O=CO2+4H+ |
| D.高温下微生物蛋白质变性失活,故升温不一定能提高电池的效率 |
您最近一年使用:0次
2023-05-05更新
|
769次组卷
|
5卷引用:四川省南充市嘉陵第一中学2022-2023学年高一下学期4月期中考试化学试题
四川省南充市嘉陵第一中学2022-2023学年高一下学期4月期中考试化学试题辽宁省六校协作体2022-2023学年高一下学期期末考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题(已下线)重难点03 原电池原理的应用与化学电源-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)重难点03 原电池的工作原理与相关判断-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
4 . 如图所示原电池装置中,溶液为稀硫酸,电子流向如图所示。下列说法正确的是
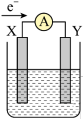

| A.电极X为正极 |
| B.X电极上发生氧化反应,Y电极上发生还原反应 |
C.氢气产生在X电极上, 移向X电极 移向X电极 |
| D.电子流动方向为:X电极→导线→Y电极→溶液→X电极 |
您最近一年使用:0次
名校
解题方法
5 . 人类的一切活动都离不开能量,人们不仅利用化学反应获得新物质,也需从化学反应中获得能量。回答下列问题:
Ⅰ、键能是指在1 × 105 Pa、298 K时,将1 mol气态分子分离成气态原子所需要的能量,其单位为kJ·mol−1,已知H—H的键能为436 kJ·mol−1;N≡N的键能为946 kJ·mol−1;N—H的键能为391 kJ·mol−1。
(1)NH3的电子式为___________ 。
(2)在1 × 105 Pa、298 K时,生成2 mol NH3(g),吸收或放出的热量为Q kJ,则Q =___________ ,能正确表示该过程的能量变化的是___________ (填标号)。
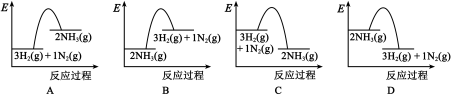
Ⅱ、电化学气敏传感器可用于监测空气中的污染物,空气中NH3的含量监测原理如图所示。
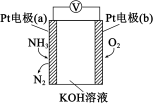
(3)正极为___________ (填“a”或“b”)电极,负极发生的电极反应式为___________ ,原电池总反应方程式为___________ 。
(4)溶液中OH−向电极___________ (填“a”或“b”)移动,电池工作一段时间后,溶液c(OH−)___________ (填“变大”“变小”或“不变”)。
(5)当转移电子数为6.02 × 1023时,被还原的气体的质量为___________ g。
Ⅰ、键能是指在1 × 105 Pa、298 K时,将1 mol气态分子分离成气态原子所需要的能量,其单位为kJ·mol−1,已知H—H的键能为436 kJ·mol−1;N≡N的键能为946 kJ·mol−1;N—H的键能为391 kJ·mol−1。
(1)NH3的电子式为
(2)在1 × 105 Pa、298 K时,生成2 mol NH3(g),吸收或放出的热量为Q kJ,则Q =

Ⅱ、电化学气敏传感器可用于监测空气中的污染物,空气中NH3的含量监测原理如图所示。

(3)正极为
(4)溶液中OH−向电极
(5)当转移电子数为6.02 × 1023时,被还原的气体的质量为
您最近一年使用:0次
2023-04-29更新
|
294次组卷
|
2卷引用:四川省成都市蓉城名校联盟2022-2023学年高一下学期期中联考化学试题
10-11高一下·辽宁大连·阶段练习
名校
解题方法
6 . 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的c(H+)均减小 | D.产生气泡的速率甲比乙慢 |
您最近一年使用:0次
2023-04-28更新
|
1845次组卷
|
115卷引用:四川省雅安中学2020-2021学年高一下学期开学考试化学试题
四川省雅安中学2020-2021学年高一下学期开学考试化学试题四川省泸州市龙马潭区2023-2024学年高一下学期5月期中考试化学试题(已下线)2010—2011学年辽宁省大连协作体高一4月月考化学试卷(已下线)2010—2011学年云南省芒市中学高一下学期期末考试化学试卷理(已下线)2010—2011学年山东省任城一中高一下学期期末考试化学试卷(已下线)2012-2013学年福建省福州文博中学高一下学期期末考试化学试卷(已下线)2014年高一化学人教版必修2 期中测试练习卷(已下线)2013-2014湖南师大附中第二学期期中考试高一化学试卷(已下线)2013-2014四川省雅安中学下学期期中考试高二化学试卷(已下线)2013-2014山西省山大附中高一下学期期中化学试卷(已下线)2013-2014四川省雅安中学下学期期中考试高二化学试卷2014-2015陕西省三原北城中学高一下学期第一次月考化学试卷2014-2015安徽省宣郞广三校高一下学期期中联考化学试卷2014-2015学年吉林省松原市扶余县第一中学高一下期末化学试卷2015-2016北京大学附中宇华教育集团高一12月化学卷2015-2016学年河北武邑中学高一下5.15周考化学试卷2015-2016学年江西省宜春三中高一下期中化学试卷2015-2016学年浙江省宁波市效实中学高一下期中化学试卷2015-2016学年广东省仲元中学高一下期末文科化学试卷2016-2017学年浙江省温州市“十五校联合体”高一下学期期中联考化学试卷河北省张家口市第一中学2016-2017学年高一(实验班、普通班)6月月考(文)化学试题广西贵港市覃塘高级中学2016-2017学年高一6月月考化学试题河北省张家口市2016-2017学年高一下学期期末考试化学试题高中化学人教版 选修四 第四章 电化学基础 第一节 原电池 原电池新疆兵团第二师华山中学2017-2018学年高一下学期期中考试化学试题黑龙江省绥滨县第一中学2018-2019学年高一(理)下学期期中考试化学试题吉林省吉林市第三中学2018-2019学年高一5月阶段测试化学试题山西省祁县第二中学校2018-2019学年高一下学期期末考试化学试题上海市浦东新区2017-2018学年高一上学期期末化学试题上海市金山中学2015-2016学年高一下学期期中考试化学试题6.1.2 化学反应与电能——2020年春高一新人教版第二册化学一课一练山东省滕州市第一中学2019-2020学年高一下学期第一次月考化学试题第2章 化学键化学反应规律 综合拓展——B拓展区 夯实基础(鲁科版(2019)第二册)第2章 化学键 化学反应与能量 综合拓展——B拓展区 夯实基础(鲁科版必修2)2020年春高一化学新人教版第二册课后同步:6.1.2 化学反应与电能河北省唐山市海港高级中学2019-2020学年高一下学期第五次校考化学试题安徽省合肥市2019—2020学年高一下学期期中考试化学试题河北省邯郸市肥乡区第一中学2019-2020学年高一下学期开学考试化学试题江西省南昌市实验中学2019-2020学年高一5月摸底考试化学试题江苏省响水中学2019-2020学年高一下学期期中考试化学试题贵州省贵阳市第十四中学2019-2020学年高一下学期期末考试化学试题上海理工大附中2014-2015学年高一上学期期末化学试卷河北省秦皇岛市卢龙县中学2019-2020学年高一下学期第二次调研考试化学试题贵州省贵阳十四中2019-2020学年高一下学期期末考试化学试题高中化学苏教2019版必修第二册-专题6 第三单元 第1课时 化学能转化为电能(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一5月月考化学试题辽宁省朝阳市建平县实验中学2020-2021学年度高一下学期期末考试化学试题(已下线)第14讲 原电池-2020-2021学年秋季班高一上学期化学教材知识点精讲练(沪科版)甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(文)试题甘肃省庆阳市第六中学2020-2021学年高一下学期期中考试化学(理)试题广东省茂名高州市2020-2021学年高一下学期期末考试化学试题吉林省乾安县第四中学2020-2021学年高一下学期期中考试化学试题福建省福州市文博中学2020-2021学年高一下学期期中考试化学试题(已下线)章末培优 第6章 化学反应与能量-2021-2022学年高一化学课后培优练(人教版2019必修第二册)湖南省长沙市雅礼中学2021-2022学年高一下学期期中联考化学试题天津市南开大学附属中学2021-2022学年高一下学期期中检测化学试题(已下线)第06练 原电池的工作原理及其应用-2022年【暑假分层作业】高一化学(人教版2019必修第二册)甘肃省武威市凉州区2021-2022学年高一下学期期末考试化学试题辽宁省东北师范大学连山实验高中2021-2022学年高一下学期第一次线上考试化学试题吉林省松原市油田第十一中学2021-2022学年高一下学期期末考试化学试题湖南省长沙市湖南师大附中2022-2023学年高一下学期第一次月考化学试题 湖南师范大学附属中学2022-2023学年高一下学期第一次月考化学试题第六章 化学反应与能量(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)广东省深圳市光明区高级中学、 深圳市光明书院2022-2023学年高一下学期4月期中联考化学试题(已下线)第六章 化学反应与能量【单元测试B卷】(已下线)2010—2011学年海南省洋浦中学高二上学期期末考试化学试卷(已下线)2011-2012年云南省建水一中高二上学期期中考试化学(理)试题(已下线)2011-2012学年甘肃武威六中高二上学期期末考试化学(理)试卷(已下线)2011-2012学年吉林省松原市油田高中高二上学期期末考试化学试卷(已下线)2011-2012学年安徽省六安市徐集中学高二上学期期末考试化学试卷(已下线)2012年苏教版高中化学选修4 1.2化学能与电能的转化(已下线)2014届山东省济南一中高二上学期期末考试化学试卷 2014-2015学年福建省清流一中高二上学期月考化学理试卷2014-2015山东省淄博市沂源一中高二12月月考化学试卷2014-2015陕西省西安市庆安高级中学高二上学期期末化学试卷2014-2015山东省淄博市沂源县第一中学高二12月月考化学试卷2014-2015陕西省西安市七十中高二上学期期末考试化学试卷2015-2016学年甘肃省天水一中高二上学期第一次段中考试化学试卷2015-2016北京大学附中宇华教育集团高二12月化学卷2015-2016学年江苏省扬州中学高二上期中必修化学试卷2015-2016学年安徽省安庆市怀宁县高河中学高二上期末化学试卷2015-2016学年福建省八县一中高二上学期期末考试化学试卷2016-2017学年山东省德州市陵城一中高二上10月月考化学试卷2016-2017学年陕西西藏民族学院附中高二上月考二化学卷2017届浙江省温州中学高三3月高考模拟化学试卷广东省广州市第二中学2016-2017学年高二下学期期中考试化学试题浙江省东阳中学2016-2017学年高二下学期期中考试化学试题浙江省2018版考前特训(2017年10月)学考70快练:原电池山东省枣庄市第八中学南校区高二10月份月考化学试题福建省惠安惠南中学2017-2018学年高二10月月考(理)化学试题山东省锦泽技工学校2017-2018学年高二10月月考化学试题福建省闽侯第六中学2017-2018学年高二12月月考化学试题浙江省宁波市北仑中学2018-2019学年高二上学期期初返校考试化学试题吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题(已下线)2018年11月21日 《每日一题》人教选修4-原电池工作原理甘肃省武威市第十八中学2018-2019学年高二上学期期末考试化学试题【全国百强校】重庆市第八中学2018-2019学年高二上学期期中考试化学试题【校级联考】黑龙江省龙东南七校2018-2019学年高二上学期期末联考化学试题陕西省咸阳市西藏民族大学附属中学2019-2020学年高二上学期第二次月考化学试题山西省应县第一中学校2019-2020学年高二上学期第四次月考化学试题云南省西双版纳傣族自治州勐腊县第一中学2019-2020学年高二上学期期末考试化学试题内蒙古赤峰市宁城县2019-2020学年高二上学期期末考试化学试题江苏省宿豫中学2019-2020学年度高二下学期调研测试(实验班)化学试题贵州省遵义市航天高级中学2020-2021学年高二上学期第一次月考化学(文)试题黑龙江省农垦建三江管理局第一高级中学2020-2021学年高二上学期期中考试化学试题河北省石家庄市藁城区第一中学2019-2020学年高二上学期第三次月考化学试题内蒙古通辽市科尔沁区大林高中2020-2021学年高二4月月考化学试题2011年全国高中学生化学素质和实验能力竞赛(广东初赛B组)试题(已下线)1.2.1 原电池的工作原理(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)河北省顺平县中学2021-2022学年高二上学期第一次月考化学试题广东省揭阳市惠来县第一中学2021-2022学年高二上学期第二次阶段考试化学试题(已下线)第08练 以新型化学电源及电极反应式的书写突破原电池原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)4.1.1 原电池的工作原理-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)福建省南安市柳城中学2021-2022学年高二上学期期中考试化学试题
名校
7 . 肼-空气燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示,设 为阿伏加德罗常数的值。下列叙述不正确的是
为阿伏加德罗常数的值。下列叙述不正确的是
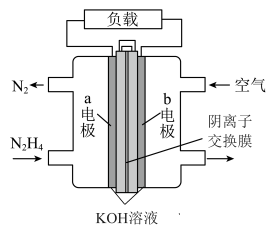
 为阿伏加德罗常数的值。下列叙述不正确的是
为阿伏加德罗常数的值。下列叙述不正确的是
| A.b电极为正极 |
B.a电极的电极反应式为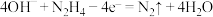 |
C.理论上当燃料电池消耗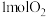 时,电路中转移4 时,电路中转移4 个电子 个电子 |
| D.工作一段时间后,KOH溶液的浓度基本不变 |
您最近一年使用:0次
2023-04-27更新
|
221次组卷
|
3卷引用:四川省资阳市乐至中学2022-2023学年高一下学期期中考试化学试题
名校
8 . 热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水 混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为
混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为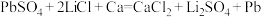 ,下列有关说法正确的是
,下列有关说法正确的是
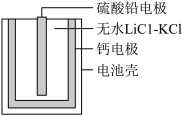
 混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为
混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为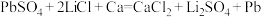 ,下列有关说法正确的是
,下列有关说法正确的是
| A.该电池在常温时就能正常工作 |
B.放电过程中, 向正极移动 向正极移动 |
C.正极反应式: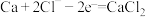 |
| D.每转移0.4mol电子,理论上生成41.4gPb |
您最近一年使用:0次
2023-04-27更新
|
300次组卷
|
2卷引用:四川省宜宾市第四中学校2022-2023学年高一下学期5月期中考试化学试题
名校
9 . 某化学兴趣小组为了探索Zn电极在原电池中的作用,设计并进行了以下一系列实验。
已知:Zn与Al的化学性质基本相似, 。
。
回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为___________ 。
②每转移0.1 mol电子,此时负极材料减少的质量为___________ g。
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为___________ 。
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
②石墨电极上发生___________ (填“氧化”或“还原”)反应。
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为___________ 。
②外电路中电子的流动方向为___________ 。
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为___________ 。
已知:Zn与Al的化学性质基本相似,
 。
。回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为
②每转移0.1 mol电子,此时负极材料减少的质量为
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将
②石墨电极上发生
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为
②外电路中电子的流动方向为
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为
您最近一年使用:0次
2023-04-18更新
|
360次组卷
|
7卷引用:四川省峨眉第二中学校2022-2023学年高一下学期4月月考化学试题
名校
解题方法
10 . Fe-Cu原电池的示意图如图,电池工作时,下列说法正确的是

| A.Fe电极为正极 |
| B.Cu电极上发生还原反应 |
C. 移向Fe电极 移向Fe电极 |
| D.外电路中电子的流动方向:Cu→导线→Fe |
您最近一年使用:0次
2023-04-18更新
|
330次组卷
|
10卷引用:四川省峨眉第二中学校2022-2023学年高一下学期4月月考化学试题
四川省峨眉第二中学校2022-2023学年高一下学期4月月考化学试题河北省2022-2023学年高一下学期期中考试化学试题河北省沧州市沧县中学2022-2023学年高一下学期期中考试化学试题陕西省西安市第八十三中学2022-2023学年高一下学期中考试化学试题广东省汕头市2022-2023学年高一下学期4月期中考试化学试题湖南省怀化市溆浦县玉潭高级中学2022-2023学年高一下学期第一次月考化学试题江西省部分学校2022-2023学年高一下学期4月期中联考化学试题(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)吉林省长春外国语学校2023-2024学年高二上学期11月期中考试化学试题山东省泰安市宁阳四中2023-2024学年高二上学期期末化学模拟试卷



