22-23高一下·广东深圳·期中
名校
1 . 电池是人类生产和生活中的重要能量来源。人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。
(1)知识源于实践。学习原电池知识后,某学习小组以 和
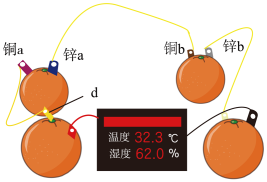
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是_______(填字母)。
(3)将 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
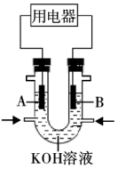
实验测得电子定向移向 电极,则
电极,则_______ (填“ ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为_______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: ,请回答下列问题:
,请回答下列问题:
①放电时,正极反应式为_______ 。
②放电时,负极附近溶液的碱性_______ 。(填“增强”或“减弱”)
(5) 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
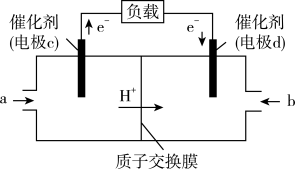
电池总反应为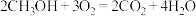 ,则
,则 电极反应式为
电极反应式为_______ ,若线路中转移 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为_______  。
。
(1)知识源于实践。学习原电池知识后,某学习小组以
 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
A.每个水果果汁中的 移向正极 移向正极 |
B.锌 、 、 发生的电极反应式为 发生的电极反应式为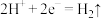 |
C.四个水果电池串联,则电极 为铜片 为铜片 |
D.铜 为电池正极,发生氧化反应 为电池正极,发生氧化反应 |
| A.锌锰电池工作一段时间后碳棒会变细 |
| B.氢氧燃料电池具有高效的特点,能量转化率可达100% |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
D.铅蓄电池负极是 ,正极是 ,正极是 |
 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
实验测得电子定向移向
 电极,则
电极,则 ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
 ,请回答下列问题:
,请回答下列问题:①放电时,正极反应式为
②放电时,负极附近溶液的碱性
(5)
 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
电池总反应为
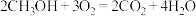 ,则
,则 电极反应式为
电极反应式为 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为 。
。
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
(1)用下图装置探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积,记录实验据如下表:
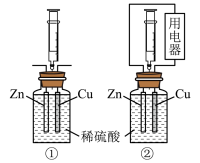
下列说法不正确 的是_______。
(2) 还原
还原 电化学法制备甲醇
电化学法制备甲醇 的工作原理如图所示:
的工作原理如图所示:

通入 的一端是电池的
的一端是电池的_______ 极(填“正”或“负”),电池工作过程中 通过质子膜向
通过质子膜向_______ (填“左”或者“右”)移动,通入 的一端发生的电极反应式为
的一端发生的电极反应式为_______ 。
(1)用下图装置探究原电池中的能量转化。图中注射器用来收集气体并读取气体体积,记录实验据如下表:

| 实验 数据 时间  | ① | ② | ||
气体体积 | 溶液温度/℃ | 气体体积 | 溶液温度/℃ | |
| 0 | 0 | 22.0 | 0 | 22.0 |
| 8.5 | 30 | 24.8 | 50 | 23.8 |
| 10.5 | 50 | 26.0 | - | - |
A. 内,生成气体的平均速率①<② 内,生成气体的平均速率①<② |
| B.时间相同时,对比两装置的溶液温度,说明反应释放的总能量①>② |
| C.生成气体体积相同时,对比两装置的溶液温度,说明②中反应的化学能部分转化为电能 |
D.两装置中的 表面均有气泡产生 表面均有气泡产生 |
 还原
还原 电化学法制备甲醇
电化学法制备甲醇 的工作原理如图所示:
的工作原理如图所示:
通入
 的一端是电池的
的一端是电池的 通过质子膜向
通过质子膜向 的一端发生的电极反应式为
的一端发生的电极反应式为
您最近一年使用:0次
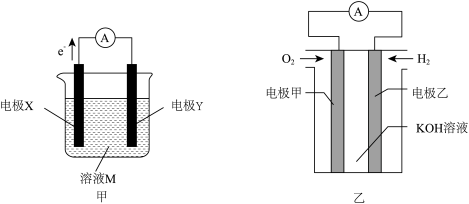
3 . 原电池是利用氧化还原反应设计的装置,该装置的特点是使氧化反应和还原反应在两个电极进行,“迫使”电子沿着特定的路线移动,从而产生电能。甲、乙两个原电池装置如图所示:
(1)若装置甲的溶液M为稀硫酸,两个电极采用镁棒和铝棒。
①电极X为_______ (填“正极”或“负极”),该电极反应式为_______ 。
②该电池的正极是_______ (填“镁棒”或“铝棒”),该电极产物W是_______ (填化学式)。
③该原电池总反应的化学方程式是_______ 。
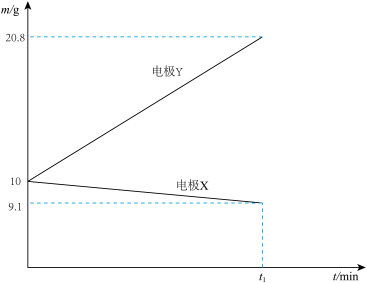
(2)若装置甲中两电极质量变化与时间的关系如图所示,其中一个电极为Ag电极,则该电池的电解质溶液为_______ (填化学式)溶液,电极X为_______ (填字母)
(3)将(1)中原电池生成的气体产物W通入装置乙中可制备燃料电池。
①正极为_______ (填“电极甲”或“电极乙”),该电极发生_______ (填“氧化反应”或“还原反应”)。
②该电池工作时,外电路中电子由_______ (填“电极甲”或“电极乙”,下同)流出;电解质溶液中的 移向
移向_______ 。
(1)若装置甲的溶液M为稀硫酸,两个电极采用镁棒和铝棒。
①电极X为
②该电池的正极是
③该原电池总反应的化学方程式是
(2)若装置甲中两电极质量变化与时间的关系如图所示,其中一个电极为Ag电极,则该电池的电解质溶液为
(3)将(1)中原电池生成的气体产物W通入装置乙中可制备燃料电池。
①正极为
②该电池工作时,外电路中电子由
 移向
移向
您最近一年使用:0次
2023-08-20更新
|
262次组卷
|
5卷引用:海南省部分学校2022-2023学年高一下学期7月期末考试化学试题
海南省部分学校2022-2023学年高一下学期7月期末考试化学试题(已下线)猜想04 化学反应与热能、电能(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)(已下线)清单03 化学反应与能量(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)重难点03 原电池的工作原理与相关判断-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
解题方法
4 . 回答下列问题:
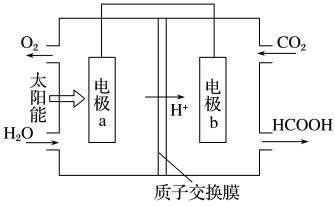
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作____ 极,表面发生的电极反应为____ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
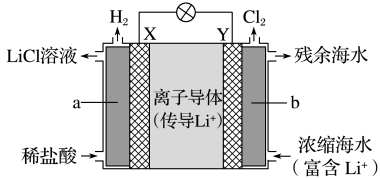
①X为____ 极,Y极反应式为_____ 。
②Y极生成1molCl2时,____ molLi+移向____ (填“X”或“Y”)极。
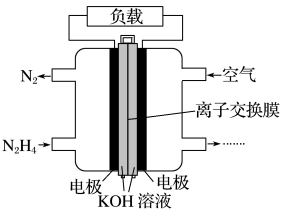
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为____ ;正极反应式为____ 。
(4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。
①负极反应式为_____ ;
②正极反应式为_____ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1molCl2时,
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为

(4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。
①负极反应式为
②正极反应式为
您最近一年使用:0次
名校
5 . 盐酸羟胺 主要用作还原剂和定影剂。以外排烟气中的
主要用作还原剂和定影剂。以外排烟气中的 以及
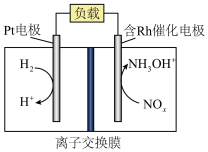
以及 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
 主要用作还原剂和定影剂。以外排烟气中的
主要用作还原剂和定影剂。以外排烟气中的 以及
以及 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
A.制备总反应方程式为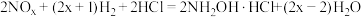 |
| B.该电化学装置中的离子交换膜最好选择质子交换膜 |
| C.制备过程中,Pt电极所在极室溶液的pH基本保持不变 |
D.每生成1mol盐酸羟胺,电路中转移电子的物质的量: |
您最近一年使用:0次
6 . 合成氨对人类生存具有重大意义:
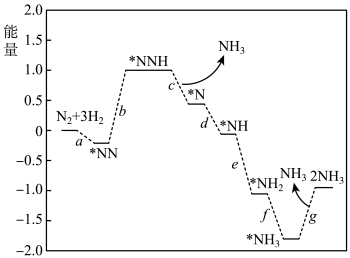
(1)传统工业合成法:反应为N2(g)+3H2(g) 2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
①N2的电子式是___ 。
②写出步骤b的化学方程式___ 。
③由图象可知合成氨反应的∆H__ 0(填“>”、“<”或“=”)。
④工业生产中,除了温度采用400℃—500℃外,促进该反应正向进行的措施是(至少两点)___ 。
(2)电化学制备方法:目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域发生反应的离子方程式是___ 。
②溶液中H+的移动方向是___ (填“向左”或“向右”)。
③下列说法正确的是___ 。
A.该装置可以实现电能转化为化学能
B.电极a是燃料电池的负极
C.该方法相较于传统工业合成方法具有条件温和,对环境友好等优点
(1)传统工业合成法:反应为N2(g)+3H2(g)
 2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
2NH3(g) ∆H。科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
①N2的电子式是
②写出步骤b的化学方程式
③由图象可知合成氨反应的∆H
④工业生产中,除了温度采用400℃—500℃外,促进该反应正向进行的措施是(至少两点)
(2)电化学制备方法:目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域发生反应的离子方程式是
②溶液中H+的移动方向是
③下列说法正确的是
A.该装置可以实现电能转化为化学能
B.电极a是燃料电池的负极
C.该方法相较于传统工业合成方法具有条件温和,对环境友好等优点
您最近一年使用:0次
名校
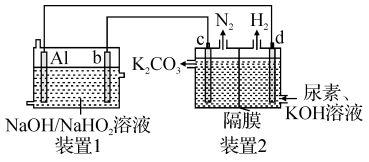
7 . 目前研究比较热门的Al—H2O2电池,其电池总反应为2Al+3HO =2Al
=2Al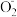 +OH-+H2O。现以Al—H2O2电池电解尿素[CO(NH2)2]的碱性溶液制备氢气(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法正确的是
+OH-+H2O。现以Al—H2O2电池电解尿素[CO(NH2)2]的碱性溶液制备氢气(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法正确的是
 =2Al
=2Al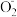 +OH-+H2O。现以Al—H2O2电池电解尿素[CO(NH2)2]的碱性溶液制备氢气(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法正确的是
+OH-+H2O。现以Al—H2O2电池电解尿素[CO(NH2)2]的碱性溶液制备氢气(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法正确的是
| A.Al为负极,c为阴极 |
| B.装置1中OH-移向电极b |
C.电极c的电极反应式为CO(NH2)2-6e-+8OH-=CO +N2+6H2O +N2+6H2O |
| D.通电一段时间后,若Al电极的质量减轻5.4g,则d电极产生H26.72L |
您最近一年使用:0次
2021-09-11更新
|
866次组卷
|
4卷引用:湖北省新高考联考协作体2021-2022学年高三上学期起点考试化学试题
湖北省新高考联考协作体2021-2022学年高三上学期起点考试化学试题湖北省阳新高中2021-2022学年高二上学期9月月考化学试题(已下线)专题08 电化学之电解池-【微专题·大素养】备战2022年高考化学讲透提分要点湖北省枣阳市第一中学2022-2023学年高三上学期9月月考化学试题
解题方法
8 . 某硫酸工厂运用电化学原理设计了如图所示的装置,实现了用SO2发电的同时制备硫酸。图中电极是含催化剂、多孔吸附性的惰性材料。下列说法正确的是
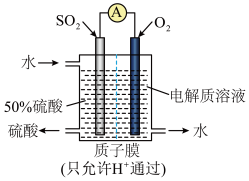

| A.通入SO2气体的一极是负极,发生还原反应 |
| B.正极的电极反应:O2+4e−=2O2− |
| C.该装置工作时的总反应:2SO2+O2+2H2O=2H2SO4 |
| D.氢离子向负极区移动,与负极生成的SO42−结合形成硫酸 |
您最近一年使用:0次
解题方法
9 . CO是一种重要的能源物质。
(1)下列反应原理适合实验室制备CO的是_______ (填选项字母)。
A.C+H2O CO+H2B.2C+O2
CO+H2B.2C+O2 2CO C.HCOOH
2CO C.HCOOH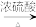 CO+H2O
CO+H2O
(2)用于检测CO含量的某气敏传感器的工作原理如图所示。

①该装置工作时,将_______ 能转化为______ 能。
②工作时,电极 I 作____ 极,电极 II 上的电极反应式为_____________ 。
③向电极 I 缓缓通入10 L 混合气体 ( 其他气体不参加反应)后,测得电路中通过2 mole-,则该混合气体中CO的含量为___ mol/L
(1)下列反应原理适合实验室制备CO的是
A.C+H2O
 CO+H2B.2C+O2
CO+H2B.2C+O2 2CO C.HCOOH
2CO C.HCOOH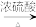 CO+H2O
CO+H2O(2)用于检测CO含量的某气敏传感器的工作原理如图所示。

①该装置工作时,将
②工作时,电极 I 作
③向电极 I 缓缓通入10 L 混合气体 ( 其他气体不参加反应)后,测得电路中通过2 mole-,则该混合气体中CO的含量为
您最近一年使用:0次
解题方法
10 . 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
由此可判断这四种金属的活动性顺序是
| 实验 | |||
| 装置 | 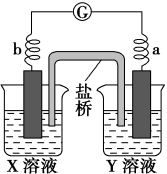 | 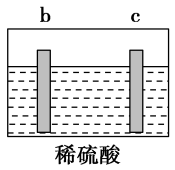 | 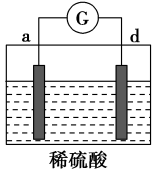 |
| 部分实验现象 | a极质量减小,b极质量增大 | b上有气体产生,c上无变化 | 在导线中,电流从a极流向d极 |
| A.a>b>c>d | B.b>c>d>a |
| C.d>a>b>c | D.a>b>d>c |
您最近一年使用:0次



