名校
解题方法
1 . Ⅰ.回答下列问题
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:
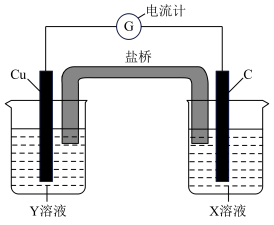
①写出电极反应式。正极:_______ ;负极:_______ 。
②图中X溶液的溶质是_______ (填化学式,下同),Y溶液的溶质是_______ 。
③原电池工作时,盐桥中的_______ (填“阳”或“阴”)离子向X溶液方向移动。
(2)控制合适的条件将反应2Fe3++2I-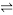 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:

①反应开始时,乙中石墨电极上发生_______ (填“氧化”或“还原”,下同)反应,电极反应式为_______ 。甲中石墨电极上发生_______ 反应,电极反应式为_______ 。
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作_______ (填“正”或“负”)极,该电极的电极反应式为_______ 。
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_______ 。
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式_______ 。实验结果未见到蓝色。
(5)乙同学认为甲同学的实验方案有问题,理由是_______ 。请设计原电池证明Ag+也能氧化 Iˉ,画出装置图,并标明电极材料及电解质溶液。______
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:

①写出电极反应式。正极:
②图中X溶液的溶质是
③原电池工作时,盐桥中的
(2)控制合适的条件将反应2Fe3++2I-
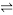 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:
①反应开始时,乙中石墨电极上发生
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式
(5)乙同学认为甲同学的实验方案有问题,理由是
您最近一年使用:0次
解题方法
2 . 根据信息填空
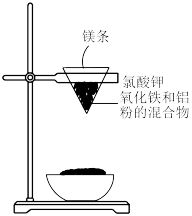
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:_______ 。
(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液______ 。该原电池中,三价铁离子向_______ (填“正极”或“负极”)移动。负极的电极反应式为_______

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式_______ 。
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法_______ (只填一种方法)。
(1)用如图所示的装置进行铝热法炼铁实验,写出铝热法炼铁反应的化学方程式:

(2)已知:Fe+2FeCl3=3FeCl2,利用这一反应,设计一个原电池,画出示意图,标明电极材料名称,电解质溶液

(3)古代《药性论》中有关铅丹(Pb3O4)的描述是治惊悸狂走,呕逆,消渴,铅丹(Pb3O4)也可作为防锈用涂料,呈红褐色,又名红丹。
①铅丹可用PbO在空气中加热制备,请写出有关反应的化学方程式
②铅丹曾用于铁制品防锈,请举例说明铁制品防锈的其它方法
您最近一年使用:0次
名校
解题方法
3 . 利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是


| A.a极的电极反应式为:CH4-8e-+4O2-=CO2+2H2O |
| B.A膜和C均为阳离子交换膜 |
| C.可用铁电极替换Y极室的石墨电极 |
| D.a极上通入2.24L(标准状况)甲烷,X极室Ca2+减少0.8mol |
您最近一年使用:0次
解题方法
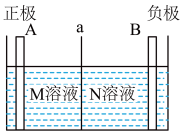
4 . 某实验小组用铜和 溶液来制备
溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
 溶液来制备
溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
| A.电极A为铜 |
B.a为阴离子交换膜,电解质N为 |
| C.理论上每生成1molN时会消耗1molM |
| D.当B电极质量减少6.4克,则N溶液质量增加6.4克 |
您最近一年使用:0次
2022-08-18更新
|
167次组卷
|
2卷引用:贵州省遵义市新高考协作体2022-2023学年高三上学期入学质量检测理综化学试题
2022·全国·模拟预测
解题方法
5 . 2022年,冬投拥有自主知识产权的“铁—冬投产号”电池产能和发电量为一粒电池,并为电池连续生产,电池电量和产量将在全国范围内正常生产。的罐体,电池结构如不同所示,该电池的法拉第一次效率为60% 。(法拉第一次效率=mnF/(It) ,m——生成物物质的量,n——生成一个转移的电子数,F ——法线数字即是摩尔电子的第一个时间,我为电流,t )下面是正确的
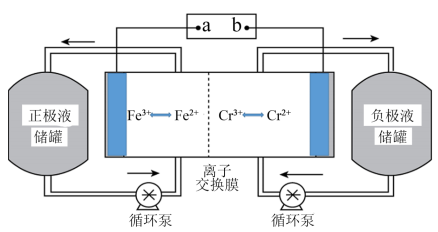

A.电池的工作原理为Fe 2+ +Cr 3+ Fe3+ +Cr 2+ Fe3+ +Cr 2+ |
| B.装置中的离子交换膜为水果交换膜 |
| C.有10mol离子通过交换膜时,可制备6g绿氢 |
| D.相对于锂电,铁铬液流电池成本低,安全性高,能量密度高 |
您最近一年使用:0次
解题方法
6 . 回答下列问题:
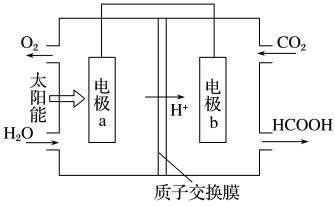
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作____ 极,表面发生的电极反应为____ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
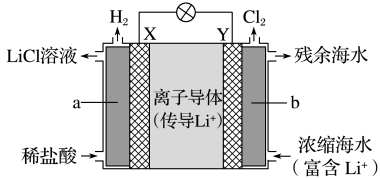
①X为____ 极,Y极反应式为_____ 。
②Y极生成1molCl2时,____ molLi+移向____ (填“X”或“Y”)极。
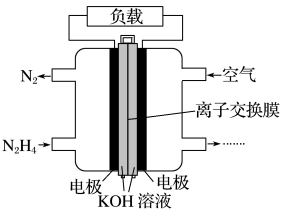
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为____ ;正极反应式为____ 。
(4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。
①负极反应式为_____ ;
②正极反应式为_____ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1molCl2时,
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为

(4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。
①负极反应式为
②正极反应式为
您最近一年使用:0次
解题方法
7 . 我国科学家研究出一种新型电池,可利用太阳光持续完成过氧化氢制备和硫化氢吸收,其工作原理示意图如图所示(HQ和Q代表两种有机物)。下列说法正确的是
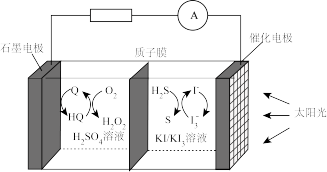

| A.该装置涉及电能直接转化为化学能 |
| B.工作时,溶液中H2SO4的物质的量逐渐减小 |
| C.工作时,理论上生成H2O2和S单质的物质的量相等 |
| D.若导线中流过2mole-,催化电极上有4molI-参与转化 |
您最近一年使用:0次
名校
解题方法
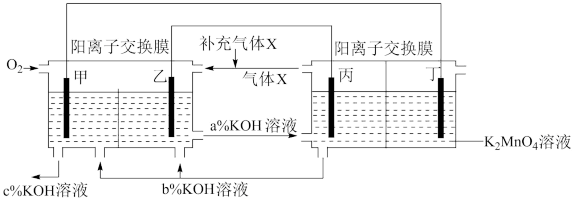
8 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为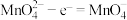 |
C.KOH溶液的质量分数: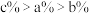 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
669次组卷
|
7卷引用:卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)
解题方法
9 . 盐酸羟胺(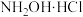 )是一种无机物,可用作合成抗癌药,其化学性质类似
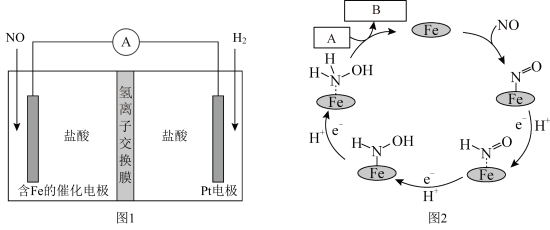
)是一种无机物,可用作合成抗癌药,其化学性质类似 。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
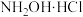 )是一种无机物,可用作合成抗癌药,其化学性质类似
)是一种无机物,可用作合成抗癌药,其化学性质类似 。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
| A.该装置能将电能转化为化学能,Pt电极为阳极 |
B.图2中,A为 ,B为 ,B为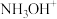 |
C.每制取0.1mol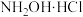 ,有3.36L(标准状况) ,有3.36L(标准状况) 参与反应 参与反应 |
| D.电池工作一段时间后,正极区溶液的pH下降 |
您最近一年使用:0次
解题方法
10 . 物质的化学能可以在不同的条件下转化为热能、电能被人类利用。按要求回答下列问题。
(1)微生物电池是指在微生物作用下将化学能转化为电能的装置。其工作原理如下图所示。
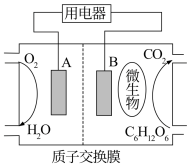
①A为生物燃料电池的_______ (填“正”或“负”)极。
②负极的电极反应式为_______ 。
③放电过程中, 由
由_______ 极区向_______ 极区迁移(填“正”或“负”)。
(2)用阴离子交换膜控制电解液中 的浓度制备纳米
的浓度制备纳米 。反应为
。反应为 ,装置如图。
,装置如图。
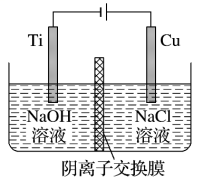
①电解时_______ 通过阴离子交换膜向_______ 极移动。
②阳极电极反应式为_______ 。
③阴极电极反应式为_______ 。
(3)我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(
”电池,以钠箔和多壁碳纳米管(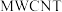 )为电极材料,可选用高氯酸钠-四甘醇二甲醚作电解液。总反应方程式为
)为电极材料,可选用高氯酸钠-四甘醇二甲醚作电解液。总反应方程式为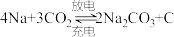 。放电时该电池“吸入”
。放电时该电池“吸入” 。
。
①放电时,正极的电极反应式为_______ 。
②可选用高氯酸钠-四甘醇二甲醚作电解液的理由是_______ 。
(1)微生物电池是指在微生物作用下将化学能转化为电能的装置。其工作原理如下图所示。

①A为生物燃料电池的
②负极的电极反应式为
③放电过程中,
 由
由(2)用阴离子交换膜控制电解液中
 的浓度制备纳米
的浓度制备纳米 。反应为
。反应为 ,装置如图。
,装置如图。
①电解时
②阳极电极反应式为
③阴极电极反应式为
(3)我国科研人员研制出的可充电“
 ”电池,以钠箔和多壁碳纳米管(
”电池,以钠箔和多壁碳纳米管(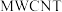 )为电极材料,可选用高氯酸钠-四甘醇二甲醚作电解液。总反应方程式为
)为电极材料,可选用高氯酸钠-四甘醇二甲醚作电解液。总反应方程式为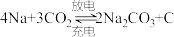 。放电时该电池“吸入”
。放电时该电池“吸入” 。
。①放电时,正极的电极反应式为
②可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
您最近一年使用:0次



