名校
解题方法
1 . 化学电源在生产生活中有着广泛的应用,请回答下列问颕:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
(2)电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极分别为 和Zn,电解液为KOH溶液。工作时电池总反应为:
和Zn,电解液为KOH溶液。工作时电池总反应为: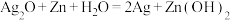 。
。
①工作时电流从___________ 极流向___________ 极(两空均选填“ ”或“Zn”);
”或“Zn”);
②负极的电极反应式为:___________ ;
③工作时电池正极区的pH___________ (选填“增大”“减小”或“不变”);
④外电路中每通过0.2mol电子,锌的质量理论上减少___________ g。
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“ ”设计一种化学电池(正极材料用石墨棒),回答下列问题:
”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是___________ (填化学式),电解质溶液是___________ (填化学式)溶液。
②正极上发生的电极反应为___________ 。
③若导线上转移的电子为1mol,则消耗的金属铜的质量为___________ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
A.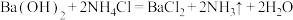 |
B. |
C. |
D. |
 和Zn,电解液为KOH溶液。工作时电池总反应为:
和Zn,电解液为KOH溶液。工作时电池总反应为: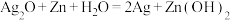 。
。①工作时电流从
 ”或“Zn”);
”或“Zn”);②负极的电极反应式为:
③工作时电池正极区的pH
④外电路中每通过0.2mol电子,锌的质量理论上减少
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“
 ”设计一种化学电池(正极材料用石墨棒),回答下列问题:
”设计一种化学电池(正极材料用石墨棒),回答下列问题:①该电池的负极材料是
②正极上发生的电极反应为
③若导线上转移的电子为1mol,则消耗的金属铜的质量为
您最近半年使用:0次
名校
2 . 硫酸亚铁铵,俗名为莫尔盐[ ],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
 ],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
],它是一种蓝绿色无机复盐,也是一种重要的化工原料,以下制备该物质的说法中错误的是
A.步骤Ⅱ到步骤Ⅲ的操作,缩短了溶液与空气接触的时间,降低 被氧化的风险 被氧化的风险 |
| B.玻璃棒缠绕铜丝的主要目的是铜丝和铁粉接触形成原电池,加快化学反应速率 |
C.步骤Ⅱ到步骤Ⅳ发生的反应方程式为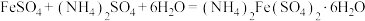 |
| D.从溶液中获得莫尔盐,可以直接经过蒸发结晶的实验操作获得纯净的莫尔盐 |
您最近半年使用:0次
2024-04-22更新
|
215次组卷
|
2卷引用:2024届河北省雄安新区雄安部分高中高三下学期一模化学试题
3 . 我国科学家研发了一种可逆电池装置,充电时该装置可吸收CO2合成甲酸,其具体工作原理如图所示。已知将阴离子、阳离子复合组成双极膜,双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法错误的是
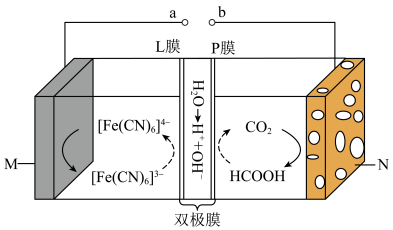
| A.L膜是阴离子膜,P膜是阳离子膜 |
B.充电时,N电极上发生的电极反应式为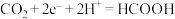 |
| C.放电时,电子由a流向电源的M极 |
| D.充电时,外电路中每通过1mol电子,理论上复合膜层间有0.5molH2O解离 |
您最近半年使用:0次
2024-03-27更新
|
252次组卷
|
2卷引用:2024届河北省张家口市高三下学期一模化学试题
名校
4 . 某低成本储能电池原理如图所示。下列说法正确的是
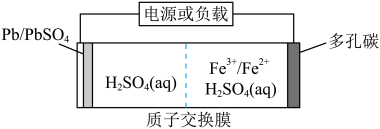
| A.放电时右边电极的电势高于左边 |
| B.储能过程中化学能转变为电能 |
C.放电时右侧 通过质子交换膜移向左侧 通过质子交换膜移向左侧 |
D.充电总反应: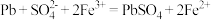 |
您最近半年使用:0次
2024-03-11更新
|
121次组卷
|
2卷引用:河北省唐山市第一中学2023-2024学年高二下学期开学化学试卷
解题方法
5 . 下列实验方案、对应现象和结论有错误的是
| 实验方案 | 现象 | 结论 | |
| A | 将注射器充满 气体,再将活塞往里推,压缩体积 气体,再将活塞往里推,压缩体积 | 从注射器侧面观察,气体颜色加深 | 加压平衡向生成 气体的方向移动 气体的方向移动 |
| B | 用铁片、铜片、稀硫酸等组成原电池 | 铜片表面有气泡产生 | 铁的金属性强于铜 |
| C | 室温下,测量等浓度的KA、KB两种弱酸盐溶液的pH | 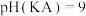 、 、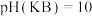 | 水解能力: |
| D | 向沸水中滴加5~6滴饱和 溶液,持续煮沸 溶液,持续煮沸 | 溶液先变成红褐色再析出沉淀 |  先水解得 先水解得 胶体再聚集成 胶体再聚集成 沉淀 沉淀 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法不正确的是
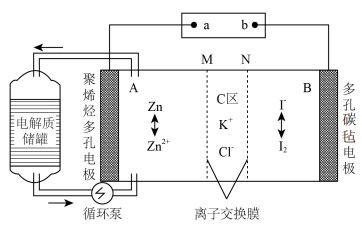

| A.放电时,B电极反应式:I2+2e-=2I- |
| B.放电时,电解质储罐中离子总浓度增大 |
| C.M为阴离子交换膜,N为阳离子交换膜 |
| D.充电时,A极增重65g时,C区增加的离子数为2NA |
您最近半年使用:0次
名校
7 . 银铝电池具有能量密度高的优点,其工作原理如图所示,电池放电时的反应为2Al+3Ag2O+2NaOH+3H2O=2Na[Al(OH)4]+6Ag。
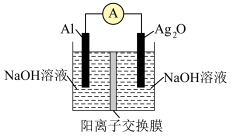
下列说法错误的是

下列说法错误的是
| A.Al为电源负极 | B.正极反应为Ag2O+2e-+H2O=2Ag+2OH- |
| C.放电时负极区pH增大 | D.放电时Na+通过交换膜向右侧移动 |
您最近半年使用:0次
2023-11-10更新
|
683次组卷
|
4卷引用:河北省定州市2023-2024学年高二上学期11月期中考试化学试题
名校
8 . 高铁电池的总反应为: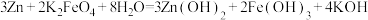 。如图是高铁电池的模拟实验装置,下列说法不正确的是
。如图是高铁电池的模拟实验装置,下列说法不正确的是

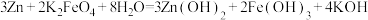 。如图是高铁电池的模拟实验装置,下列说法不正确的是
。如图是高铁电池的模拟实验装置,下列说法不正确的是
A.该电池放电时正极的电极反应式为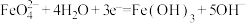 |
B. 被氧化,转移3mol电子 被氧化,转移3mol电子 |
| C.放电过程中负极附近溶液的pH减小 |
| D.盐桥中盛有饱和KCl溶液,此盐桥中氯离子向右移动 |
您最近半年使用:0次
2023-11-09更新
|
803次组卷
|
2卷引用:河北省唐山市十县一中联盟2023-2024学年高二上学期期中考试化学试题
名校
9 . 汽车的启动电源常用铅酸蓄电池,该电池在放电时的总反应为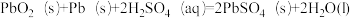 。
。
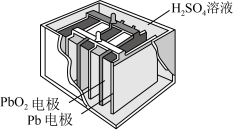
下列说法正确的是
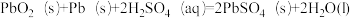 。
。
下列说法正确的是
| A.该铅酸蓄电池属于一次电池 |
B.负极的电极反应式为 |
| C.铅酸蓄电池放电时,每转移0.2mol电子消耗0.4molH2SO4 |
| D.电池放电时,两电极质量均增加,且每转移1mol电子,电池正极质量增加32g |
您最近半年使用:0次
名校
解题方法
10 . 回答下列问题:
(1)电解硫酸亚铁和硫酸铝溶液得到液体聚合硫酸铝铁[AlaFeb(OH)m(SO4)n]。装置如图1所示(阴离子交换膜只允许阴离子通过,电极为惰性电极):
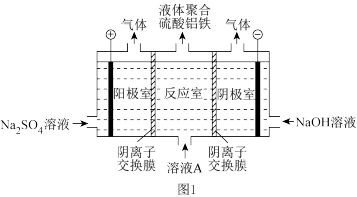
①电解过程阳极室溶液 pH 的变化是___________ (填“增大”、“减小”或“不变”)。
②简述在反应室中生成液体聚合硫酸铝铁的原理___________ 。
(2)如图2是一种用电解原理来制备 H2O2,并用产生的 H2O2处理废氨水的装置。

①Ir-Ru 惰性电极吸附 O2生成 H2O2,其电极反应式为___________ 。。
②理论上电路中每转移3 mol e-,最多可以处理废氨水中溶质(以NH3计)的质量是___________ g。
(3)为探究金属的腐蚀情况,某同学取一张用饱和 NaCl 溶液浸湿的石蕊试纸,平铺在一块金属板上,按如图3所示的方法连接电路。
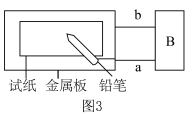
①若试纸为红色石蕊试纸,金属板为一锌片,B 处为一灵敏电流计,接通电路,将铅笔芯(主要成分为石墨)放置在试纸上一段时间,发现电流计指针发生偏转,则铅笔芯与试纸接触处颜色___________ 。
②若金属板为一铂片,B 处为一直流电源,接通电源后,若试纸为蓝色石蕊试纸,将铅笔芯放置在试纸上一段时间后,若接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色,则铅笔芯与试纸接触处的电极反应式为___________ 。
(1)电解硫酸亚铁和硫酸铝溶液得到液体聚合硫酸铝铁[AlaFeb(OH)m(SO4)n]。装置如图1所示(阴离子交换膜只允许阴离子通过,电极为惰性电极):

①电解过程阳极室溶液 pH 的变化是
②简述在反应室中生成液体聚合硫酸铝铁的原理
(2)如图2是一种用电解原理来制备 H2O2,并用产生的 H2O2处理废氨水的装置。

①Ir-Ru 惰性电极吸附 O2生成 H2O2,其电极反应式为
②理论上电路中每转移3 mol e-,最多可以处理废氨水中溶质(以NH3计)的质量是
(3)为探究金属的腐蚀情况,某同学取一张用饱和 NaCl 溶液浸湿的石蕊试纸,平铺在一块金属板上,按如图3所示的方法连接电路。

①若试纸为红色石蕊试纸,金属板为一锌片,B 处为一灵敏电流计,接通电路,将铅笔芯(主要成分为石墨)放置在试纸上一段时间,发现电流计指针发生偏转,则铅笔芯与试纸接触处颜色
②若金属板为一铂片,B 处为一直流电源,接通电源后,若试纸为蓝色石蕊试纸,将铅笔芯放置在试纸上一段时间后,若接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色,则铅笔芯与试纸接触处的电极反应式为
您最近半年使用:0次
2023-09-19更新
|
70次组卷
|
2卷引用:河北省唐县第一中学2023-2024学年高二上学期9月月考化学试题



