名校
解题方法
1 . 用于驱动潜艇的液氨—液氧燃料电池示意图如下图所示,下列有关说法正确的是
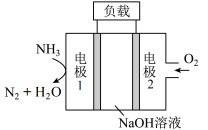
| A.电极2发生氧化反应 |
B.电池工作时, 向负极移动 向负极移动 |
C.电极1发生的电极反应为 |
D.当电路中转移 ,消耗氧气的体积为 ,消耗氧气的体积为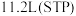 |
您最近半年使用:0次
名校
2 . 关于下列实验事实的给出的解释或结论不正确的是
| 选项 | 实验事实 | 解释或结论 |
| A. |  与 与 溶液反应产生黄色沉淀和气体( 溶液反应产生黄色沉淀和气体( ) ) | 反应生成难溶的 ,增大了 ,增大了 的还原性 的还原性 |
| B. | 将 气体通入 气体通入 溶液中,溶液先变为红棕色(含 溶液中,溶液先变为红棕色(含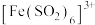 ),过一段时间又变成浅绿色 ),过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| C. | 取一定量固体于试管中,加入浓 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 | 该固体为铵盐 |
| D. | 将变黑的银器放入装满食盐水的铝盆中,一段时间后银器恢复往日光泽 | 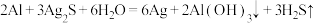 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . 铝硫二次电池是一种具有高能量密度、廉价原材料、有前途的替代储能装置,一种铝硫电池如图所示,放电时的电池总反应为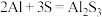 。下列说法错误的是
。下列说法错误的是

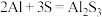 。下列说法错误的是
。下列说法错误的是
A.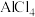 和 和 中均存在配位键 中均存在配位键 |
| B.该电池电解质区域所用溶剂不可以为水 |
C.电池放电时的正极反应式为 |
| D.用该电池保护地下铁管道不被腐蚀,铁管道应连接电池的硫碳电极 |
您最近半年使用:0次
名校
解题方法
4 . 锂二氧化碳电池可在常温下同时实现二氧化碳的锚定与转化,可以在深海作业、火星探测等高二氧化碳的环境中得到应用,电池总反应为:4Li+3CO2  2Li2CO3+C,下列说法错误的是
2Li2CO3+C,下列说法错误的是
 2Li2CO3+C,下列说法错误的是
2Li2CO3+C,下列说法错误的是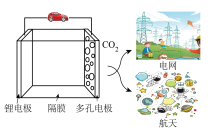
| A.该电池不能用水溶液作为电解液 |
B.放电时,正极的电极反应为: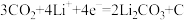 |
| C.充电时,若以铅蓄电池为电源,则锂电极应与Pb极相连接 |
| D.充电时,当生成3.36L(标准状况下) CO2,通过隔膜迁移的Li+数目为0.4NA |
您最近半年使用:0次
2023-12-11更新
|
178次组卷
|
3卷引用:福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题
福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题(已下线)专题07 原电池-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)宁夏开元学校2023-2024学年高二上学期期末考试化学试题
名校
解题方法
5 . 如图装置,能溶解辉铜矿石(主要成分是Cu2S)制得硫酸铜。下列说法正确的是
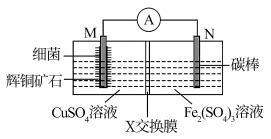

| A.X交换膜可以是阳离子交换膜 |
B.M极上的电极反应式为Cu2S+10e-+4H2O=2Cu2++8H++SO |
| C.为证明右侧产物,可取少量溶液加入K3[Fe(CN)6]溶液,观察是否有蓝色沉淀 |
| D.M极的电势高于N极的电势 |
您最近半年使用:0次
2023-11-11更新
|
313次组卷
|
2卷引用:福建省福州市八县一中2023-2024学年高二上学期11月期中化学试题
名校
6 . 某小组同学实验验证“ ”为可逆反应。
”为可逆反应。
(1)实验验证
实验Ⅰ:将含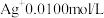 的溶液与
的溶液与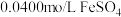 溶液(
溶液( )等体积混合,产生灰黑色沉淀,溶液呈黄色。
)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入 溶液(
溶液( ),固体完全溶解。
),固体完全溶解。
①取Ⅰ中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:___________ 。
②Ⅱ中溶液选用 ,不选用
,不选用 的原因为
的原因为___________ 。
综合上述实验,证实“ ”为可逆反应。
”为可逆反应。
(2)采用电化学装置进行验证。
小组同学设计如图电化学装置进行实验:

①按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为___________ 溶液;b为___________ 溶液;(写a、b化学式)
②再向左侧烧杯中滴加较浓的___________ 溶液(填化学式),产生的现象为___________ ,表明“ ”为可逆反应。
”为可逆反应。
 ”为可逆反应。
”为可逆反应。(1)实验验证
实验Ⅰ:将含
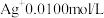 的溶液与
的溶液与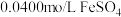 溶液(
溶液( )等体积混合,产生灰黑色沉淀,溶液呈黄色。
)等体积混合,产生灰黑色沉淀,溶液呈黄色。实验Ⅱ:向少量Ag粉中加入
 溶液(
溶液( ),固体完全溶解。
),固体完全溶解。①取Ⅰ中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:
②Ⅱ中溶液选用
 ,不选用
,不选用 的原因为
的原因为综合上述实验,证实“
 ”为可逆反应。
”为可逆反应。(2)采用电化学装置进行验证。
小组同学设计如图电化学装置进行实验:

①按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为
②再向左侧烧杯中滴加较浓的
 ”为可逆反应。
”为可逆反应。
您最近半年使用:0次
名校
解题方法
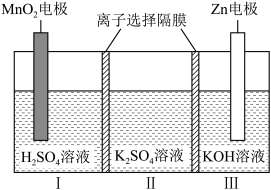
7 . 一种水性电解液 离子选择双隔膜电池如图所示(
离子选择双隔膜电池如图所示( 溶液中,
溶液中, 以
以 存在)。电池放电时,下列叙述正确的是
存在)。电池放电时,下列叙述正确的是
 离子选择双隔膜电池如图所示(
离子选择双隔膜电池如图所示( 溶液中,
溶液中, 以
以 存在)。电池放电时,下列叙述正确的是
存在)。电池放电时,下列叙述正确的是
A.Ⅱ区的 通过隔膜向Ⅲ区迁移 通过隔膜向Ⅲ区迁移 |
B.电子由 电极经外电路流向Zn电极 电极经外电路流向Zn电极 |
C. 电极反应: 电极反应: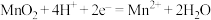 |
| D.Zn电极为负极,发生还原反应 |
您最近半年使用:0次
8 . 下图是飞船和空间站中利用Sabatier反应再生氧气的大体流程。
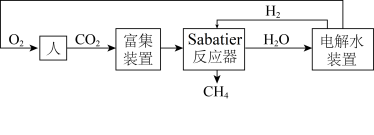
(1)已知:2H2(g)+O2(g) 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1
CH4(g)+2O2(g) CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
则Sabatier反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=___________ 。
(2)二氧化碳的富集装置如图所示。
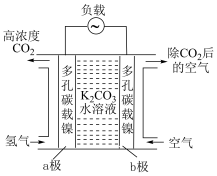
①该富集法采用___________ 原理(填“原电池”或“电解池”)。当a极上消耗1molH2,并保持电解液溶质不变时,b极上除去的CO2在标准状况下的体积为___________ 。
②工作一段时间后,K2CO3溶液的pH___________ (填“变大”“变小”或“不变”)。
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是___________ 。
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是___________ 。
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=___________ (用P0表示)。已知Kp是以分压表示的平衡常数,分压=总压×物质的量分数。
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为___________ (填化学式)。

(1)已知:2H2(g)+O2(g)
 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1CH4(g)+2O2(g)
 CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1则Sabatier反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=(2)二氧化碳的富集装置如图所示。

①该富集法采用
②工作一段时间后,K2CO3溶液的pH
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为
| 离子种类 | H+ | OH- |  SO SO | Cl- |  CO CO | K+ | Na+ |
| 摩尔电导率×104(S·m2·mol-1) | 349.82 | 198.0 | 79.8 | 76.34 | 72.0 | 73.52 | 50.11 |
您最近半年使用:0次
名校
9 . “化学多米诺实验“即只需控制第一个反应,利用反应中气体产生的压力和虹吸作用原理使若干化学实验依次发生。如图是一个“化学多米诺实验”。
已知:①Cu2++4NH3·H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2分解的催化剂)
②A和C中的硫酸溶液浓度相同
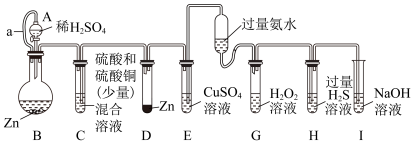
下列有关分析错误的是
已知:①Cu2++4NH3·H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2分解的催化剂)
②A和C中的硫酸溶液浓度相同

下列有关分析错误的是
| A.B装置中反应速率大于D装置中反应速率 |
| B.E装置中现象为试管内蓝色液面下降 |
| C.H装置中出现浅黄色浑浊 |
| D.该实验成功的重要条件是整套装置气密性良好 |
您最近半年使用:0次
2023-09-02更新
|
181次组卷
|
2卷引用:福建省政和县第一中学2023-2024学年高三上学期第一次月考化学试题
10 . 锂硫电池放电过程中正极变化为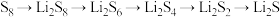 。我国科学家掺入Ni解决
。我国科学家掺入Ni解决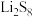 、
、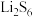 、
、 溶解度小、易透过隔膜的问题。下列说法正确的是
溶解度小、易透过隔膜的问题。下列说法正确的是

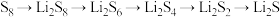 。我国科学家掺入Ni解决
。我国科学家掺入Ni解决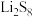 、
、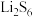 、
、 溶解度小、易透过隔膜的问题。下列说法正确的是
溶解度小、易透过隔膜的问题。下列说法正确的是
A.放电时,负极电解质溶液每增重0.07g,电路转移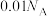 电子 电子 |
B.充电时,电池的总反应方程式为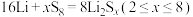 |
| C.Ni对多硫化物的吸附能力相比于石墨烯更小 |
| D.Ni应当掺杂在电池隔膜的正极一侧 |
您最近半年使用:0次



