1 . 下图是飞船和空间站中利用Sabatier反应再生氧气的大体流程。
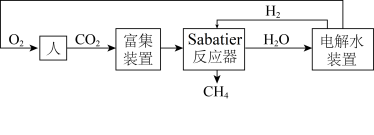
(1)已知:2H2(g)+O2(g) 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1
CH4(g)+2O2(g) CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
则Sabatier反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=___________ 。
(2)二氧化碳的富集装置如图所示。
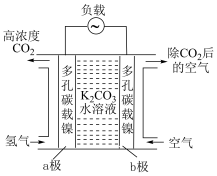
①该富集法采用___________ 原理(填“原电池”或“电解池”)。当a极上消耗1molH2,并保持电解液溶质不变时,b极上除去的CO2在标准状况下的体积为___________ 。
②工作一段时间后,K2CO3溶液的pH___________ (填“变大”“变小”或“不变”)。
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是___________ 。
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是___________ 。
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=___________ (用P0表示)。已知Kp是以分压表示的平衡常数,分压=总压×物质的量分数。
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为___________ (填化学式)。

(1)已知:2H2(g)+O2(g)
 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1CH4(g)+2O2(g)
 CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1则Sabatier反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=(2)二氧化碳的富集装置如图所示。

①该富集法采用
②工作一段时间后,K2CO3溶液的pH
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为
| 离子种类 | H+ | OH- |  SO SO | Cl- |  CO CO | K+ | Na+ |
| 摩尔电导率×104(S·m2·mol-1) | 349.82 | 198.0 | 79.8 | 76.34 | 72.0 | 73.52 | 50.11 |
您最近一年使用:0次
名校
解题方法
2 . 有机物电极材料具有来源丰富、可降解等优点,一种负极材料为固态聚酰亚胺-水系二次电池的结构如图所示。下列说法正确的是
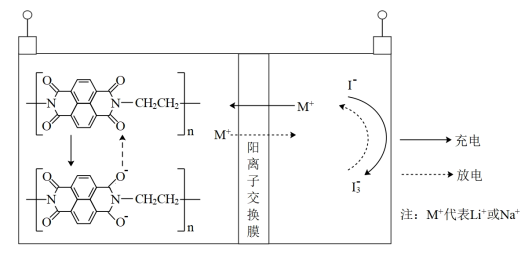

| A.充电时有机电极发生了氧化反应 |
B.充电时每转移 ,右室离子数目减少 ,右室离子数目减少 |
C.放电时负极电极反应为: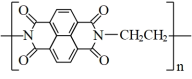 -2e-= -2e-=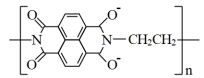 |
D.将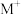 由 由 换成 换成 ,电池的比能量会下降 ,电池的比能量会下降 |
您最近一年使用:0次
2022-04-14更新
|
2564次组卷
|
18卷引用:福建省龙岩第一中学2022届高三毕业班模拟训练(二)化学试题
福建省龙岩第一中学2022届高三毕业班模拟训练(二)化学试题福建省厦门第一中学2022-2023学年高三上学期11月期中考试化学试题广东省佛山市普通高中2022届高三教学质量检测(二)化学试题广东省佛山市2022届高三下学期4月第二次教学质量监测(二模)化学试题(已下线)必刷卷04-2022年高考化学考前信息必刷卷(全国乙卷)(已下线)押江苏卷第12题 电化学及其应用 -备战2022年高考化学临考题号押题(江苏卷)(已下线)【直抵名校】04-备战2022年高考化学名校进阶模拟卷(通用版)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题湖南省岳阳县第一中学2022届高三下学期5月月考化学试题湖南省湘东九校2021-2022学年高二下学期期末联考化学试题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)化学(辽宁A卷)-学易金卷:2023年高考第一次模拟考试卷湖南省株洲市九方中学2022-2023学年高三上学期第四次月考化学试题辽宁省葫芦岛市第一高级中学2022-2023学年高三上学期期末线上教学阶段检测化学试题江苏省常州市第一中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市第二中学2023届高三第七次月考化学试题(已下线)T10-电化学原理山东省滕州市2023-2024学年高三上学期期中考试化学试题
名校
解题方法
3 . 以金属切削废料(由铁屑和镍钴合金、金刚砂组成)为原料回收镍钴生产NiSO4·7H2O和CoCl2·6H2O的工艺如图:
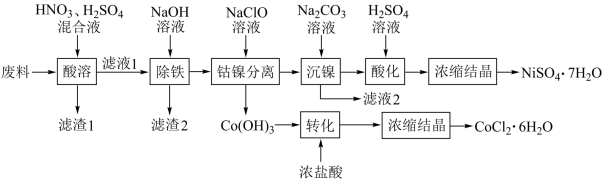
已知:①相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
②常温下,Ksp(NiCO3)=1.0×10-7。
回答下列问题:
(1)将废料研磨成粉的作用是___ 。
(2)理论上“除铁”需控制pH的范围为___ ,“滤渣2”中除Fe(OH)3外,还有少量黄钠铁矾[Na2Fe6(SO4)4(OH)12],写出Fe3+生成黄钠铁矾的离子方程式:___ 。
(3)写出“钴镍分离”时发生反应的离子方程式:___ 。“镍钴分离”后溶液中c(Ni2+)=1.0mol·L-1,若“滤液2”中c(CO )=10-5mol·L-1,则沉镍率=
)=10-5mol·L-1,则沉镍率=___ [沉镍率=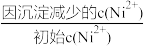 ]。
]。
(4)“转化”时产生的气体为___ 。
(5)碱性镍氢电池是国产比亚迪汽车车载电池之一,其电池反应为:NiOOH+MH Ni(OH)2+M。放电时,负极反应式为
Ni(OH)2+M。放电时,负极反应式为___ 。

已知:①相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Co3+ | Co2+ | Fe3+ | Fe2+ | Ni2+ |
| 开始沉淀的pH | 0.3 | 7.2 | 1.5 | 6.3 | 6.9 |
| 沉淀完全的pH | 1.1 | 9.2 | 2.8 | 8.3 | 8.9 |
回答下列问题:
(1)将废料研磨成粉的作用是
(2)理论上“除铁”需控制pH的范围为
(3)写出“钴镍分离”时发生反应的离子方程式:
 )=10-5mol·L-1,则沉镍率=
)=10-5mol·L-1,则沉镍率=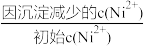 ]。
]。(4)“转化”时产生的气体为
(5)碱性镍氢电池是国产比亚迪汽车车载电池之一,其电池反应为:NiOOH+MH
 Ni(OH)2+M。放电时,负极反应式为
Ni(OH)2+M。放电时,负极反应式为
您最近一年使用:0次
2021-04-07更新
|
514次组卷
|
4卷引用:福建省莆田一中2021届高三模拟质量检测化学试题
福建省莆田一中2021届高三模拟质量检测化学试题湖南省常德市2021届高三第一次(3月)模拟考试化学试题(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)湖南省永州市第一中学2022届高三第二次月考化学试题
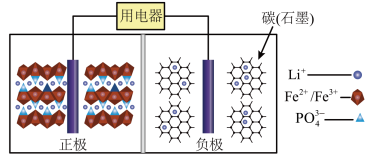
4 . 高能LiFePO4电池多应用于公共交通,结构如图所示。电池中间是聚合物的隔膜,其主要作用是在反应过程中只让Li+通过,原理如下:(1−x)LiFePO4+xFePO4+LixCn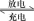 LiFePO4+nC。下列说法
LiFePO4+nC。下列说法错误 的是( )
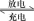 LiFePO4+nC。下列说法
LiFePO4+nC。下列说法
| A.放电时,Li+向正极移动 |
| B.放电时,电子由负极→用电器→正极 |
| C.充电时,阴极反应为xLi++nC+xe-=LixCn |
| D.充电时,阳极质量增重 |
您最近一年使用:0次
2020-03-26更新
|
253次组卷
|
2卷引用:福建省龙岩市2020年高中毕业班3月教学质量检查(全国I卷)理综化学试题



