名校
解题方法
1 . 一种新型微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,下列说法正确的是。
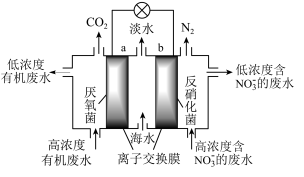
| A.该电池能在高温下工作 |
| B.a极为电池的正极 |
| C.有机废水处理后pH降低 |
D.处理 的电极反应为 的电极反应为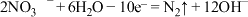 |
您最近半年使用:0次
名校
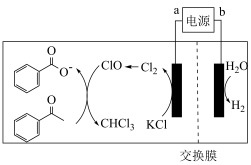
2 . 某高能锂离子电池的总反应为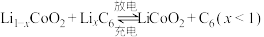 ,以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
,以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
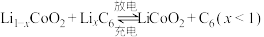 ,以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
,以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
A.锂离子电池放电时, 极质量增加 极质量增加 |
B.锂离子电池充电时, 极发生还原反应 极发生还原反应 |
C.交换膜 为阳离子交换膜 为阳离子交换膜 |
D.生成苯甲酸盐的反应为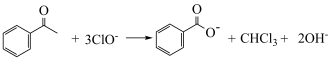 |
您最近半年使用:0次
名校
解题方法
3 . 巴蜀中学化学实验小组利用下图所示微生物电池将污水中苯酚(C6H6O)转化为无毒无害的物质并产生电能(M、N 均为石墨电极)。下列说法错误的是
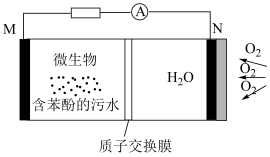

| A.该电池不适宜在高温环境下工作 |
B.M极的电极反应式为: |
C.每消耗标准状况下22.4L  时,理论上能处理约含 13.4g苯酚的废水 时,理论上能处理约含 13.4g苯酚的废水 |
| D.电池工作过程中,正极区的pH降低 |
您最近半年使用:0次
名校
解题方法
4 . 如图所示,杠杆A、B两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑铁丝反应及两边浮力的变化)

| A.杠杆为导体和绝缘体时,均为A端高B端低 |
| B.杠杆为导体和绝缘体时,均为A端低B端高 |
| C.当杠杆为绝缘体时,A端低B端高;当杠杆为导体时,A端高B端低 |
| D.当杠杆为绝缘体内,A端高B端低;当杠杆为导体时,A端低B端高 |
您最近半年使用:0次
2023-08-08更新
|
527次组卷
|
86卷引用:重庆市第三十中学2018-2019学年高一5月月考化学试题
重庆市第三十中学2018-2019学年高一5月月考化学试题(已下线)2011届安徽省蚌埠二中高三第一学期期中考试化学试卷(已下线)2010-2011学年河南省郑州一中高一下学期期末考前模拟化学试题(已下线)2012届浙江省慈溪市高三上学期期中考试化学试卷(已下线)2011-2012学年四川省成都铁中高二下学期2月学业检测化学试卷(已下线)2011-2012学年江西省铅山一中等四校高一下学期联考化学试卷(已下线)2011-2012学年江西省横峰中学高一下学期期中考试化学试卷(已下线)2011-2012学年湖北省襄阳市四校联考高一下学期期中考试化学试卷(已下线)2011-2012学年浙江省衢州一中高一下学期期中检测化学试卷(已下线)2011-2012学年湖北省武汉市五校高一下学期期中统考化学试卷(已下线)2011-2012学年江苏省苏州五中高二第二学期期中考试化学试卷(已下线)2012-2013学年陕西省长安一中高一下学期期中考试化学试卷(已下线)2012-2013学年山东省微山县第一中学高一下学期期中考试化学试卷(已下线)2014年高一化学人教版必修2 模块水平检测2练习卷2014—2015江西省九江市彭泽县第二高中高一下学期期中考试化学试卷2014-2015学年湖北省松滋一中高一下学期6月月考化学试卷2015-2016学年宁夏中卫一中高二下第一次月考化学试卷2015-2016学年河北省邯郸市大名等四县高一下学期期中联考化学试卷2015-2016学年湖北省襄阳市老河口一中高一下期中化学试卷2015-2016学年河北省枣强中学高一下期中化学试卷2015-2016学年浙江省杭州市七校高一下学期期中化学试卷2015-2016学年湖北省枣阳市白水高中高一5月月考化学试卷2015-2016学年河北省邯郸市曲周一中高一下期中化学试卷2015-2016学年山西省太原五中高一下期末化学试卷2015-2016学年河北省石家庄市辛集中学高一下第一次段考化学试卷2015-2016学年湖北省松滋一中高一下学期期末化学试卷2016-2017学年福建省四地六校高二上第一次月考化学试卷甘肃省嘉峪关市第一中学2016-2017学年高一下学期期中考试化学试题四川省资阳中学2016-2017学年高一下学期期中化学试题河南省郑州市中牟县二中2017-2018学年高二第一次月考化学试题2018届高三一轮复习化学:微考点48-电池原理及其应用山西省忻州市第一中学2017-2018学年高二上学期摸底考试化学试题宁夏银川市六盘山高级中学2017-2018学年高二上学期第一次月考化学试题宁夏育才中学孔德校区2017-2018学年高二12月月考化学试题《课时同步君》2017-2018学年高一化学人教必修2-2.2.2 发展中的化学电源(已下线)《周末培优君》2017-2018学年高一下学期化学-第06周 化学能与电能安徽省蚌埠市第二中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2017-2018学年高一下学期期末考试化学试题2018-2019学年人教版高中化学选修四电化学基础章末综合测评题(四)【全国百强校】福建省三明市第一中学2018-2019学年高二上学期第一次月考化学试题甘肃省兰州市第五十八中学2018-2019学年高二(理科)第一学期期末考试化学试题(已下线)考点09 原电池原理及其应用——备战2019年浙江新高考化学考点甘肃省武威市第六中学2018-2019学年高一下学期第二次学段考试化学试题【全国百强校】广东省中山市纪念中学2018~2019学年高一下学期第二次段考化学试题广东省广州大学附属东江中学2018-2019学年高一下学期期末考试化学试题浙江省东阳中学2019-2020学年高二上学期期中考试化学试题2019——2020学年人教版必修2 第二章 化学反应与能量【懂做原理题】2020届高三化学选修4二轮专题练——原电池的应用、双液原电池第二章 化学反应与能量学 综合拓展——B 拓展区 夯实基础(人教版必修2)第六章 化学反应与能量 综合拓展——B拓展区 夯实基础(人教版(2019)第二册)河北省邯郸市磁县第二中学2019-2020学年高一下学期期中考试化学试卷湖南省邵东县第一中学2019-2020学年高二下学期第一次月考化学试题山西省晋中市平遥中学2019-2020高一下学期在线学习质量检测化学试题河南省新安县第一高级中学2019-2020学年高一下学期5月月考化学试题甘肃省兰州市第一中学2019-2020学年高一下学期期中考试化学试题河北省石家庄市辛集市第二中学2019-2020学年高一下学期期末考试化学试题广西钦州市2019-2020学年高一下学期期末教学质量监测化学(理)试题云南省玉溪市峨山一中2020-2021学年高二上学期开学考试化学试题福建省连城县第一中学2020-2021学年高二上学期第一次月考化学试题必修第二册RJ第6章综合拓展(已下线)第四章 检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)吉林省白城市洮南市第一中学2020-2021学年高二上学期第三次月考化学试题人教版2019必修第二册 第六章 第一节 第2课时 化学反应与电能高中化学苏教2019版必修第二册-专题6 第三单元 第2课时 化学电源云南省保山第九中学2019-2020学年高二下学期期末考试化学试题黑龙江省大庆市实验中学实验一部2020-2021学年高一下学期4月阶段性教学质量检测化学试题山东省高密市第五中学2020-2021学年高一下学期4月月考化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 B 素养拓展区河北深州市长江中学2021-2022学年高二上学期10月月考化学(文)试题(已下线)第08讲 化学反应与电能(讲义)-【寒假自学课】2023年高一化学寒假精品课(人教版2019必修第二册)云南省曲靖市罗平县第五中学2021-2022学年高二4月月考化学试题安徽省蚌埠第三中学2021-2022学年高一下学期4月阶段测试化学试题黑龙江省双鸭山市集贤县2021-2022学年高一下学期期中考试化学试题内蒙古赤峰二中2021-2022学年高一下学期第二次月考化学试题江西省抚州市金溪县第一中学2021-2022学年高一下学期第二次月考化学试题辽宁省沈阳市新民市第一高级中学2020-2021学年高一下学期期中考试化学试题湖北省黄冈市麻城市第二中学2021-2022学年高一下学期3月月考化学试题 河南省濮阳市元龙高级中学2021-2022学年高二下学期5月月考化学试题河南省洛阳市宜阳县第一高级中学2022-2023学年高二上学期第五次能力达标测试化学试题黑龙江省哈尔滨工业大学附属中学2022-2023学年高一下学期期末考试化学试题河北省邯郸市大名县第一中学2022-2023学年高一下学期3月月考化学试题云南迪庆藏族自治州民族中学2022-2023学年高一下学期期末考试化学试题第2课时 化学反应与电能(已下线)专题05 化学反应与能量变化(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)(已下线)期中测试卷二【测试范围:第五、六章】-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)6.1.2 化学反应与电能 随堂练习
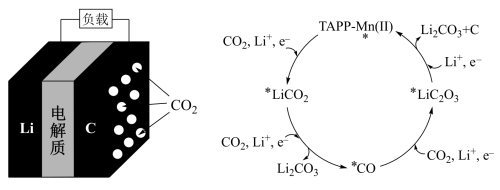
5 .  可充电电池的结构和催化剂
可充电电池的结构和催化剂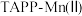 作用下正极反应可能的历程如下图所示。下列说法错误的是
作用下正极反应可能的历程如下图所示。下列说法错误的是
 可充电电池的结构和催化剂
可充电电池的结构和催化剂 作用下正极反应可能的历程如下图所示。下列说法错误的是
作用下正极反应可能的历程如下图所示。下列说法错误的是
A. 电池不能使用 电池不能使用 水溶液做离子导体 水溶液做离子导体 |
B.放电时,电流由C电极经负载、 电极、电解质回到C电极 电极、电解质回到C电极 |
C.放电时,负极反应为: |
D.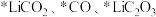 均为正极反应的中间产物 均为正极反应的中间产物 |
您最近半年使用:0次
名校
解题方法
6 . 某实验小组进行Na2SO3的有关探究活动。
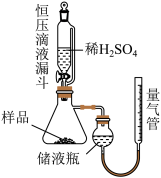
Ⅰ.久置样品纯度的测定
②调节储液瓶与量气管的相对高度,让两边液面在同一水平线上,读数体积为V1mL;
③打开恒压滴液漏斗下端的活塞,加入过量的稀硫酸,比其充分反应:
④调节储液瓶与量气锌的相对高度,让两边液面在同一水平线上,读数体积为V2mL。
(1)进行实验前需进行的操作是_______ ;
(2)使用恒压滴液漏斗添加稀硫酸的优点_______ ;
(3)储液瓶中盛装的液体试剂是_______ ,读数前要调节液面高度是为了消除_______ 对气体体积影响;
(4)若该实验条件为标准状况,则 纯度为
纯度为_______ (用含V1、V2、m的式子表达,已知读数V1>V2)。
Ⅱ.探究CuCl2溶液与 溶液反应
溶液反应
将1 mL0.2 mol/L 溶液与2mL0.2mol/LCuCl2溶液混合,立即生成橙黄色沉淀,3 min后沉淀颜色变浅并伴有少量白色沉淀产生,振荡1min沉淀全部变为白色(CuCl)。
溶液与2mL0.2mol/LCuCl2溶液混合,立即生成橙黄色沉淀,3 min后沉淀颜色变浅并伴有少量白色沉淀产生,振荡1min沉淀全部变为白色(CuCl)。
查阅资料:i橙黄色沉淀为2CuSO4·Cu2SO3·H2O,转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性;
ii原电池装置中物质氧化性与还原性强弱差异越大,电压越大。
(5)反应物生成白色沉淀的离子方程式为_______ ,橙黄色沉淀与Cl-全部转化为CuCl的离子方程式_______ ;
(6)设计如下图实验装置,验证Cl-能提高Cu2+的氧化性
则X为_______ ,
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅰ.久置样品纯度的测定
②调节储液瓶与量气管的相对高度,让两边液面在同一水平线上,读数体积为V1mL;
③打开恒压滴液漏斗下端的活塞,加入过量的稀硫酸,比其充分反应:
④调节储液瓶与量气锌的相对高度,让两边液面在同一水平线上,读数体积为V2mL。
(1)进行实验前需进行的操作是
(2)使用恒压滴液漏斗添加稀硫酸的优点
(3)储液瓶中盛装的液体试剂是
(4)若该实验条件为标准状况,则
 纯度为
纯度为Ⅱ.探究CuCl2溶液与
 溶液反应
溶液反应将1 mL0.2 mol/L
 溶液与2mL0.2mol/LCuCl2溶液混合,立即生成橙黄色沉淀,3 min后沉淀颜色变浅并伴有少量白色沉淀产生,振荡1min沉淀全部变为白色(CuCl)。
溶液与2mL0.2mol/LCuCl2溶液混合,立即生成橙黄色沉淀,3 min后沉淀颜色变浅并伴有少量白色沉淀产生,振荡1min沉淀全部变为白色(CuCl)。查阅资料:i橙黄色沉淀为2CuSO4·Cu2SO3·H2O,转化为CuCl的原因可能是Cl-提高了Cu2+的氧化性;
ii原电池装置中物质氧化性与还原性强弱差异越大,电压越大。
(5)反应物生成白色沉淀的离子方程式为
(6)设计如下图实验装置,验证Cl-能提高Cu2+的氧化性
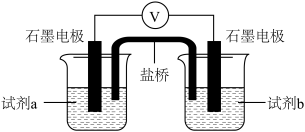
| 试剂a | 试剂b | 电压表读数 |
0.2mol/L 溶液 溶液 | 0.2mol/L 溶液 溶液 | E1 |
0.2mol/L 溶液 溶液 | X | E2 |

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近半年使用:0次
2023·四川内江·三模
名校
解题方法
7 . 电化学合成具有反应条件温和、反应试剂纯净和生产效率高等优点,利用下图所示装置可合成己二腈[NC(CH2)4CN]。充电时生成己二腈,放电时生成O2,其中a、b是互为反置的双极膜,双极膜中的H2O会解离出H+和OH-向两极移动。下列说法正确的是。
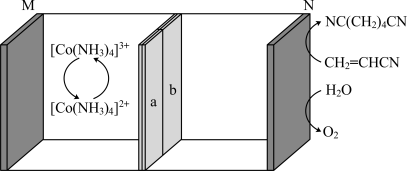

| A.放电时,M极作正极,电极反应式为[Co(NH3)4]3++e-=[Co(NH3)4]2+ |
| B.放电时,双极膜中H+向N极移动 |
| C.充电时,阳极的电极反应式为2CH2=CHCN+2e-+2H+=NC(CH2)4CN |
| D.若充电时制得1molNC(CH2)4CN,则放电时需生成1molO2,才能使左室溶液恢复至初始状态 |
您最近半年使用:0次
2023-05-28更新
|
260次组卷
|
3卷引用:选择题11-14
8 . 组成原电池的装置如图所示,下列叙述不正确的是

| A.电子Zn沿导线流向Cu |
| B.锌是负极,发生氧化反应 |
| C.电池工作时,铜片质量减小 |
| D.电流由铜片经导线流向锌片 |
您最近半年使用:0次
2023-04-19更新
|
402次组卷
|
2卷引用:重庆市江津第五中学校2022-2023学年高一下学期期中考试化学试题
名校
9 . 海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。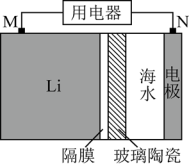
(1)N极为该电池的___________ 极。该电池的总反应为:___________
(2)N极上发生的电极反应为:___________ 、___________
(3)玻璃陶瓷的作用是___________

(1)N极为该电池的
(2)N极上发生的电极反应为:
(3)玻璃陶瓷的作用是
您最近半年使用:0次
名校
10 . 某电池的总反应式为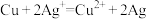 ,该原电池的正确组合是
,该原电池的正确组合是
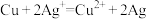 ,该原电池的正确组合是
,该原电池的正确组合是| 选项 | A | B | C | D |
| 正极材料 | Cu | Ag | Ag | Cu |
| 负极材料 | Ag | Cu | Cu | Ag |
| 电解质溶液 |  |  |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-03-12更新
|
1516次组卷
|
6卷引用:重庆市部分区2022-2023学年高一下学期期末联考化学试题



