名校
1 . 关于下列实验事实的给出的解释或结论不正确的是
| 选项 | 实验事实 | 解释或结论 |
| A. |  与 与 溶液反应产生黄色沉淀和气体( 溶液反应产生黄色沉淀和气体( ) ) | 反应生成难溶的 ,增大了 ,增大了 的还原性 的还原性 |
| B. | 将 气体通入 气体通入 溶液中,溶液先变为红棕色(含 溶液中,溶液先变为红棕色(含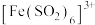 ),过一段时间又变成浅绿色 ),过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| C. | 取一定量固体于试管中,加入浓 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 溶液,产生白色沉淀,将湿润的红色石蕊试纸靠近,试纸变蓝 | 该固体为铵盐 |
| D. | 将变黑的银器放入装满食盐水的铝盆中,一段时间后银器恢复往日光泽 | 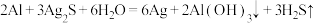 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 铝硫二次电池是一种具有高能量密度、廉价原材料、有前途的替代储能装置,一种铝硫电池如图所示,放电时的电池总反应为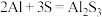 。下列说法错误的是
。下列说法错误的是

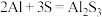 。下列说法错误的是
。下列说法错误的是
A. 和 和 中均存在配位键 中均存在配位键 |
| B.该电池电解质区域所用溶剂不可以为水 |
C.电池放电时的正极反应式为 |
| D.用该电池保护地下铁管道不被腐蚀,铁管道应连接电池的硫碳电极 |
您最近一年使用:0次
3 . 下图是飞船和空间站中利用Sabatier反应再生氧气的大体流程。
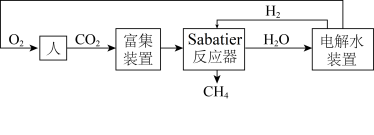
(1)已知:2H2(g)+O2(g) 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1
CH4(g)+2O2(g) CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
则Sabatier反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=___________ 。
(2)二氧化碳的富集装置如图所示。
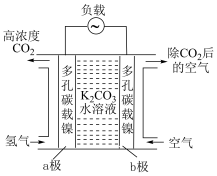
①该富集法采用___________ 原理(填“原电池”或“电解池”)。当a极上消耗1molH2,并保持电解液溶质不变时,b极上除去的CO2在标准状况下的体积为___________ 。
②工作一段时间后,K2CO3溶液的pH___________ (填“变大”“变小”或“不变”)。
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是___________ 。
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是___________ 。
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=___________ (用P0表示)。已知Kp是以分压表示的平衡常数,分压=总压×物质的量分数。
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为___________ (填化学式)。

(1)已知:2H2(g)+O2(g)
 2H2O(g) ∆H=﹣483.6kJ·mol-1
2H2O(g) ∆H=﹣483.6kJ·mol-1CH4(g)+2O2(g)
 CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1
CO2(g)+2H2O(g) ∆H=﹣802.3kJ·mol-1则Sabatier反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的∆H=
CH4(g)+2H2O(g)的∆H=(2)二氧化碳的富集装置如图所示。

①该富集法采用
②工作一段时间后,K2CO3溶液的pH
(3)一定条件下,进行上述Sabatier反应:
①在恒温恒压装置中,下列能说明反应达到平衡状态的是
a.混合气体的密度不再改变 b.混合气体的总质量不再改变
c.混合气体平均摩尔质量不再改变 d.v正(CO2)=2v逆(H2O)
②在Sabatier反应器的前端维持较高温度800K,其目的是
③在温度为T、压强为P0的条件下,按n(CO2)∶n(H2)=1∶4投料进行反应,平衡时CO2的转化率为50%,Kp=
(4)在298K时,几种离子的摩尔电导率如下表。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现O2的再生,从导电性角度选择最适宜的电解质为
| 离子种类 | H+ | OH- |  SO SO | Cl- |  CO CO | K+ | Na+ |
| 摩尔电导率×104(S·m2·mol-1) | 349.82 | 198.0 | 79.8 | 76.34 | 72.0 | 73.52 | 50.11 |
您最近一年使用:0次
4 . 水相锌离子电池工作原理如图。研究发现,往ZnSO4溶液中添加戊二酸(GA),在电极表面生成戊二酸锌保护层,可避免生成碱式硫酸锌,显著提高该电池的循环使用次数。下列说法错误的是
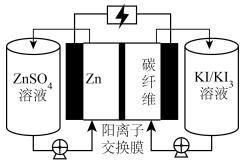

| A.放电时,Zn2+定向移向碳纤维电极 |
| B.添加GA,充电时附着的戊二酸锌保护层被还原生成锌 |
C.充电时,碳纤维做阴极,电极反应式为I +2e-=3I- +2e-=3I- |
| D.放电时产生碱式硫酸锌的可能原因是Zn与水反应使溶液pH升高 |
您最近一年使用:0次
2023-05-08更新
|
216次组卷
|
2卷引用:福建省泉州市2022-2023学年高三适应性练习化学试题
名校
解题方法
5 . 2022 年中国团队在巴塞罗那获得“镁未来技术奖”。一种以MgCl2-聚乙烯醇为电解液的镁电池如图所示。下 列说法不正确的是
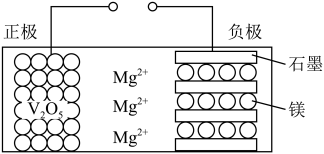

| A.放电时,正极的电极反应式为Mg2+ +2e- +V2O5=MgV2O5 |
| B.放电一段时间后,聚乙烯醇中的c(Mg2+)几乎保持不变 |
| C.充电时,Mg2+ 嵌入V2O5晶格中 |
| D.若将电解液换成MgCl2水溶液,工作时电池可能产生鼓包 |
您最近一年使用:0次
2023-04-25更新
|
293次组卷
|
3卷引用:福建省“德化一中、永安一中、漳平一中”三校协作2023-2024学年高三上学期12月联考化学试题
名校
6 . 回答下列问题
(1)高铁酸钾( )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中,其电池方程式为:
)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中,其电池方程式为: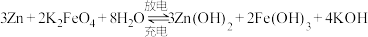 。如图1所示是高铁电池的模拟实验装置。
。如图1所示是高铁电池的模拟实验装置。


①该电池放电时正极反应式为_______ 。
②盐桥中盛有饱和 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向_______ (填“左”或“右”)移动;
③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_______ 。
(2) 和
和 是主要大气污染物,利用如图装置可同时吸收
是主要大气污染物,利用如图装置可同时吸收 和
和 。
。

① 是直流电源的
是直流电源的_______ 极。
②已知电解池的阴极室中溶液的 在4~7之间,阴极的电极反应为
在4~7之间,阴极的电极反应为_______ 。
③用离子方程式表示吸收 的原理
的原理_______ 。
(1)高铁酸钾(
 )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中,其电池方程式为:
)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中,其电池方程式为: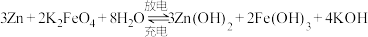 。如图1所示是高铁电池的模拟实验装置。
。如图1所示是高铁电池的模拟实验装置。

①该电池放电时正极反应式为
②盐桥中盛有饱和
 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向③图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)
 和
和 是主要大气污染物,利用如图装置可同时吸收
是主要大气污染物,利用如图装置可同时吸收 和
和 。
。
①
 是直流电源的
是直流电源的②已知电解池的阴极室中溶液的
 在4~7之间,阴极的电极反应为
在4~7之间,阴极的电极反应为③用离子方程式表示吸收
 的原理
的原理
您最近一年使用:0次
名校
解题方法
7 . 某同学为了完成相应的实验目的,所采用的实验装置不合理的是
| 选项 | A | B |
| 实验目的 | 分离溴苯与水 | 石油分馏 |
| 实验装置 |  |  |
| 选项 | C | D |
| 实验目的 | 比较Zn与Cu的活泼性 | 铝热法制取少量的铁 |
| 实验装置 |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . Li/I2电池是常温固体电解质电池,常用于心脏起搏器。负极是锂,正极是碘添加有机材料(如P2VP)做成的导电体多相电极。总反应为2Li +P2VP·nI2=P2VP·(n-1)I2+2LiI。有关说法错误的是
| A.该电池的正极反应式为: 2Li+ +P2VP·nI2 +2e- =P2VP·(n-1)I2 +2LiI |
| B.中间区域LiI的沉积,会使电池电压逐渐下降,对心脏起搏器起到预警作用 |
| C.添加材料P2VP的作用是增强正极材料的导电性 |
| D.其正负极活性物质消耗质量比为7:127 |
您最近一年使用:0次
2022-05-27更新
|
207次组卷
|
2卷引用:福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题
9 . 某同学为了完成相应的实验目的,所采用的实验装置不合理的是
| 选项 | A | B |
| 实验目的 | 分离溴苯与水 | 石油分馏 |
| 实验装置 | 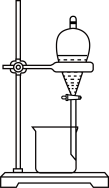 | 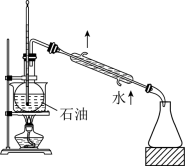 |
| 选项 | C | D |
| 实验目的 | 比较Zn与Cu的活泼性 | 用四氯化碳萃取碘水中的碘 |
| 实验装置 | 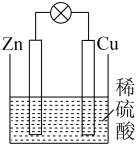 | 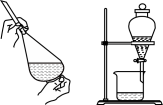 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 科学家最近发明了一种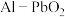 电池,电解质为
电池,电解质为 ,通过x和y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域
,通过x和y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域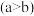 ,结构示意图如图所示。下列说法正确的是
,结构示意图如图所示。下列说法正确的是
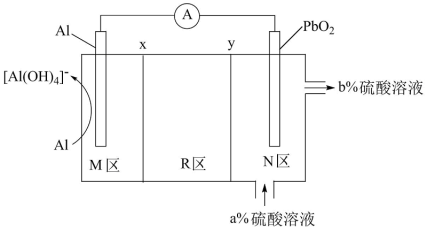
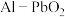 电池,电解质为
电池,电解质为 ,通过x和y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域
,通过x和y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域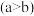 ,结构示意图如图所示。下列说法正确的是
,结构示意图如图所示。下列说法正确的是
A. 通过x膜移向M区 通过x膜移向M区 |
| B.R区域的电解质浓度逐渐减小 |
C.放电时, 电极反应为: 电极反应为: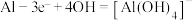 |
D.每消耗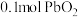 时,电路中转移 时,电路中转移 电子 电子 |
您最近一年使用:0次



