解题方法
1 . 为实现低碳环保的目标,北京冬奥会各赛区推广使用氢氧燃料电池汽车。某种氢氧燃料电池的内部结构示意图如图。

(1)a处通入_______ ,右侧的电极反应式为________ 。
(2)若电路中通过3mol电子,则负极消耗物质的质量为_______ g。

(1)a处通入
(2)若电路中通过3mol电子,则负极消耗物质的质量为
您最近半年使用:0次
解题方法
2 . 化学与生活密切相关,下列叙述正确的是
A.造纸工业常用 处理纸浆,利用了 处理纸浆,利用了 的漂白性 的漂白性 |
| B.尼龙和棉布的主要成分都是天然纤维 |
| C.氢氧燃料电池绿色无污染,属于二次电池 |
| D.硅胶和生石灰有较强的还原性,可用于防止食品氧化变质 |
您最近半年使用:0次
3 . 下列物质结构与性质或物质性质与用途具有对应关系的是
| A.H2具有还原性,可作为氢氧燃料电池的燃料 |
| B.氨极易溶于水,液氨可用作制冷剂 |
| C.H2O分子之间形成氢键,H2O(g)的热稳定性比H2S(g)的高 |
| D.N2H4中的N原子与H+形成配位键,N2H4具有还原性 |
您最近半年使用:0次
4 . 下列过程能实现化学能转化为电能的是
| A. 氢氧燃料电池 | B. 电磁炉加热 | C. 天然气燃烧 | D. 太阳能发电 |
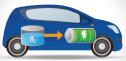 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。

(1)写出电极反应式Cu电极_____ 。盐桥中向CuSO4溶液中迁移的离子是_____ (填离子符号)。
(2)如图是利用H2与O2的反应设计氢氧燃料电池的装置示意图,通入O2的电极是电池的_____ (填“正”或“负”)极,通入H2的电极反应式是_____ ,消耗标况下5.6L氧气时,外电路中通过的电子数为_____ 。
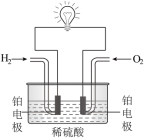

(1)写出电极反应式Cu电极
(2)如图是利用H2与O2的反应设计氢氧燃料电池的装置示意图,通入O2的电极是电池的

您最近半年使用:0次
名校
解题方法
6 . 电化学手段对于研究物质性质以及工业生产中都有重要价值。
Ⅰ.结合所学知识,按要求回答问题。
(1)碱性锌锰电池的总反应为 ,写出正极反应式
,写出正极反应式___________ 。
Ⅱ.载人航天工程对科学研究及太空资源开发具有重要意义,其发展水平是衡量一个国家综合国力的重要指标。中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩瀚星辰的征途。
(2)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的___________ 极, 向
向___________ (填“正”或“负”)极作定向移动,Y极的电极反应式为___________ 。
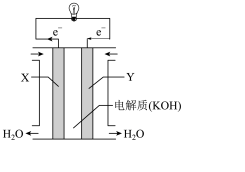
(3)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲得常温下1.8L水,则电池内电子转移的物质的量约为___________ mol
(4)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将________ 能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为: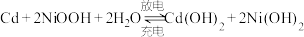 ,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性________ (填“增大”“减小”或“不变”)。
Ⅰ.结合所学知识,按要求回答问题。
(1)碱性锌锰电池的总反应为
 ,写出正极反应式
,写出正极反应式Ⅱ.载人航天工程对科学研究及太空资源开发具有重要意义,其发展水平是衡量一个国家综合国力的重要指标。中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次正式踏上飞向浩瀚星辰的征途。
(2)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断X极为电池的
 向
向
(3)在宇宙飞船或潜艇中,还可利用氢氧燃料电池所产生的水作为饮用水,今欲得常温下1.8L水,则电池内电子转移的物质的量约为
(4)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将
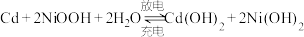 ,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
,当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性
您最近半年使用:0次
7 . 化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中正确的是
A.电解饱和食盐水时,阳极的电极反应为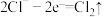 |
B.氢氧燃料电池的正极反应: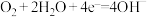 |
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为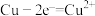 |
D.钢铁发生电化学腐蚀的负极反应: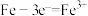 |
您最近半年使用:0次
名校
8 . 元素周期表中VIA族元素单质及其化合物有着广泛应用。O2可用作氢氧燃料电池的氧化剂;O3具有杀菌、消毒、漂白等作用。硫有多种单质,如 2
2 4
4 S6
S6 S8等,用硫黄熏蒸中药材的传统由来已久。硫与氧气反应制得的SO2可用来生产H2SO4,硫酸及硫酸盐是重要化工原料;H2S是一种易燃的有毒气体(燃烧热为
S8等,用硫黄熏蒸中药材的传统由来已久。硫与氧气反应制得的SO2可用来生产H2SO4,硫酸及硫酸盐是重要化工原料;H2S是一种易燃的有毒气体(燃烧热为 -1
-1 是制取多种硫化物的原料;用SO2与SeO2(白色晶体)的水溶液反应可制备硒,硒(34Se)是一种半导体材料。碲(52Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以电解强碱性Na2TeO3溶液制备Te。下列化学反应表示正确的是
是制取多种硫化物的原料;用SO2与SeO2(白色晶体)的水溶液反应可制备硒,硒(34Se)是一种半导体材料。碲(52Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以电解强碱性Na2TeO3溶液制备Te。下列化学反应表示正确的是
 2
2 4
4 S6
S6 S8等,用硫黄熏蒸中药材的传统由来已久。硫与氧气反应制得的SO2可用来生产H2SO4,硫酸及硫酸盐是重要化工原料;H2S是一种易燃的有毒气体(燃烧热为
S8等,用硫黄熏蒸中药材的传统由来已久。硫与氧气反应制得的SO2可用来生产H2SO4,硫酸及硫酸盐是重要化工原料;H2S是一种易燃的有毒气体(燃烧热为 -1
-1 是制取多种硫化物的原料;用SO2与SeO2(白色晶体)的水溶液反应可制备硒,硒(34Se)是一种半导体材料。碲(52Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以电解强碱性Na2TeO3溶液制备Te。下列化学反应表示正确的是
是制取多种硫化物的原料;用SO2与SeO2(白色晶体)的水溶液反应可制备硒,硒(34Se)是一种半导体材料。碲(52Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以电解强碱性Na2TeO3溶液制备Te。下列化学反应表示正确的是A.H2S燃烧的热化学方程式: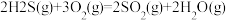  |
B.电解强碱性Na2TeO3溶液的阴极反应: |
C.SO2和SeO2的水溶液反应制备硒: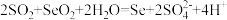 |
D.氢氧燃料电池(H2SO4为电解质溶液)负极反应为: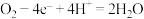 |
您最近半年使用:0次
2023-12-06更新
|
509次组卷
|
2卷引用:江苏省徐州市第一中学、淮阴中学、姜堰中学2023-2024学年高三上学期联考化学试题
名校
解题方法
9 . 2023年10月26日,神舟十七号载人飞船成功发射,我国6名航天员再次太空会师。下列说法错误的是
| A.SiO2可用作航天器的太阳能电池板 |
| B.液氢燃料具有高效能,无污染的特点 |
| C.电解水产生的氧气可以保持空间站有氧环境 |
| D.“分子筛”可以捕捉空间站的CO2 |
您最近半年使用:0次
2023-12-06更新
|
78次组卷
|
2卷引用:黑龙江省大庆实验中学2023-2024学年高二上学期期中考试化学试题
名校
10 . 2022年北京冬奥会期间,赛区内使用了氢燃料清洁能源车辆,某氢氧燃料电池工作如图所示。下列说法不正确的是


| A.此电池反应为自发的氧化还原反应 |
B.电极b表面反应为: |
| C.电池工作过程中K+向负极迁移 |
| D.氢氧燃料电池将化学能转化为电能的转化率高于火力发电,提高了能源利用率 |
您最近半年使用:0次



