名校
解题方法
1 . 下列物质结构与性质或物质性质与用途具有对应关系的是
A. 具有还原性,可作为氢氧燃料电池的燃料 具有还原性,可作为氢氧燃料电池的燃料 |
| B.氨极易溶于水,液氨可用作制冷剂 |
C. 熔点高,可用作电解冶炼铝的原料 熔点高,可用作电解冶炼铝的原料 |
D. 溶液呈酸性,可用于蚀刻电路板上的铜 溶液呈酸性,可用于蚀刻电路板上的铜 |
您最近半年使用:0次
2 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.氯碱工业,当阴极产生2.24L(标况)氯气,则外电路转移0.2 mol电子 |
| B.铅酸蓄电池工作过程中,每通过2 mol电子,负极质量减轻207 g |
| C.在电解精炼粗铜的过程中,当阴极质量增重32 g时转移的电子数为NA |
| D.氢氧燃料电池正极消耗22.4 L气体时,负极消耗气体的分子数为2NA |
您最近半年使用:0次
名校
解题方法
3 . 化学用语是学习化学的重要工具,下列化学用语正确的是
A.钢铁发生电化学腐蚀的正极反应式: |
B.氢氧燃料电池的负极反应式: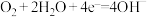 |
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为: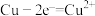 |
D.惰性电极电解饱和食盐水时,阳极的电极反应为: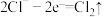 |
您最近半年使用:0次
4 . 下面是几种常见的化学电源示意图,有关说法不正确 的是
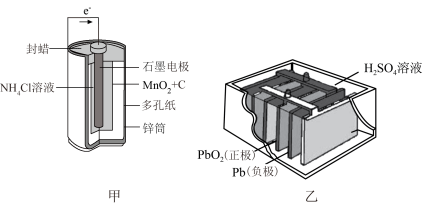
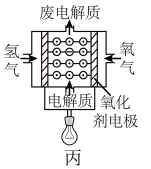


| A.甲、乙、丙分别属于一次电池、二次电池和燃料电池 |
| B.甲电池放电时,电子从锌筒经外电路到石墨电极 |
| C.氢氧燃料电池中负极通入氧气发生还原反应 |
| D.乙电池充电时将电能转化为化学能 |
您最近半年使用:0次
名校
解题方法
5 . 按要求回答下列问题:
(1)已知:1gH2完全燃烧生成液态水的热量为142.9kJ,请写出氢气燃烧热 的热化学方程式_______ 。
(2)H2CO3的电离方程式是_______ 。
(3)硫代硫酸钠(Na2S2O3)溶液与稀硫酸反应的化学方程式是_______ 。
(4)FeCl3水解的离子方程式是_______ 。
(5)写出NaHCO3溶液中的物料守恒式_______ 。
(6)写出氢氧燃料电池(电解质为碱性溶液)的正极电极方程式是_______ 。
(1)已知:1gH2完全燃烧生成液态水的热量为142.9kJ,请写出氢气
(2)H2CO3的电离方程式是
(3)硫代硫酸钠(Na2S2O3)溶液与稀硫酸反应的化学方程式是
(4)FeCl3水解的离子方程式是
(5)写出NaHCO3溶液中的物料守恒式
(6)写出氢氧燃料电池(电解质为碱性溶液)的正极电极方程式是
您最近半年使用:0次
6 . 氢氧燃料电池是一种具有应用前景的绿色电源。(______)
您最近半年使用:0次
名校
解题方法
7 . 回答下列问题
(1)按要求写出下列电极反应式
①氢氧燃料电池酸性环境下,负极反应式:___________ ,正极反应式:___________ 。
②氢氧燃料电池碱性环境下,负极反应式:___________ ,正极反应式:___________ 。
(2)铅酸蓄电池是常用的化学电源,其电极材料分别是 和
和 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。
①铅酸蓄电池的负极材料是___________ ,正极反应式为___________ 。
②电池工作时,溶液中 移向
移向___________ 极(填“正”或“负”)。
③电池工作时,电解质溶液的
___________ (填“增大”“减小”或“不变”)。
④若有 电子从负极流出,则参加反应的
电子从负极流出,则参加反应的 是
是___________  ,负极的质量变化是增大
,负极的质量变化是增大___________ g。
(1)按要求写出下列电极反应式
①氢氧燃料电池酸性环境下,负极反应式:
②氢氧燃料电池碱性环境下,负极反应式:
(2)铅酸蓄电池是常用的化学电源,其电极材料分别是
 和
和 ,电解质溶液为稀硫酸,该电池工作时发生的总反应为
,电解质溶液为稀硫酸,该电池工作时发生的总反应为 。试回答下列问题。
。试回答下列问题。①铅酸蓄电池的负极材料是
②电池工作时,溶液中
 移向
移向③电池工作时,电解质溶液的

④若有
 电子从负极流出,则参加反应的
电子从负极流出,则参加反应的 是
是 ,负极的质量变化是增大
,负极的质量变化是增大
您最近半年使用:0次
名校
解题方法
8 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A.反应 的反应物总键能小于生成物总键能,该反应的 的反应物总键能小于生成物总键能,该反应的 |
B.氢氧燃料电池的负极反应为 |
C.常温常压下,氢氧燃料电池放电过程中消耗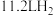 ,转移电子的数目为 ,转移电子的数目为 |
D.同温同压下, ,在燃料电池和点燃条件下的 ,在燃料电池和点燃条件下的 不同 不同 |
您最近半年使用:0次
名校
解题方法
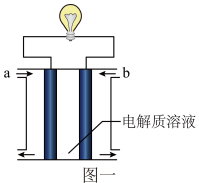
9 . 图一所示是一个燃料电池的示意图,a、b表示通入的气体,当此燃料电池工作时:_______ 。(设气体为同温、同压)
(2)如果a极通入CH4,b极通入O2,NaOH溶液作电解质溶液,则通CH4的电极上的电极反应为:________ 。
(3)如果a极通入乙烯,b极通入O2,H2SO4溶液作电解质溶液,则通乙烯的电极上的电极反应为:_________ 。
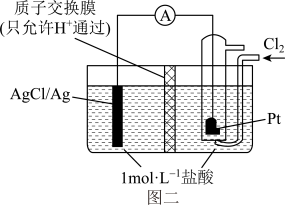
(4)某原电池装置初始状态如图二所示,交换膜两侧的溶液体积均为2L,该电池总反应为_______ ,当电路中转移1mol电子时,共有_______ mol离子通过交换膜,交换膜右侧溶液中c(HCl)=_______ mol•L-1(忽略溶液体积变化和Cl2溶于水)。
(2)如果a极通入CH4,b极通入O2,NaOH溶液作电解质溶液,则通CH4的电极上的电极反应为:
(3)如果a极通入乙烯,b极通入O2,H2SO4溶液作电解质溶液,则通乙烯的电极上的电极反应为:
(4)某原电池装置初始状态如图二所示,交换膜两侧的溶液体积均为2L,该电池总反应为
您最近半年使用:0次
名校
10 . 2022北京冬奥会赛区内使用氢燃料清洁能源车辆,这种车辆利用原电池原理提供清洁电能,某氢氧燃料电池工作原理如图所示。下列说法正确的是


| A.电极a为电池的正极 |
B.电池工作过程中, 向负极迁移 向负极迁移 |
C.电极b表面反应为 |
D.氢氧燃料电池中正极消耗 (标准状况)气体时,电路中通过的电子数目为2NA (标准状况)气体时,电路中通过的电子数目为2NA |
您最近半年使用:0次
2023-08-31更新
|
607次组卷
|
3卷引用:第四章 章末训练



