解题方法
1 .
(1)下列有关说法正确的是____ 。
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在
E.将乙醇与浓硫酸共热制得的气体通入酸性 溶液中,检验气体中是否含有乙烯
溶液中,检验气体中是否含有乙烯
F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在NH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:

K.硝酸钡溶液中通入足量的SO2: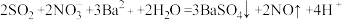
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一: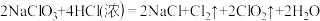
对于该反应,下列说法中正确的是_____ 。
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。

②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为______ (填化学式),理由为_______ 。
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式____ 。
(1)下列有关说法正确的是
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在

E.将乙醇与浓硫酸共热制得的气体通入酸性
 溶液中,检验气体中是否含有乙烯
溶液中,检验气体中是否含有乙烯F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在NH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:

K.硝酸钡溶液中通入足量的SO2:
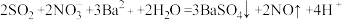
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一:
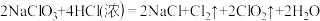
对于该反应,下列说法中正确的是
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。

②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 利用铝 电池电解
电池电解 溶液制备
溶液制备 的装置如图所示。N极为铝电极,其余电极为石墨电极,下列说法错误的是
的装置如图所示。N极为铝电极,其余电极为石墨电极,下列说法错误的是
 电池电解
电池电解 溶液制备
溶液制备 的装置如图所示。N极为铝电极,其余电极为石墨电极,下列说法错误的是
的装置如图所示。N极为铝电极,其余电极为石墨电极,下列说法错误的是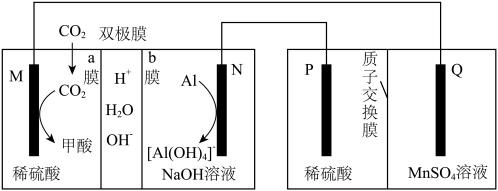
A.双极膜产生的 移向M极 移向M极 |
| B.Q极端的电势高于P极端 |
| C.装置工作时,消耗的气体与生成的气体的物质的量相等 |
D.外电路中通过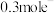 时,氢氧化钠溶液的质量增加2.7g 时,氢氧化钠溶液的质量增加2.7g |
您最近一年使用:0次
名校
解题方法
3 . 用锂硫电池处理含有氯化铵的废水装置如图,锂硫电池工作原理:16Li + S8 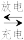 8Li2S。下列说法正确的
8Li2S。下列说法正确的
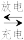 8Li2S。下列说法正确的
8Li2S。下列说法正确的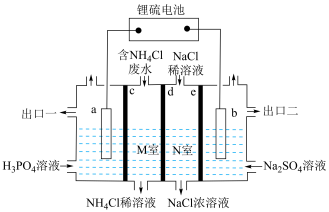
| A.a 电极与锂硫电池的正极相连 |
| B.c、e为阴离子交换膜,d为阳离子交换膜 |
| C.当锂硫电池中消耗32g硫时,N室增加的离子总物质的量为4 mol |
| D.出口一和出口二物质分别为H3PO4浓溶液、Na2SO4浓溶液 |
您最近一年使用:0次
2024-03-22更新
|
476次组卷
|
2卷引用:东北三省三校(哈师大附中、东北师大附中、辽宁省实验中学)2023-2024学年高三下学期第一次联合模拟考化学试卷
名校
解题方法
4 . 一种利用电化学方法处理废水的装置如图所示,利用电解过程中产生的Cl2杀菌消毒,并将废水中钙、镁离子形成沉淀除去。下列说法错误的是
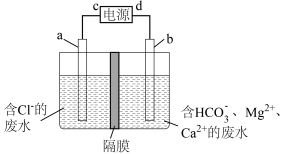
| A.a极为阳极 |
| B.d极发生氧化反应 |
C.b极发生的电极反应为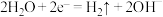 |
| D.每产生0.5molCl2,在阴极室产生1molCaCO3沉淀 |
您最近一年使用:0次
2023-12-04更新
|
246次组卷
|
2卷引用:辽宁省部分学校2023-2024学年高三上学期11月期中大联考化学试题
名校
5 . 利用丙酮酸与废水中的 电催化耦合,可在温和条件下去除
电催化耦合,可在温和条件下去除 并生产丙氨酸,其工作原理如图。
并生产丙氨酸,其工作原理如图。 ,丙氨酸主要以
,丙氨酸主要以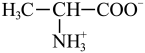 形式存在于溶液中。下列说法错误的是
形式存在于溶液中。下列说法错误的是
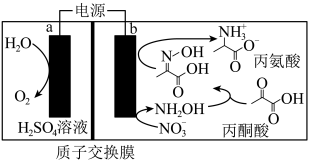
A.电极 连接电源的正极 连接电源的正极 |
B.阴极的电极反应有: |
C.反应一段时间后,阴极区溶液的 基本不变 基本不变 |
D. 极区生成 极区生成 丙氨酸时, 丙氨酸时, 极区至少生成了 极区至少生成了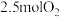 |
您最近一年使用:0次
2024-04-21更新
|
310次组卷
|
3卷引用:辽宁省沈阳市第一二〇中学2024届高三下学期第十次质量监测化学试题
名校
6 . 中国海洋大学科学家发现海泥细菌电池的电压可以高达0.8V,在这种海水/海泥界面存在的天然电压驱动下,海泥细菌产生的电子可以源源不断的传输出来,持续产生电能。下列说法错误的是
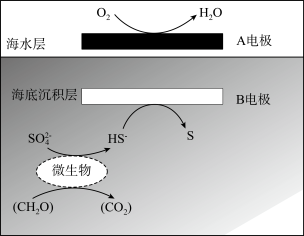
| A.电极电势:A<B |
| B.天然的海泥层和海水层分别为负极和正极的导电介质 |
C.海底沉积层可发生反应: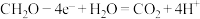 |
| D.海底沉积层/海水天然界面作为“质子交换膜材料”,不需要任何人工膜材料 |
您最近一年使用:0次
7日内更新
|
124次组卷
|
2卷引用:辽宁省大连市2023-2024学年高三下学期第二次模拟考试化学试卷
7 . 金属锰用于生产多种重要的合金。工业上由碳酸锰矿(主要成分为MnCO3,还含有Fe3O4、MgO、SiO2等杂质)制备金属锰的工艺流程如图所示。下列说法错误的是

| A.“浸渣”的主要成分可用于制造陶瓷和耐火材料 |
| B.“氧化”时消耗的过氧化氢与Fe2+的物质的量之比为1:3 |
| C.“沉铁”时发生反应的离子方程式为3MnCO3+2Fe3++3H2O=3Mn2++2Fe(OH)3+3CO2↑ |
| D.“电解”过程中提高电解质溶液的酸度,电解效率会降低 |
您最近一年使用:0次
2024-05-31更新
|
98次组卷
|
2卷引用:辽宁省部分高中2024届高三下学期二轮复习联考(二)化学试题
名校
8 . 高氯酸钾是一种强氧化剂,易溶于水。以氯化钠为原料制备高氯酸钾的一种流程如图:

下列说法错误的是

下列说法错误的是
| A.“电解”步骤中,电解槽内宜使用阳离子交换膜 |
| B.“高温分解”反应中氧化剂和还原剂的物质的量之比为1:3 |
| C.本实验条件下,KClO4在水中的溶解度比NaClO4小 |
| D.“转化”过程所得副产物也可在上述流程中循环利用 |
您最近一年使用:0次
名校
解题方法
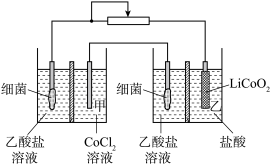
9 . 设计如图所示装置回收金属钴。保持细菌所在环境的pH稳定,借助细菌降解乙酸盐生成 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料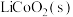 转化为
转化为 。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料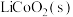 转化为
转化为 。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
。工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
| A.装置工作时,甲室溶液的pH逐渐减小 |
B.乙室电极反应式为 |
| C.为了保持细菌所在环境的pH稳定,两侧都应选择阳离子交换膜 |
D.若甲室 减少150mg,乙室 减少150mg,乙室 增加300mg,则此时已进行过溶液转移 增加300mg,则此时已进行过溶液转移 |
您最近一年使用:0次
2024-01-06更新
|
411次组卷
|
2卷引用:辽宁省盘锦市高级中学2023-2024学年高二上学期12月阶段联考化学试卷
10 . 工业上通过电解 共熔物制取金属Na的装置如图所示,已知在电解过程中会产生一定量的金属Ca,下列说法错误的是
共熔物制取金属Na的装置如图所示,已知在电解过程中会产生一定量的金属Ca,下列说法错误的是
 共熔物制取金属Na的装置如图所示,已知在电解过程中会产生一定量的金属Ca,下列说法错误的是
共熔物制取金属Na的装置如图所示,已知在电解过程中会产生一定量的金属Ca,下列说法错误的是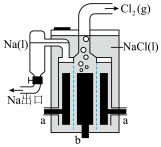
| A.b电极为阳极 |
B.添加 的目的之一是降低电解质体系的熔点 的目的之一是降低电解质体系的熔点 |
C.阴极反应: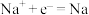 ; ; |
D.为防止生成的Na与 接触,阴、阳两极之间应用钢板隔开 接触,阴、阳两极之间应用钢板隔开 |
您最近一年使用:0次



