2023·山东济南·一模
解题方法
1 . 电解 水溶液制备
水溶液制备 的装置如图所示。电解后测得b极区溶液中溶质的总物质的量增大。下列说法错误的是
的装置如图所示。电解后测得b极区溶液中溶质的总物质的量增大。下列说法错误的是

 水溶液制备
水溶液制备 的装置如图所示。电解后测得b极区溶液中溶质的总物质的量增大。下列说法错误的是
的装置如图所示。电解后测得b极区溶液中溶质的总物质的量增大。下列说法错误的是
A. 水溶液盛放在a极区 水溶液盛放在a极区 |
| B.离子交换膜为阳离子交换膜 |
| C.当外电路转移2 mol电子时,两极室溶液质量变化相差76 g |
D.“电解法”所得副产品可用作“酸性歧化法”制备 的原料 的原料 |
您最近一年使用:0次
解题方法
2 . 科学家利用图装置(其中A和B均为惰性电极)进行电化学固氮,在常温常压下得到肼。下列有关说法正确的是
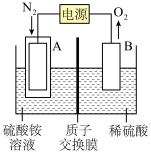
| A.电极B为阴极 |
| B.H+穿过质子交换膜向B电极一侧移动 |
C.A电极的反应式为: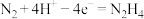 |
| D.相同条件下,A电极每消耗22.4LN2,B电极理论上生成22.4LO2 |
您最近一年使用:0次
2024-04-16更新
|
192次组卷
|
2卷引用:上海市虹口区2023-2024学年高三下学期二模考试化学试卷
名校
解题方法
3 . 实验室用石墨电极电解加有酚酞的饱和NaCl溶液,装置如图1所示。氯碱工业用图2所示装置制备NaOH等工业原料。
(1)a为电解池的___________ 极,a处的电极反应式为___________ 。
(2)b处的电极反应式为___________ ,
(3)该电解池中发生的总反应的离子方程式为___________ 。
(4)下列与电解饱和食盐水有关的说法,正确的是___________ (填字母)。
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.电解熔融NaCl与电解NaCl溶液所得产物相同
Ⅱ.氯碱工业(图2)
(5)利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
①气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是___________ ,气体Y是___________ 。
②阳离子交换膜避免了Cl2与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程___________ 。

(1)a为电解池的
(2)b处的电极反应式为
(3)该电解池中发生的总反应的离子方程式为
(4)下列与电解饱和食盐水有关的说法,正确的是
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.电解熔融NaCl与电解NaCl溶液所得产物相同
Ⅱ.氯碱工业(图2)
(5)利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
①气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是
②阳离子交换膜避免了Cl2与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程
您最近一年使用:0次
2024-03-12更新
|
84次组卷
|
2卷引用:上海市育才中学2023-2024学年高二下学期期中调研(等级考)化学试题
名校
4 . 进行了如图所示的实验,下列说法错误的是

A.石灰石的作用是消耗氯化铁溶液中的 |
| B.欲提纯Z中红褐色的物质,需进行过滤、渗析操作 |
| C.Z中分散系能产生丁达尔效应 |
| D.对Z中液体进行电泳实验,发现阳极区域颜色变深 |
您最近一年使用:0次
5 . CO2的综合利用,通过化学的方法实现CO2的资源化利用是一种理想的CO2减排途径。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集CO2制储氢物质HCOOH
(1)CO2被___________ (填“氧化”或“还原”)为HCOOH,该铂电极为___________ 极。
(2)写出该铂电极的电极方程式___________ 。
(3)当电路中转移3 mol电子时,理论上可生成HCOOH___________ g。
Ⅱ.利用CO2制备CO
一定温度下,在恒容密闭容器中投入一定量CO2和H2进行反应:CO2(g) + H2(g) CO(g) + H2O(g)。
CO(g) + H2O(g)。
(4)下列事实能说明上述反应达到平衡状态的是__________。
(5)在恒定温度与容积下,可以提高CO2平衡转化率的措施有__________。
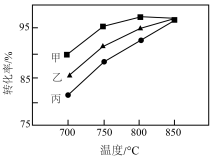
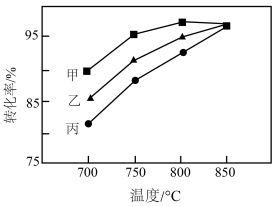
(6)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是_________。
Ⅲ.利用CO2制备甲醇
一定条件下,向恒容密闭容器中通入一定量的CO2和H2.涉及反应如下:
主反应:CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol
CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol
副反应:CO2(g) + H2(g) CO(g) + H2O(g) ΔH = +40.5 kJ/mol
CO(g) + H2O(g) ΔH = +40.5 kJ/mol
(7)其他条件相同,不同压强下,平衡时CO2转化率随温度的变化关系如图所示。
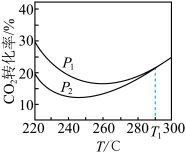
①压强P1___________ P2(填“<”或“>”)。
②图中温度高于T1时,两条曲线重叠的原因是:___________ 。
(8)实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、n(CO2):n(H2) = 1:3,持续通入原料,同时控制出气流量。
①为了维持体系压强恒定,需控制出气流量小于进气流量,原因为:___________ 。
②已知出气流量为0.03 mol/min,单位时间CO2的转化率为60 %,则流出气体中CO的百分含量为___________ 。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集CO2制储氢物质HCOOH
(1)CO2被
(2)写出该铂电极的电极方程式
(3)当电路中转移3 mol电子时,理论上可生成HCOOH
Ⅱ.利用CO2制备CO
一定温度下,在恒容密闭容器中投入一定量CO2和H2进行反应:CO2(g) + H2(g)
 CO(g) + H2O(g)。
CO(g) + H2O(g)。(4)下列事实能说明上述反应达到平衡状态的是__________。
| A.体系内n(CO) : n(H2O) = 1 : 1 | B.体系压强不再发生变化 |
| C.体系内各物质浓度不再发生变化 | D.体系内CO的体积分数不再发生变化 |
(5)在恒定温度与容积下,可以提高CO2平衡转化率的措施有__________。
| A.向反应容器中充入H2 | B.向反应容器中充入CO2 |
| C.添加更有效的催化剂 | D.利用合适试剂干燥混合气体 |
(6)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是_________。

| A.850℃下,该时间段内甲、乙、丙可能均达到平衡 |
| B.700℃下,甲对应的活化能最大 |
| C.一般催化剂既能降低活化能,又能降低过渡态的能量 |
| D.其它条件一定时,随着温度升高,单位体积内活化分子数占比增大 |
Ⅲ.利用CO2制备甲醇
一定条件下,向恒容密闭容器中通入一定量的CO2和H2.涉及反应如下:
主反应:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol
CH3OH(g) + H2O(g) ΔH = −90.4 kJ/mol副反应:CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH = +40.5 kJ/mol
CO(g) + H2O(g) ΔH = +40.5 kJ/mol(7)其他条件相同,不同压强下,平衡时CO2转化率随温度的变化关系如图所示。

①压强P1
②图中温度高于T1时,两条曲线重叠的原因是:
(8)实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、n(CO2):n(H2) = 1:3,持续通入原料,同时控制出气流量。
①为了维持体系压强恒定,需控制出气流量小于进气流量,原因为:
②已知出气流量为0.03 mol/min,单位时间CO2的转化率为60 %,则流出气体中CO的百分含量为
您最近一年使用:0次
名校
6 . 通过化学的方法实现 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径。
减排途径。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集 制储氢物质
制储氢物质 。
。
(1) 被
被___________ (填“氧化”或“还原”)为 ,该铂电极为
,该铂电极为___________ 极。
(2)写出该铂电极的电极方程式___________ 。
(3)当电路中转移 电子时,理论上可生成
电子时,理论上可生成
___________ g。
Ⅱ.利用 制备CO
制备CO
一定温度下,在恒容密闭容器中投入一定量 和
和 进行反应:
进行反应:

(4)在恒定温度与容积下,可以提高 平衡转化率的措施有___________。
平衡转化率的措施有___________。
(5)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是___________。
(6)恒容密闭容器中发生上述反应,在投料比 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度T(B)
平衡转化率如图所示。则B和D两点的温度T(B)___________ T(D)(填“<”、“>”或“=”),其原因是___________ 。

Ⅲ.利用制备甲醇
一定条件下,向恒容密闭容器中通入一定量和 ,实际可能发生以下两个反应:
,实际可能发生以下两个反应:
主反应:
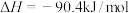
副反应:
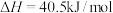
(7)其他条件相同,不同压强下,平衡时 转化率随温度的变化关系如图所示。
转化率随温度的变化关系如图所示。

①压强
___________  (填“<”或“>”)。
(填“<”或“>”)。
②如图中温度高于 时,两条曲线重叠的原因是:
时,两条曲线重叠的原因是:___________ 。
 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径。
减排途径。Ⅰ.利用酸性水溶液电解池在铂电极上捕集
 制储氢物质
制储氢物质 。
。(1)
 被
被 ,该铂电极为
,该铂电极为(2)写出该铂电极的电极方程式
(3)当电路中转移
 电子时,理论上可生成
电子时,理论上可生成
Ⅱ.利用
 制备CO
制备CO一定温度下,在恒容密闭容器中投入一定量
 和
和 进行反应:
进行反应:

(4)在恒定温度与容积下,可以提高
 平衡转化率的措施有___________。
平衡转化率的措施有___________。A.向反应容器中充入 | B.向反应容器中充入 |
| C.添加更有效的催化剂 | D.利用合适试剂干燥混合气体 |
(5)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是___________。

| A.850℃下,该时间段内甲、乙、丙可能均达到平衡 |
| B.700℃下,甲对应的活化能最大 |
| C.一般催化剂既能降低活化能,又能降低过渡态的能量 |
| D.其它条件一定时,随着温度升高,单位体积内活化分子数占比增大 |
(6)恒容密闭容器中发生上述反应,在投料比
 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度T(B)
平衡转化率如图所示。则B和D两点的温度T(B)
Ⅲ.利用制备甲醇
一定条件下,向恒容密闭容器中通入一定量和
 ,实际可能发生以下两个反应:
,实际可能发生以下两个反应:主反应:

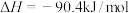
副反应:

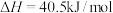
(7)其他条件相同,不同压强下,平衡时
 转化率随温度的变化关系如图所示。
转化率随温度的变化关系如图所示。
①压强

 (填“<”或“>”)。
(填“<”或“>”)。②如图中温度高于
 时,两条曲线重叠的原因是:
时,两条曲线重叠的原因是:
您最近一年使用:0次
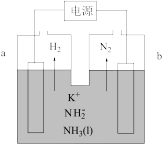
7 . 液氨中存在平衡: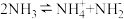 。如图所示为电解池装置,以
。如图所示为电解池装置,以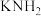 的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
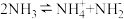 。如图所示为电解池装置,以
。如图所示为电解池装置,以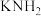 的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
的液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
| A.b电极连接的是电源的负极 | B.a电极的反应为 |
| C.电解过程中,阴极附近K+浓度减小 | D.理论上两极产生的气体物质的量之比为1:1 |
您最近一年使用:0次
2021-10-23更新
|
7500次组卷
|
22卷引用:上海市实验学校2021-2022学年高三下学期3月月考化学试题
上海市实验学校2021-2022学年高三下学期3月月考化学试题2021年新高考海南化学高考真题黑龙江省哈尔滨师范大学附属中学2021-2022学年高三上学期期中考试化学试题2021年海南高考化学试题变式题1-10(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点03 电化学基础知识-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题(已下线)考点19 电解池-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第35练 电解池-2023年高考化学一轮复习小题多维练(全国通用)湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)微专题33 四步敲定高考新情景电池电极反应式的书写-备战2023年高考化学一轮复习考点微专题江苏省扬州中学2022-2023学年高二上学期10月月考化学试题黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期期中考试化学试题云南省玉溪市峨山县第一中学2022-2023学年高二上学期期中考试化学试题(已下线)专题05 化学能与电能的转化(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用章末检测卷(四) 化学反应与电能(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)云南省西双版纳傣族自治州第一中学2022-2023学年高二下学期期末考试化学试题(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
8 . 氯碱工业中常用离子交换膜法电解制碱(如图1所示)

(1)如果粗盐中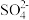 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去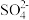 ,该钡试剂可以是
,该钡试剂可以是_______ ;
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)写出图1中阴极的电极反应式为___________ ;已知阳离子交换膜只允许正离子通过,阴离子交换膜只允许负离子通过。工业上若用图2装置电解饱和Na2SO4溶液来生产纯净的NaOH和H2SO4,则该装置最主要的缺陷是___________ 。

(3)银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示如下: 假若以此电池为电源,电解饱和食盐水制得氯气0.050mol,这时电池的负极材料及消耗的物质的量至少是______;
假若以此电池为电源,电解饱和食盐水制得氯气0.050mol,这时电池的负极材料及消耗的物质的量至少是______;
(4)对于所得的氯气下列说法不正确的是______
(5)在一定温度下,氯气溶于水的过程及其平衡常数为:


 K2
K2
其中p为Cl2(g)的平衡压强,c (Cl2)为Cl2在水溶液中的平衡浓度。
①推测 的焓变ΔH1
的焓变ΔH1___________ 0,(填“>”、“=”或“<”)理由是___________ 。
②平衡常数K2的表达式为K2=___________ 。
③氯气在水中的溶解度(以物质的量浓度表示)为C,则C =___________ 。(提示:氯气在水中的溶解度包括游离态的氯气和已经反应掉的氯气之和;用平衡压强p和上述平衡常数K1、K2表示,忽略HClO的电离)
(6)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO2)为原料生产TiCl4,相应的化学方程式为:
I. ΔHI=+181kJ·mol-1,KI=3.4×10-29
ΔHI=+181kJ·mol-1,KI=3.4×10-29
Ⅱ. ΔHⅡ= - 221kJ·mol-1,KⅡ=1.2×1048,
ΔHⅡ= - 221kJ·mol-1,KⅡ=1.2×1048,
结合数据说明氯化过程中加碳的理由___________ 。

(1)如果粗盐中
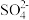 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去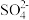 ,该钡试剂可以是
,该钡试剂可以是A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)写出图1中阴极的电极反应式为

(3)银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示如下:
 假若以此电池为电源,电解饱和食盐水制得氯气0.050mol,这时电池的负极材料及消耗的物质的量至少是______;
假若以此电池为电源,电解饱和食盐水制得氯气0.050mol,这时电池的负极材料及消耗的物质的量至少是______;| A.银0.025 mol | B.锌0.050 mol | C.银0.100 mol | D.锌0.200 mol |
(4)对于所得的氯气下列说法不正确的是______
| A.可采用碱石灰干燥氯气 |
| B.可通过排饱和食盐水法收集氯气 |
| C.常温下,可通过加压使氯气液化而储存于钢瓶中 |
| D.工业上,常用氢气和氯气反应生成的氯化氢溶于水制取盐酸 |
(5)在一定温度下,氯气溶于水的过程及其平衡常数为:


 K2
K2其中p为Cl2(g)的平衡压强,c (Cl2)为Cl2在水溶液中的平衡浓度。
①推测
 的焓变ΔH1
的焓变ΔH1②平衡常数K2的表达式为K2=
③氯气在水中的溶解度(以物质的量浓度表示)为C,则C =
(6)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO2)为原料生产TiCl4,相应的化学方程式为:
I.
 ΔHI=+181kJ·mol-1,KI=3.4×10-29
ΔHI=+181kJ·mol-1,KI=3.4×10-29Ⅱ.
 ΔHⅡ= - 221kJ·mol-1,KⅡ=1.2×1048,
ΔHⅡ= - 221kJ·mol-1,KⅡ=1.2×1048,结合数据说明氯化过程中加碳的理由
您最近一年使用:0次
名校
9 . 传统的石棉隔膜法电解饱和食盐水因电耗高、污染严重,已逐步被综合能耗低、污染小的新型离子交换膜所取代,如用阳离子交换膜法电解食盐水制浓烧碱溶液的流程如图所示。
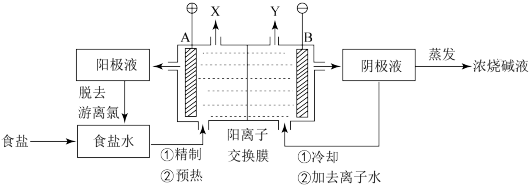
下列有关说法正确的是

下列有关说法正确的是
A.A极为阳极, 发生氧化反应生成的气体X为 发生氧化反应生成的气体X为 |
B.阴极发生的电极反应式为: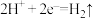 |
C.电解饱和食盐水的离子方程式为: |
D.常温常压下,每生成 气体Y,理论上能产生 气体Y,理论上能产生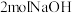 |
您最近一年使用:0次
22-23高二下·上海浦东新·期中
名校
解题方法
10 . 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,下列说法错误的个数是

①X是负极,Y是正极
②若用右侧装置(电解液改为 溶液)在钥匙上镀铜,则将钥匙放在b处
溶液)在钥匙上镀铜,则将钥匙放在b处
③ 溶液的酸性先增强,当铜电极有气泡产生时,此后一段时间酸性会继续增强
溶液的酸性先增强,当铜电极有气泡产生时,此后一段时间酸性会继续增强
④若用右侧装置(电解液改为 溶液)精炼粗铜时,则将粗铜放在b处
溶液)精炼粗铜时,则将粗铜放在b处

①X是负极,Y是正极
②若用右侧装置(电解液改为
 溶液)在钥匙上镀铜,则将钥匙放在b处
溶液)在钥匙上镀铜,则将钥匙放在b处③
 溶液的酸性先增强,当铜电极有气泡产生时,此后一段时间酸性会继续增强
溶液的酸性先增强,当铜电极有气泡产生时,此后一段时间酸性会继续增强④若用右侧装置(电解液改为
 溶液)精炼粗铜时,则将粗铜放在b处
溶液)精炼粗铜时,则将粗铜放在b处| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次



