解题方法
1 . 许多有机化学反应包含电子的转移,使这些反应在电解池中进行时称为电有机合成。制取尼龙-66的原料已二腈 用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是
用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是
 用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是
用量很大,传统上以乙炔和甲醛经过很长路线才能合成己二腈。如改用电合成法,则先以丙烯为原料制备丙烯腈,再用丙烯腈电合成法直接生成己二腈。如图是利用铅酸蓄电池作为电源电合成己二腈的示意图,下列说法错误的是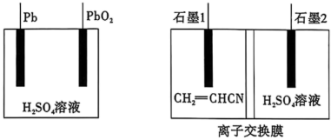
| A.石墨1应与铅酸蓄电池的Pb电极相连 |
| B.离子交换膜应使用阳离子交换膜 |
C.石墨电极1上发生的电极反应为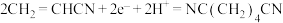 |
D.每生成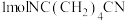 ,石墨2所在极区溶液减重16g ,石墨2所在极区溶液减重16g |
您最近一年使用:0次
2 . 以 为原料合成了葡萄糖和长链脂肪酸,这项突破为人工和半人工合成“粮食”提供了新技术.合成路线为
为原料合成了葡萄糖和长链脂肪酸,这项突破为人工和半人工合成“粮食”提供了新技术.合成路线为 葡萄糖、长链脂肪酸.下列说法正确的是
葡萄糖、长链脂肪酸.下列说法正确的是
 为原料合成了葡萄糖和长链脂肪酸,这项突破为人工和半人工合成“粮食”提供了新技术.合成路线为
为原料合成了葡萄糖和长链脂肪酸,这项突破为人工和半人工合成“粮食”提供了新技术.合成路线为 葡萄糖、长链脂肪酸.下列说法正确的是
葡萄糖、长链脂肪酸.下列说法正确的是| A.过程①、②中化学能转化为电能 |
| B.葡萄糖分子中含有醛基、羧基 |
| C.在酒化酶的催化下,葡萄糖能发生水解反应生成乙醇 |
D. 和 和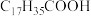 互为同系物 互为同系物 |
您最近一年使用:0次
3 . 我国科学家以海水为氯源合成 ,
, -二氯酮,其装置如图。并以其为原料合成药物米托坦c,合成路线为
-二氯酮,其装置如图。并以其为原料合成药物米托坦c,合成路线为
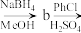
 。下列说法
。下列说法
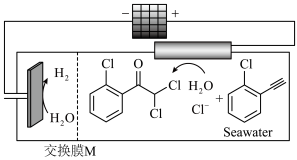
A.阳极反应: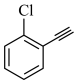 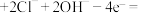   |
| B.M为阳离子交换膜 |
C.b为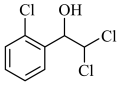 |
| D.整个转化中碳原子的杂化轨道类型有3种 |
您最近一年使用:0次
名校
4 . 我国力争于2030年前做到碳达峰、2060年前实现碳中和,体现了中国对解决气候问题的担当。 是目前大气中含量最高的一种温室气体。减弱温室效应的方法之一是将
是目前大气中含量最高的一种温室气体。减弱温室效应的方法之一是将 回收利用,科学家研究利用回收的
回收利用,科学家研究利用回收的 制取甲醛
制取甲醛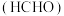 。请回答下列问题:
。请回答下列问题:
(1)已知:①

②
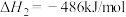
写出 和
和 合成甲醛和水蒸气的热化学方程式
合成甲醛和水蒸气的热化学方程式_______ 。
(2)一定条件下,将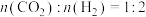 的混合气体充入恒温恒容的密闭容器中,发生反应
的混合气体充入恒温恒容的密闭容器中,发生反应 。下列说明反应已经达到平衡状态的是
。下列说明反应已经达到平衡状态的是_______ (填字母)。
a.混合气体的平均相对分子质量不变 b.该反应的平衡常数保持不变
c. 的体积分数保持不变 d.容器内气体密度保持不变
的体积分数保持不变 d.容器内气体密度保持不变
(3)在一定条件下,在容积恒定为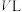 的密闭容器中充入
的密闭容器中充入 与
与 在催化剂作用下合成甲醇:
在催化剂作用下合成甲醇: 。
。 转化率与温度、压强的关系如图所示:
转化率与温度、压强的关系如图所示:

①
_______ (填“<”“>”或“=”) 。该反应是
。该反应是_______ (填“吸”或“放”)热反应。
②图中b、c、d三点的化学平衡常数为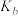 、
、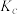 、
、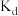 ,从大到小的顺序为
,从大到小的顺序为_______ 。
③电解法制氢气。科研小组设计如图所示电解池,利用 和
和 在碱性电解液中制备水煤气(
在碱性电解液中制备水煤气( 、
、 ),产物中
),产物中 和
和 物质的量之比为
物质的量之比为 。电极B是
。电极B是_______ 极

 是目前大气中含量最高的一种温室气体。减弱温室效应的方法之一是将
是目前大气中含量最高的一种温室气体。减弱温室效应的方法之一是将 回收利用,科学家研究利用回收的
回收利用,科学家研究利用回收的 制取甲醛
制取甲醛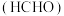 。请回答下列问题:
。请回答下列问题:(1)已知:①


②

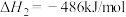
写出
 和
和 合成甲醛和水蒸气的热化学方程式
合成甲醛和水蒸气的热化学方程式(2)一定条件下,将
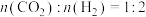 的混合气体充入恒温恒容的密闭容器中,发生反应
的混合气体充入恒温恒容的密闭容器中,发生反应 。下列说明反应已经达到平衡状态的是
。下列说明反应已经达到平衡状态的是a.混合气体的平均相对分子质量不变 b.该反应的平衡常数保持不变
c.
 的体积分数保持不变 d.容器内气体密度保持不变
的体积分数保持不变 d.容器内气体密度保持不变(3)在一定条件下,在容积恒定为
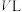 的密闭容器中充入
的密闭容器中充入 与
与 在催化剂作用下合成甲醇:
在催化剂作用下合成甲醇: 。
。 转化率与温度、压强的关系如图所示:
转化率与温度、压强的关系如图所示:
①

 。该反应是
。该反应是②图中b、c、d三点的化学平衡常数为
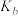 、
、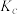 、
、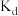 ,从大到小的顺序为
,从大到小的顺序为③电解法制氢气。科研小组设计如图所示电解池,利用
 和
和 在碱性电解液中制备水煤气(
在碱性电解液中制备水煤气( 、
、 ),产物中
),产物中 和
和 物质的量之比为
物质的量之比为 。电极B是
。电极B是
您最近一年使用:0次
解题方法
5 . 近日,清华大学某团队设计出了一种双极性膜(将 解离成
解离成 和
和 )电解合成
)电解合成 反应器,简化模型如图所示,下列说法错误的是
反应器,简化模型如图所示,下列说法错误的是
 解离成
解离成 和
和 )电解合成
)电解合成 反应器,简化模型如图所示,下列说法错误的是
反应器,简化模型如图所示,下列说法错误的是
| A.电极a的电势小于电极b的电势 |
B.通电时双极性膜将水解离为 和 和 , , 向阴极方向移动 向阴极方向移动 |
C.阴极的电极反应式为 |
| D.维持电流强度0.5A,电池工作5min,理论上产生约0.012L气体(已折算成标准状况下) |
您最近一年使用:0次
名校
解题方法
6 . 我国科技工作者设计以  和
和 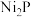 纳米片为催化电极材料,电催化合成偶氮化合物的装置如图所示 (
纳米片为催化电极材料,电催化合成偶氮化合物的装置如图所示 ( 代表烃基,
代表烃基,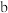 极产物为偶氮苯),该装置工作时,下列说法错误的是
极产物为偶氮苯),该装置工作时,下列说法错误的是

 和
和 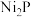 纳米片为催化电极材料,电催化合成偶氮化合物的装置如图所示 (
纳米片为催化电极材料,电催化合成偶氮化合物的装置如图所示 ( 代表烃基,
代表烃基,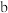 极产物为偶氮苯),该装置工作时,下列说法错误的是
极产物为偶氮苯),该装置工作时,下列说法错误的是
A. 从右往左移动 从右往左移动 |
B.电极 的电极电势高于电极 的电极电势高于电极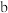 |
C.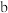 极反应为:2 极反应为:2 +8e—+4H2O= +8e—+4H2O= +8OH— +8OH— |
D.消耗  的同时生成 的同时生成 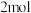 偶氮苯 偶氮苯 |
您最近一年使用:0次
解题方法
7 . 制造尼龙-66的原料已二腈用量很大,工业采用丙烯腈( )电解合成己二腈[
)电解合成己二腈[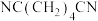 ],电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈(
],电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈(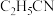 )等副产物,向Y极区电解液中加入少量季铵盐四丁基氢氧化铵[阳离子
)等副产物,向Y极区电解液中加入少量季铵盐四丁基氢氧化铵[阳离子 ,R为烃基],当溶液的
,R为烃基],当溶液的 时,己二腈的产率最高。下列说法
时,己二腈的产率最高。下列说法不正确 的是
 )电解合成己二腈[
)电解合成己二腈[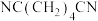 ],电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈(
],电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈(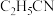 )等副产物,向Y极区电解液中加入少量季铵盐四丁基氢氧化铵[阳离子
)等副产物,向Y极区电解液中加入少量季铵盐四丁基氢氧化铵[阳离子 ,R为烃基],当溶液的
,R为烃基],当溶液的 时,己二腈的产率最高。下列说法
时,己二腈的产率最高。下列说法
| A.电极X接电源正极,发生氧化反应 |
B.电极Y上ⅰ的电极反应式为: |
| C.生成1.0mol己二腈和丙腈的混合物,则X极区溶液的质量变化至少18g |
| D.季铵盐增强电解液的电导率,增加丙烯腈的溶解度促进ⅰ发生,抑制ⅱ和ⅲ反应,提高产品产率 |
您最近一年使用:0次
8 . 我国的二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。 CO2的资源化利用有利于实现我国提出的“碳达峰”与“碳中和”目标。
Ⅰ.早在二十世纪初,工业上以 CO2和 NH3为原料在一定温度和压强下合成尿素。反应分两步:① CO2和NH3生成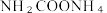 ;②
;②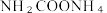 分解生成尿素。反应过程能量变化如下图所示:
分解生成尿素。反应过程能量变化如下图所示:_______ (填“①”或“②”);合成尿素总反应的热化学方程式为_______ (△H用含E₁、E₂、E₃、E₄的式子表示)。
Ⅱ.利用 CO2生产甲醇是资源化利用 CO2的另一种有效途径。涉及的反应如下:
反应i:
反应ii: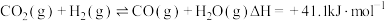
反应iii: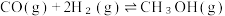 ΔH=-90.6 kJ·mo
ΔH=-90.6 kJ·mo
(2)不同压强下,按照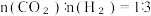 投料,发生上述三个可逆反应,实验测定 CO2的平衡转化率和
投料,发生上述三个可逆反应,实验测定 CO2的平衡转化率和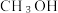 的平衡产率随温度的变化关系如下图所示,下列说法正确的是_______。
的平衡产率随温度的变化关系如下图所示,下列说法正确的是_______。
(3)在一容积可变的密闭容器中,充有1mol CO和 ,用于合成甲醇。只发生上述反应iii,CO的平衡转化率(α)与温度(T)、压强(P)的关系如下图所示,请回答下列问题:
,用于合成甲醇。只发生上述反应iii,CO的平衡转化率(α)与温度(T)、压强(P)的关系如下图所示,请回答下列问题:_______ ,并解释判断理由_______ 。
②若达到平衡状态B时容器的体积为2L,则达到平衡状态A时容器的体积为_______ L。
Ⅲ.用光电化学法将CO2还原为有机物可实现碳资源的再生利用,其装置如图丙所示,其他条件一定时,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图丁所示: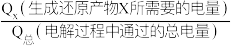 100%,其中电量Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
100%,其中电量Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
(4)当电解电压为U1Ⅴ时,阴极生成HCOOH的电极反应式为_______ 。
(5)当电解电压为U2V时,电解生成的HCHO和HCOOH的物质的量之比为7:5,则生成HCHO的法拉第效率m为_______ 。
Ⅰ.早在二十世纪初,工业上以 CO2和 NH3为原料在一定温度和压强下合成尿素。反应分两步:① CO2和NH3生成
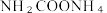 ;②
;②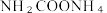 分解生成尿素。反应过程能量变化如下图所示:
分解生成尿素。反应过程能量变化如下图所示:
Ⅱ.利用 CO2生产甲醇是资源化利用 CO2的另一种有效途径。涉及的反应如下:
反应i:

反应ii:
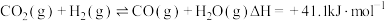
反应iii:
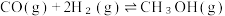 ΔH=-90.6 kJ·mo
ΔH=-90.6 kJ·mo
(2)不同压强下,按照
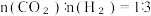 投料,发生上述三个可逆反应,实验测定 CO2的平衡转化率和
投料,发生上述三个可逆反应,实验测定 CO2的平衡转化率和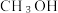 的平衡产率随温度的变化关系如下图所示,下列说法正确的是_______。
的平衡产率随温度的变化关系如下图所示,下列说法正确的是_______。
A.压强大小: 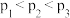 |
B.图甲的纵坐标表示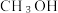 的平衡产率 的平衡产率 |
C.图乙中 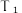 时以反应ii为主,压强改变对平衡无影响 时以反应ii为主,压强改变对平衡无影响 |
D.选择低温低压的反应条件可同时提高平衡时 的转化率和 的转化率和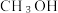 的产率 的产率 |
(3)在一容积可变的密闭容器中,充有1mol CO和
 ,用于合成甲醇。只发生上述反应iii,CO的平衡转化率(α)与温度(T)、压强(P)的关系如下图所示,请回答下列问题:
,用于合成甲醇。只发生上述反应iii,CO的平衡转化率(α)与温度(T)、压强(P)的关系如下图所示,请回答下列问题:
②若达到平衡状态B时容器的体积为2L,则达到平衡状态A时容器的体积为
Ⅲ.用光电化学法将CO2还原为有机物可实现碳资源的再生利用,其装置如图丙所示,其他条件一定时,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图丁所示:

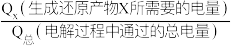 100%,其中电量Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
100%,其中电量Qx=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。(4)当电解电压为U1Ⅴ时,阴极生成HCOOH的电极反应式为
(5)当电解电压为U2V时,电解生成的HCHO和HCOOH的物质的量之比为7:5,则生成HCHO的法拉第效率m为
您最近一年使用:0次
9 . 环氧乙烷(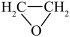 简称EO)是一种重要的有机合成原料和高效消毒剂。由乙烯经电解制备EO的原理示意图如图,下列说法不正确的是
简称EO)是一种重要的有机合成原料和高效消毒剂。由乙烯经电解制备EO的原理示意图如图,下列说法不正确的是
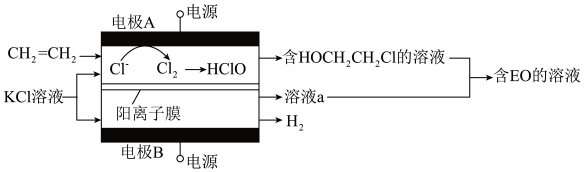
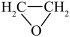 简称EO)是一种重要的有机合成原料和高效消毒剂。由乙烯经电解制备EO的原理示意图如图,下列说法不正确的是
简称EO)是一种重要的有机合成原料和高效消毒剂。由乙烯经电解制备EO的原理示意图如图,下列说法不正确的是
| A.电极A接电源的负极 |
B.阳极室产生Cl2后发生的反应有:Cl2+H2O HCl+HClO HCl+HClO |
C.该过程的总反应为:CH2=CH2+H2O 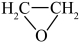 +H2 +H2 |
| D.溶液a为KCl和KOH的混合溶液 |
您最近一年使用:0次
解题方法
10 . 制造尼龙 的原料已二腈用量很大,工业采用丙烯腈
的原料已二腈用量很大,工业采用丙烯腈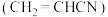 电解合成已二腈
电解合成已二腈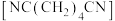 ,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈
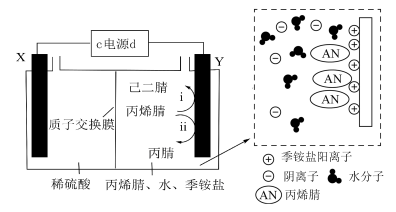
,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈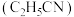 等副产物,向
等副产物,向 极区电解液中加入少量季铵盐,当溶液的
极区电解液中加入少量季铵盐,当溶液的 时,已二腈的产率最高。下列说法不正确的是
时,已二腈的产率最高。下列说法不正确的是
 的原料已二腈用量很大,工业采用丙烯腈
的原料已二腈用量很大,工业采用丙烯腈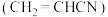 电解合成已二腈
电解合成已二腈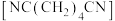 ,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈
,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈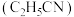 等副产物,向
等副产物,向 极区电解液中加入少量季铵盐,当溶液的
极区电解液中加入少量季铵盐,当溶液的 时,已二腈的产率最高。下列说法不正确的是
时,已二腈的产率最高。下列说法不正确的是
A.电源 极的电势高于 极的电势高于 极 极 |
B.电极 上 上 的电极反应式为: 的电极反应式为: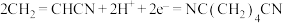 |
C.生成 已二腈和丙腈的混合物,则 已二腈和丙腈的混合物,则 极区溶液的质量理论上减少 极区溶液的质量理论上减少 |
| D.季铵盐可增强电解液的电导率,抑制ⅱ反应的发生,提高已二腈的选择性 |
您最近一年使用:0次



