1 . 为了实现“碳中和”,研发 的利用技术成为热点。
的利用技术成为热点。
反应I:
反应Ⅱ:
请回答:
(1)反应I能够自发进行的条件是__________ 。
(2)向 的恒容密闭容器中充入
的恒容密闭容器中充入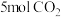 和
和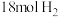 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
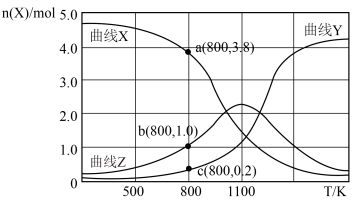
①写出曲线Y表示的含碳元素物质的化学式__________ 。
② 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
__________ [对于气相反应,用某组分 的平衡压强
的平衡压强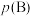 代替物质的量浓度
代替物质的量浓度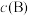 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如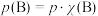 ,
, 为平衡总压强,
为平衡总压强,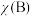 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。
(3)可用 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: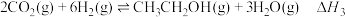 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示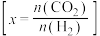 :
:

①上述反应的活化能 (正)
(正)__________  (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
② 、
、 、
、 由大到小的顺序是
由大到小的顺序是__________ 。
③从平衡角度分析,随温度升高,不同投料比时 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因__________ 。
(4)科学家提出由 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为__________ 。

(5)水系可逆 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:

①放电时复合膜中向 极移动的离子是
极移动的离子是__________ 。
②充电时多孔 纳米片电极的电极反应式为
纳米片电极的电极反应式为__________ 。
 的利用技术成为热点。
的利用技术成为热点。反应I:

反应Ⅱ:

请回答:
(1)反应I能够自发进行的条件是
(2)向
 的恒容密闭容器中充入
的恒容密闭容器中充入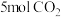 和
和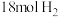 (起始压强为
(起始压强为 ),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量
),在不同温度下同时发生上述反应I和反应Ⅱ,得到平衡时各含碳物质的物质的量 与温度
与温度 的关系如下图所示。
的关系如下图所示。
①写出曲线Y表示的含碳元素物质的化学式
②
 时,反应Ⅱ的平衡常数
时,反应Ⅱ的平衡常数
 的平衡压强
的平衡压强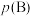 代替物质的量浓度
代替物质的量浓度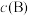 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如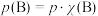 ,
, 为平衡总压强,
为平衡总压强,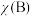 为平衡系统中
为平衡系统中 的物质的量分数]。
的物质的量分数]。(3)可用
 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: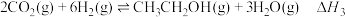 。经实验测定在不同投料比
。经实验测定在不同投料比 、
、 、
、 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示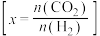 :
:
①上述反应的活化能
 (正)
(正) (逆)(填“
(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。②
 、
、 、
、 由大到小的顺序是
由大到小的顺序是③从平衡角度分析,随温度升高,不同投料比时
 的平衡转化率趋于相近的原因
的平衡转化率趋于相近的原因(4)科学家提出由
 制取
制取 的太阳能工艺如图。已知“重整系统”发生的反应中
的太阳能工艺如图。已知“重整系统”发生的反应中 ,则
,则 的化学式为
的化学式为
(5)水系可逆
 电池可吸收利用
电池可吸收利用 ,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的
,将两组阴离子、阳离子复合膜反向放置分隔两室电解液充、放电时,复合膜间的 解离成
解离成 和
和 ,工作原理如图所示:
,工作原理如图所示:
①放电时复合膜中向
 极移动的离子是
极移动的离子是②充电时多孔
 纳米片电极的电极反应式为
纳米片电极的电极反应式为
您最近半年使用:0次
解题方法
2 . 高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是
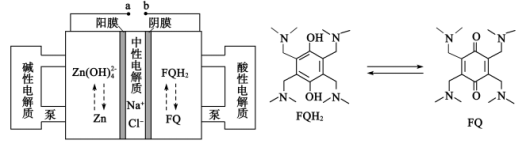

| A.放电时,正极区溶液的pH增大 |
B.放电时,负极反应式: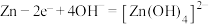 |
| C.充电时,电极a连接电源负极 |
| D.充电时,负极材料每增重13g,中性电解质溶液减少11.7g |
您最近半年使用:0次
2023-01-12更新
|
310次组卷
|
3卷引用:山东省菏泽市单县第二中学2022-2023学年高三下学期开学第一次模拟考试化学试题
名校
解题方法
3 . 铁-铬液流电池的装置如下图所示,下列说法错误的是


A.放电时, 通过质子交换膜向Y电极移动 通过质子交换膜向Y电极移动 |
B.通过该原电池反应可知氧化性: |
C.充电时,X电极的电极反应式为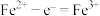 |
| D.充电完成后,可将电解质溶液泵回储液罐,将能量储存起来 |
您最近半年使用:0次
2022-09-03更新
|
190次组卷
|
2卷引用:山东省日照市2022-2023学年高二上学期8月校际联考化学试题
名校
4 . 某化学兴趣小组设计如图所示装置来研究电化学知识。
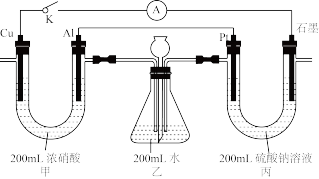
回答下列问题:
(1)闭合开关K,丙装置将___________ 能转化为___________ 能。Pt电极的名称___________ (填“正”、“负”、“阴”或“阳”)极,石墨电极上的电极反应式为___________ 。
(2)乙装置锥形瓶中发生反应的化学方程式为___________ 、___________ ;长颈漏斗的作用是___________ 。
(3)若装置气密性良好,乙中反应进行完全,当电路中有0.1mol电子发生转移时,理论上乙中生成物质的物质的量浓度为___________ (忽略溶液体积变化)。
(4)某小组在反应进行一段时间后断开开关K过一段时间再闭合开关K发现电流表指针偏转的方向与开始时不同,出现该现象的原因可能是___________ 。

回答下列问题:
(1)闭合开关K,丙装置将
(2)乙装置锥形瓶中发生反应的化学方程式为
(3)若装置气密性良好,乙中反应进行完全,当电路中有0.1mol电子发生转移时,理论上乙中生成物质的物质的量浓度为
(4)某小组在反应进行一段时间后断开开关K过一段时间再闭合开关K发现电流表指针偏转的方向与开始时不同,出现该现象的原因可能是
您最近半年使用:0次
2022-01-23更新
|
242次组卷
|
6卷引用:河南省许平汝联盟2021-2022学年高二下学期开学考试化学试题
名校
解题方法
5 . 一种聚合物锂电池通过充、放电可实现“大气固碳”(如图所示)。该电池在充电时,通过催化剂的选择性控制,只有Li2CO3发生氧化释放出CO2和O2。下列说法正确的是
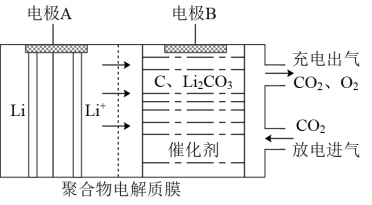

| A.该电池可选用含Li+的水溶液作电解质 |
| B.图中Li+的移动方向是充电时的移动方向 |
| C.充电时,阳极发生的反应为2Li2CO3+C-4e-=3CO2+4Li+ |
| D.该电池每循环充、放电子各4mol,理论上可固定CO2标准状况下22.4L |
您最近半年使用:0次
2022-01-20更新
|
1251次组卷
|
9卷引用:江苏省南京师范大学附属中学2021-2022学年高三下学期开学考试化学试题
江苏省南京师范大学附属中学2021-2022学年高三下学期开学考试化学试题 江苏省无锡市普通高中2021-2022学年上学期高三期末调研考试化学试题(已下线)一轮巩固卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(广东专用)(已下线)黄金卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省泰州中学2021-2022学年高二下学期第一次质量检测化学试题天津市和平区2022届高三一模化学试题(已下线)押江苏卷第12题 电化学及其应用 -备战2022年高考化学临考题号押题(江苏卷)(已下线)2022年广东卷高考真题变式题(11-16)广东省普宁市华侨中学2021-2022学年高三下学期第二次模拟考化学试题
名校
解题方法
6 . 以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2和 CO2:
2NO(g)+2CO(g) N2(g)+2CO2(g) △H =-746.5 kJ/mol ①
N2(g)+2CO2(g) △H =-746.5 kJ/mol ①
(1)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应① 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图1所示:
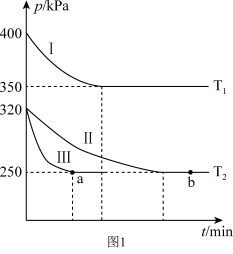
①温度:T1___________ T2(填“<”“=”或“>”)。
②CO 的平衡转化率:Ⅰ___________ Ⅱ___________ Ⅲ(填“<”“=”或“>”)。
③反应速率:a 点的 v(逆)___________ b 点的 v(正) (填“<”“=”或“>”)。
④T2时的平衡常数 Kp=___________ 。(Kp表示用平衡分压表示的平衡常数,各物质的分压=总压×各物质在混合气体中所占的物质的量分数)
(2)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图2所示。M 点___________ (填“是”或“不是”)对应温度下的平衡脱氮率, 说明理由___________ 。
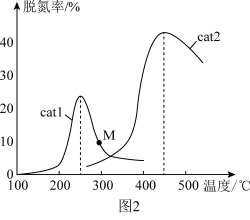
II.将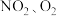 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如图3所示。
制成燃料电池,模拟工业电解法精炼银,装置如图3所示。

(3)①甲池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ附近发生的电极反应方程式为___________ 。
②若用10A的电流电解50min后,乙中阴极得到21.6gAg,则该电解池的电解效率为___________ %。(保留小数点后一位)。已知:通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为96500C•mol﹣1
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2和 CO2:
2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H =-746.5 kJ/mol ①
N2(g)+2CO2(g) △H =-746.5 kJ/mol ①(1)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应① 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图1所示:

①温度:T1
②CO 的平衡转化率:Ⅰ
③反应速率:a 点的 v(逆)
④T2时的平衡常数 Kp=
(2)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图2所示。M 点

II.将
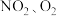 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如图3所示。
制成燃料电池,模拟工业电解法精炼银,装置如图3所示。
(3)①甲池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ附近发生的电极反应方程式为
②若用10A的电流电解50min后,乙中阴极得到21.6gAg,则该电解池的电解效率为
您最近半年使用:0次
名校
7 . 某研究机构使用Li—SO2Cl2电池作为电源电解制备Ni(H2PO2)2,其工作原理如图所示。已知电池反应为2Li+SO2Cl2=2LiCl+SO2↑,下列说法错误的是
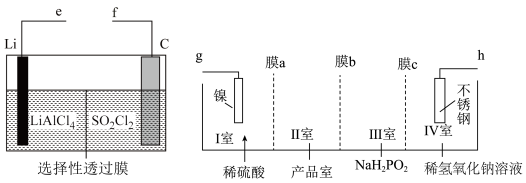

| A.电池中C电极的电极反应式为SO2Cl2+2e-=2Cl-+SO2↑ |
| B.电池的e极连接电解池的g极 |
| C.膜a、c是阳离子交换膜,膜b是阴离子交换膜 |
| D.电解池中不锈钢电极附近溶液的pH增大 |
您最近半年使用:0次
2021-01-01更新
|
1964次组卷
|
15卷引用:山东省郓城第一中学2023-2024学年高二上学期开学考试化学试题
山东省郓城第一中学2023-2024学年高二上学期开学考试化学试题河北省“五个一名校联盟”(张家口一中、唐山一中、保定一中、邯郸一中、邢台一中)2021届高三上学期第一次诊断考试化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)北京市昌平区新学道临川学校2021届高三上学期期末考试化学试题(已下线)小题19 多池多室带膜电化学装置 ——备战2021年高考化学经典小题考前必刷(全国通用)四川省成都市树德中学2020-2021学年高二下学期4月月考化学试题(已下线)课时31 新型电解池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题六 化学反应与能量 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)山东师范大学附属中学2022-2023学年高二上学期第一次月考化学试题山东省2022-2023学年高二上学期学业水平测试化学试题福建省泉州市第七中学2022-2023学年高三上学期期中考化学试题(已下线)回归教材重难点07 重温“两池”原理-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)第4讲 电解池 金属的电化学腐蚀与防护河南省南阳市第一中学校2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
8 . 如图是一个电化学过程的示意图,请按要求回答下列问题
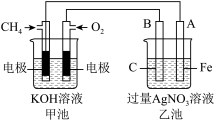
(1)甲池是___________ 装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入CH4的电极___________ 。
(3)反应一段时间后,甲池中消耗 1.6 g甲烷,则乙池中某电极的质量增加__________ g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是___________ 。
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。
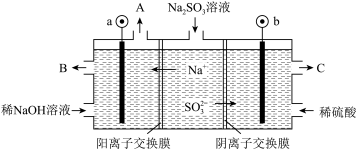
①图中a极要连接电源的___________ (填“正”或“负”)极,C口流出的物质是___________ 。
②SO 放电的电极反应式为
放电的电极反应式为___________ 。
③阴极的电极反应式为___________ 。

(1)甲池是
(2)写出电极反应式:通入CH4的电极
(3)反应一段时间后,甲池中消耗 1.6 g甲烷,则乙池中某电极的质量增加
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。

①图中a极要连接电源的
②SO
 放电的电极反应式为
放电的电极反应式为③阴极的电极反应式为
您最近半年使用:0次
2020-12-24更新
|
296次组卷
|
2卷引用:福建省宁化第一中学2021-2022学年高二上学期开学考试化学试题
9 . 如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是( )
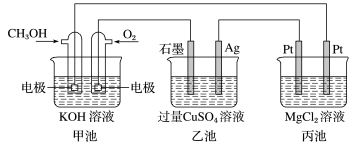
| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+ |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度 |
| D.甲池中消耗280mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体 |
您最近半年使用:0次
2020-05-16更新
|
1352次组卷
|
39卷引用:2016-2017学年甘肃省天水市第一中学高二下学期开学考试化学试卷
2016-2017学年甘肃省天水市第一中学高二下学期开学考试化学试卷(已下线)2011届江苏省苏锡常镇四市高三调研测试(一)化学试卷(已下线)2011届湖北省天门市高三模拟考试(三)(理综)化学部分(已下线)2012届浙江省重点中学协作体高三3月调研理综部分(已下线)2012届江苏省扬州中学高三3月双周练习(二)化学试卷(已下线)2014高考名师推荐化学电解规律及电化学计算(已下线)2014届江西省玉山一中高三化学强化周考(十三)试卷2015届河南省新密市青屏高中高三第三次月考化学试卷2014-2015学年湖北省武汉市第二中学高一下期末化学试卷2015-2016学年吉林省吉林一中高二上期中考试化学试卷2015-2016学年山东省新泰一中高二上学期期中测试化学试卷2016届甘肃省嘉峪关一中高三上第三次模拟考试化学试卷江西省抚州市临川第二中学2015-2016学年高二上12月月考化学试卷2016届四川省新津中学高三下学期3月月考化学试卷12016届四川省新津中学高三下学期3月月考化学试卷22015-2016学年河北省定州中学高二6月月考化学试卷2017届河北省沧州市第一中学高三上周测化学试卷2017届湖南省长沙市长郡中学高三上学期第三次月考模拟化学试卷2016-2017学年辽宁省实验中学分校高二上期中化学卷2016-2017学年江西省南昌市第二中学高二上学期期末考试化学试卷2016-2017学年甘肃省天水市第一中学高二下学期开学考试(寒假作业检测)化学试卷山西省康杰中学2018届高三上学期第一次月考化学试卷河北省邢台市第一中学2017-2018学年高二上学期第二次月考化学试题湖南省衡阳市第八中学2018届高三(实验班)第三次质检化学试题四川省广安市第二中学校2017-2018学年高二下学期第二次月考化学试题山西省运城市临猗中学2019届高三上学期第一次月考化学试题河北省承德市第一中学2018-2019学年高一下学期第三次月考化学试题河南省南阳市2018-2019学年高二上学期期中质量评估化学试题2020届高三化学化学二轮复习——高考常考题型:离子放电顺序及电解规律【夯基提能】【精编30题】河北省石家庄外国语学校2019-2020学年高二上学期期末考试化学试题(已下线)【南昌新东方】2019-2020 南昌五中高一下第一次月考人教版(2019)高二化学选择性必修1第四章 化学反应与电能 第二节 电解池 课时2 电解原理的应用黑龙江省哈尔滨市第一中学2021届高三上学期期中考试化学试题(已下线)第四章 化学反应与电能(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题浙江省温州市2021-2022学年高二上学期12月普通高中学考适应性测试化学试题江西省宜春市万载中学2021-2022学年高二上学期第二次月考化学试题(已下线)专题八 电化学的相关计算



