名校
1 . 某粗铜产品中含有Zn、Ag、Au等杂质,如图所示,用CH3OH-碱性燃料电池电解硫酸铜溶液。闭合电键K进行电解。下列说法中不正确的是( )


| A.左池负极反应式为CH3OH -6e-+8OH-=CO32-+ 6H2O |
| B.通电一段时间后,Ag、Au杂质金属沉积在电解槽底部 |
| C.若粗铜电极质量减少6.4g,则纯铜电极增重大于6.4g |
| D.电解过程中右池纯铜和粗铜分别为阴极和阳极 |
您最近一年使用:0次
2018-01-16更新
|
610次组卷
|
8卷引用:安徽省怀宁中学2019-2020学年高二上学期开学考试化学试题
名校
2 . 如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。下列有关说法正确的是
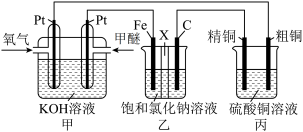

| A.反应一段时间后,乙装置中生成的氢氧化钠在铁极区 |
| B.乙装置中铁电极为阴极,电极反应式为Fe-2e-= Fe2+ |
| C.反应一段时间后,丙装置中硫酸铜溶液浓度保持不变 |
| D.通入氧气的一极为正极,发生的电极反应为O2 - 4e- + 2H2O = 4OH- |
您最近一年使用:0次
2018-01-10更新
|
359次组卷
|
13卷引用:山东省栖霞市第一中学2021-2022学年高三上学期开学摸底考试化学试题
山东省栖霞市第一中学2021-2022学年高三上学期开学摸底考试化学试题2016届湖北省七市(州)高三下学期3月联合调研理综化学试卷辽宁省葫芦岛市六校协作体2016-2017学年高二上学期期中联考化学试题山西省实验中学2018届高三上学期第二次月考化学试题北京市昌平区2018届高三化学12月月考试题(已下线)【中等生百日捷进提升系列-技能方法】专题08 电解池类选择题解题方法和策略重庆市万州第二高级中学2018-2019学年高二上学期期中考试化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高一下学期第二次考试化学试题河北安平中学2019-2020学年高二上学期第二次月考化学试题山东省实验中学2021届高三上学期第一次诊断考试化学试题山东省济南市莱芜一中2021届高三1月份月考化学试题山东省蓬莱第二中学2021-2022学年高三上学期第一次月考化学试题福建省福州市四校联盟2022-2023学年高二下学期期末联考化学试题
名校
解题方法
3 . 某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
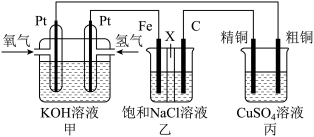
根据要求回答相关问题:
(1)通入氢气的电极为________ (填“正极”或“负极”),负极的电极反应式为__________ 。
(2)石墨电极为________ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,________ (填“铁极”或“石墨极”)区的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将________ (填“增大”“减小”或“不变”)。精铜电极上的电极反应式为____________________ 。

根据要求回答相关问题:
(1)通入氢气的电极为
(2)石墨电极为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
您最近一年使用:0次
2017-12-18更新
|
157次组卷
|
5卷引用:新疆维吾尔自治区塔城地区2022-2023学年高二下学期开学考试化学试题
名校
4 . 如图所示,甲池的总反应式为N2H4+O2===N2+2H2O。下列说法正确的是( )
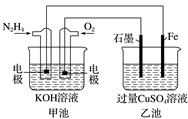

| A.甲池中负极上的电极反应式为N2H4-4e-===N2+4H+ |
| B.乙池中石墨电极上发生的反应为4OH--4e-===2H2O+O2↑ |
| C.甲池溶液pH增大,乙池溶液pH减小 |
| D.甲池中每消耗0.1 mol N2H4乙池电极上则会析出6.4 g固体 |
您最近一年使用:0次
2017-12-12更新
|
420次组卷
|
7卷引用:辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题
辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题黑龙江省哈尔滨市第六中学2018届高三12月月考化学试题山西省朔州市应县第一中学2017-2018学年高二上学期月考(四)化学试题福建省厦门市湖滨中学2017-2018学年高二下学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期12月月考化学试题(已下线)第21讲 电解池 金属的电化学腐蚀与防护 (精练)-2021年高考化学一轮复习讲练测(已下线)专题讲座(四)新型电源及电极反应式的书写(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
名校
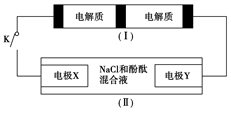
5 . 下图装置(Ⅰ)是一种可充电电池,装置(Ⅱ)为电解池。装置(Ⅰ)的离子交换膜只允许Na+通过,已知电池充、放电的化学方程式为2Na2S2+NaBr3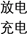 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是
| A.闭合开关K时,Na+从右到左通过离子交换膜 |
| B.闭合开关K时,负极反应式为3NaBr-2e-===NaBr3+2Na+ |
| C.闭合开关K时,当有0.1 mol Na+通过离子交换膜时,X电极上放出标准状况下气体1.12 L |
| D.闭合开关K时,X电极反应式为2Cl--2e-===Cl2↑ |
您最近一年使用:0次
2017-12-07更新
|
161次组卷
|
6卷引用:云南省大理州漾濞一中2020届高三上学期开学考试化学试题
云南省大理州漾濞一中2020届高三上学期开学考试化学试题(已下线)2012届湖南省四市九校高三上学期第一次联考化学试卷(已下线)2012-2013学年江苏省郑梁梅中学高二下学期期末考试化学试卷河北省衡水市安平中学2018届高三上学期期中考试化学试题安徽省滁州市民办高中2019-2020学年高二下学期期末考试化学试题(已下线)第24讲 电解池与金属腐蚀与保护-2021年高考化学一轮复习名师精讲练
名校
解题方法
6 . 某实验小组同学利用下图装置对电化学原理进行了一系列探究活动。

(1)甲池为装置_______ (填“原电池”或“电解池”)。
(2)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,导线中通过_________ mol电子。
(3)实验过程中,甲池左侧烧杯中NO3-的浓度_______ (填“变大”、“变小”或“不变”)。
(4)其他条件不变,若用U形铜棒代替“盐桥”,工作一段时间后取出铜棒称量,质量___________ (填“变大”、“变小”或“不变”)。若乙池中的某盐溶液是足量AgNO3溶液,则乙池中左侧Pt电极反应式为___________________________________ ,工作一段时间后,若要使乙池溶液恢复原来浓度,可向溶液中加入_____________ (填化学式)。

(1)甲池为装置
(2)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,导线中通过
(3)实验过程中,甲池左侧烧杯中NO3-的浓度
(4)其他条件不变,若用U形铜棒代替“盐桥”,工作一段时间后取出铜棒称量,质量
您最近一年使用:0次
2017-11-30更新
|
406次组卷
|
4卷引用:四川省棠湖中学2017-2018学年高二下学期开学考试化学试题
名校
7 . 下图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀铜,接通
上的c点显红色.为实现铁上镀铜,接通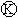 后,使c、d两点短路.下列叙述不正确的是
后,使c、d两点短路.下列叙述不正确的是
 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀铜,接通
上的c点显红色.为实现铁上镀铜,接通 后,使c、d两点短路.下列叙述不正确的是
后,使c、d两点短路.下列叙述不正确的是
| A.a为直流电源的负极 | B.c极发生的反应为2H++2e-=H2↑ |
| C.e电极为铜板 | D.f极发生还原反应 |
您最近一年使用:0次
名校
8 . 关于如图所示装置的叙述中正确的是


| A.若仅闭合K2,铁极的电极反应式:Fe – 2e=Fe2+ |
| B.若仅闭合K2,炭极上发生还原反应 |
| C.若仅闭合K1,电流由炭极沿导线流向铁极 |
| D.若仅闭合K1,炭极的电极反应式: O2+4e+4H+=2H2O |
您最近一年使用:0次
名校
解题方法
9 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合装置的电键时,观察到电流表的指针发生了偏转.请回答下列问题:

(1)甲装置的名称是______ ;Pt为 ______ 极(A.正 B.负C.阳 D.阴).
(2)写出电极反应式:Cu极______ ,C极 ______ .
(3)若乙中电极不变,将其溶液换成饱和NaCl溶液,乙中溶液的总反应的离子方程式为______ ;若要使溶液恢复到原饱和溶液的浓度,需要加入的物质是 ______ (填名称);
(4)若乙中电极不变,将其溶液换成饱和CuSO4溶液,当甲中产生0.1mol气体时,线路中转移的电子数是______ ;乙中溶液H+的浓度是 ______ (假设溶液体积是200mL,且电解过程中溶液体积不变).

(1)甲装置的名称是
(2)写出电极反应式:Cu极
(3)若乙中电极不变,将其溶液换成饱和NaCl溶液,乙中溶液的总反应的离子方程式为
(4)若乙中电极不变,将其溶液换成饱和CuSO4溶液,当甲中产生0.1mol气体时,线路中转移的电子数是
您最近一年使用:0次
名校
10 . (1)原电池反应通常是放热反应,下列反应中在理论上可设计成原电池的反应为________ (填字母), 理由是_______________________________________ 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(l) △H>0
C.CaC2(s)+2H2O(l)=Ca(OH)2(s)+C2H2(g) △H <0
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H <0
(2)以KOH溶液为电解质溶液,依据(1)所选反应设计原电池,其负极反应为________________ 。
(3)电解原理在化学工业中有着广泛的应用,现将设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y为两块电极板,则:
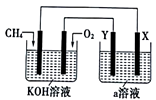
①若X和Y均为惰性电极,a为饱和NaCl溶液,则电解时检验Y电极反应产物的方法是___________ 。
②若X和Y分别为石墨和铁,a仍为饱和NaCl溶液,则电解过程中生成的白色固体物质露置在空气中,可观察到的现象是________________________________ 。
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1 molCuO,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为__________ 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(l) △H>0
C.CaC2(s)+2H2O(l)=Ca(OH)2(s)+C2H2(g) △H <0
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H <0
(2)以KOH溶液为电解质溶液,依据(1)所选反应设计原电池,其负极反应为
(3)电解原理在化学工业中有着广泛的应用,现将设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y为两块电极板,则:

①若X和Y均为惰性电极,a为饱和NaCl溶液,则电解时检验Y电极反应产物的方法是
②若X和Y分别为石墨和铁,a仍为饱和NaCl溶液,则电解过程中生成的白色固体物质露置在空气中,可观察到的现象是
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1 molCuO,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为
您最近一年使用:0次



