名校
解题方法
1 . 利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是
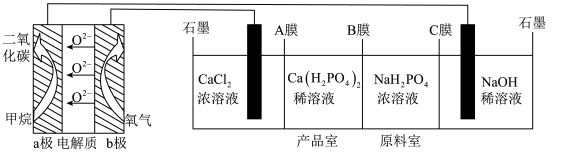
| A.a极反应:CH4-8e﹣+4O2﹣=CO2+2H2O |
| B.A、C膜均为阳离子交换膜,B膜为阴离子交换膜 |
| C.a极上通入标况下2.24L甲烷,阳极室Ca2+减少0.2mol |
| D.阳极室有氯气产生,阴极室中有氢气产生且NaOH浓度增大 |
您最近一年使用:0次
23-24高二上·广东深圳·期末
名校
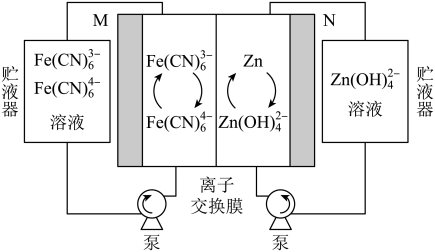
2 . 碱性锌-铁液流电池(如图)具有电压高、成本低的优点。该电池的总反应为:Zn+2Fe(CN) +4OH-
+4OH- 2Fe(CN)
2Fe(CN) +Zn(OH)
+Zn(OH) 。下列叙述正确的是
。下列叙述正确的是
 +4OH-
+4OH- 2Fe(CN)
2Fe(CN) +Zn(OH)
+Zn(OH) 。下列叙述正确的是
。下列叙述正确的是
| A.放电时,右侧贮液器中溶液浓度减小 |
| B.充电时,M电极与电源负极相连 |
C.充电时,M极电极反应式为Fe(CN) -e-=Fe(CN) -e-=Fe(CN) |
| D.放电时,电路中转移2mol电子时,负极区电解质溶液增加65g |
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作对应的离子方程式错误是
A.电解饱和MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
B.向Al2(SO4)3溶液中滴入NaHCO3溶液:Al3++3 =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
C.向Na2S2O3溶液中滴入稀H2SO4溶液:2H++ =S↓+SO2↑+H2O =S↓+SO2↑+H2O |
D.用Na2CO3溶液处理水垢中的CaSO4: (aq)+CaSO4(s)⇌CaCO3(s)+ (aq)+CaSO4(s)⇌CaCO3(s)+ (aq) (aq) |
您最近一年使用:0次
2024-01-27更新
|
642次组卷
|
5卷引用:广东省深圳市高级中学2023-2024学年高二上学期期末考试化学试题
广东省深圳市高级中学2023-2024学年高二上学期期末考试化学试题福建省厦门外国语学校2023-2024学年高二上学期期末模拟考试化学试题湖北省重点高中智学联盟2023-2024学年高二上学期12月联考化学试题 (已下线)化学(九省联考考后提升卷,贵州卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点03 离子方程式的正误判断、离子共存
解题方法
4 . 废旧锌锰电池回收处理可实现资源的再利用,初步处理后的废料中含有MnO2、MnOOH、Zn(OH)2、及Fe等,用该废料制备Zn和MnO2的一种工艺流程如下:
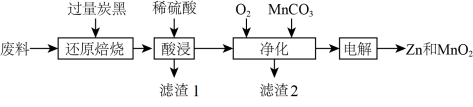
资料a:Mn的金属活动性强于Fe;
Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b:生成氢氧化物沉淀的pH
回答下列问题:
(1)“还原焙烧”是为了把Mn元素转化为MnO,请写出MnOOH发生反应的化学方程式_______ 。
(2)为了提高“酸浸”的速率,可以采取的措施有_______ ;滤渣1的主要成分为_______ 。
(3)“净化”时通入O2的目的是_______ ,加入MnCO3时必须控制pH范围为_______ ;检验净化后的溶液中是否含有Fe元素的试剂是_______ 。
(4)“电解”时MnO2在_______ (填“阳”或“阴”)极生成,其电极反应式为_______ 。

资料a:Mn的金属活动性强于Fe;
Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b:生成氢氧化物沉淀的pH
| Mn(OH)2 | Zn(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 8.1 | 6.2 | 1.9 |
| 完全沉淀时 | 10.1 | 8.2 | 3.2 |
(1)“还原焙烧”是为了把Mn元素转化为MnO,请写出MnOOH发生反应的化学方程式
(2)为了提高“酸浸”的速率,可以采取的措施有
(3)“净化”时通入O2的目的是
(4)“电解”时MnO2在
您最近一年使用:0次
名校
5 . 电镀实验在生产生活中应用广泛。
Ⅰ.某实验小组设计了如图在纽扣上电镀铜的实验装置:

(1)如图中,石墨是___________ (填阴极或阳极),对应的电极方程式为:___________ ;如图装置电解一段时间后,溶液中___________ (填微粒化学式)浓度下降,从而影响镀铜的速率和质量。
Ⅱ.实验小组利用如图装置进行铁上电镀铜的实验探究:
(2)实验①中,无色气体产生的原因是 或
或___________ 。
(3)实验①中,气体减少,推测是由于溶液中 减少,且
减少,且___________ 。
(4)欲测定实验①溶液中 的浓度,需要用容量瓶配制某标准溶液,定容时当液面离容量瓶颈部的刻度线
的浓度,需要用容量瓶配制某标准溶液,定容时当液面离容量瓶颈部的刻度线 时,改用胶头滴管滴加蒸馏水至溶液的
时,改用胶头滴管滴加蒸馏水至溶液的___________ ,用 标准溶液滴定时应选用
标准溶液滴定时应选用___________ 滴定管(填“酸式”或“碱式”)。
(5)为确定实验①电解质溶液中 的准确浓度
的准确浓度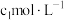 ,实验操作为:准确量取
,实验操作为:准确量取 含有
含有 的溶液于带塞锥形瓶中,调节溶液
的溶液于带塞锥形瓶中,调节溶液 ,加入过量的
,加入过量的 ,用
,用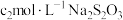 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 。上述过程中反应的离子方程式:
。上述过程中反应的离子方程式: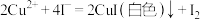 ,
, 。滴定选用的指示剂为
。滴定选用的指示剂为___________ ,滴定终点观察到的现象为:当滴入最后半滴标准溶液时,锥形㼛中溶液___________ 。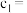
___________ (用 、
、 、
、 等的代数式表示)。滴定终点时,某同学俯视读数,其他操作均正确,则测定结果
等的代数式表示)。滴定终点时,某同学俯视读数,其他操作均正确,则测定结果___________ (填“偏大”“偏小”或“无影响”)。
(6)实验②中, 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为___________ ,反应后的体系呈___________ 色。
Ⅰ.某实验小组设计了如图在纽扣上电镀铜的实验装置:

(1)如图中,石墨是
Ⅱ.实验小组利用如图装置进行铁上电镀铜的实验探究:
| 装置示意图 | 序号 | 电解质溶液 | 实验现象 |
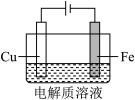 | ① | 0.1mol/L +少量 +少量 | 阴极表面有无色气体,一段时间后阴极表面有红色固体,气体减少。经检验,铁电极表面有 生成。 生成。 |
| ② | 0.1mol/L +过量氨水 +过量氨水 | 阴极表面未观察到气体,一段时间后阴极表面有致密红色固体,经检验,电解液中无Fe元素。 |
 或
或(3)实验①中,气体减少,推测是由于溶液中
 减少,且
减少,且(4)欲测定实验①溶液中
 的浓度,需要用容量瓶配制某标准溶液,定容时当液面离容量瓶颈部的刻度线
的浓度,需要用容量瓶配制某标准溶液,定容时当液面离容量瓶颈部的刻度线 时,改用胶头滴管滴加蒸馏水至溶液的
时,改用胶头滴管滴加蒸馏水至溶液的 标准溶液滴定时应选用
标准溶液滴定时应选用(5)为确定实验①电解质溶液中
 的准确浓度
的准确浓度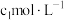 ,实验操作为:准确量取
,实验操作为:准确量取 含有
含有 的溶液于带塞锥形瓶中,调节溶液
的溶液于带塞锥形瓶中,调节溶液 ,加入过量的
,加入过量的 ,用
,用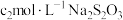 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 。上述过程中反应的离子方程式:
。上述过程中反应的离子方程式: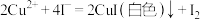 ,
, 。滴定选用的指示剂为
。滴定选用的指示剂为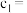
 、
、 、
、 等的代数式表示)。滴定终点时,某同学俯视读数,其他操作均正确,则测定结果
等的代数式表示)。滴定终点时,某同学俯视读数,其他操作均正确,则测定结果(6)实验②中,
 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为
您最近一年使用:0次
2023-07-13更新
|
158次组卷
|
2卷引用:广东省四校(华附,省实,广雅,深中)2022-2023学年高二下学期期末联考化学试题
解题方法
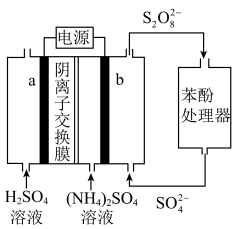
6 .  电化学循环氧化法可用于废水中苯酚降解成
电化学循环氧化法可用于废水中苯酚降解成 ,工作原理如图所示,下列说法正确的是
,工作原理如图所示,下列说法正确的是
 电化学循环氧化法可用于废水中苯酚降解成
电化学循环氧化法可用于废水中苯酚降解成 ,工作原理如图所示,下列说法正确的是
,工作原理如图所示,下列说法正确的是
A.电极 是阴极,发生还原反应 是阴极,发生还原反应 |
B.a电极的电极反应式为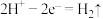 |
C.电解时, 通过阴离子交换膜从右向左迁移 通过阴离子交换膜从右向左迁移 |
D.电路中通过 电子时,理论上可处理 电子时,理论上可处理 苯酚 苯酚 |
您最近一年使用:0次
解题方法
7 . 含有硝酸盐和亚硝酸盐的酸性废水可导致水体富营养化,引发环境污染。如图是利用电化学原理处理 的原理,下列有关叙述错误的是
的原理,下列有关叙述错误的是

 的原理,下列有关叙述错误的是
的原理,下列有关叙述错误的是
A.直流电源为铅蓄电池时, 极连接Y电极 极连接Y电极 |
| B.Y电极发生还原反应 |
C.当产生 时,有 时,有 跨膜而过 跨膜而过 |
D.阳极电极反应方程式为: |
您最近一年使用:0次
解题方法
8 . 下列方程式正确的是
A.铁与稀硫酸反应的离子方程式: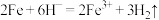 |
B.电解熔融 : : |
C.酸性高锰酸钾溶液和草酸溶液反应: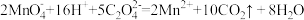 |
D.向氯水中加入碳酸钠: |
您最近一年使用:0次
解题方法
9 . 工业上 加氢制
加氢制 ,为
,为 的减排与再利用提供了一种新策略,该过程中存在如下反应:
的减排与再利用提供了一种新策略,该过程中存在如下反应:
反应Ⅰ:
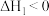
反应Ⅱ:

回答下列问题:
(1)已知: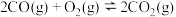

则反应

_______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)关于反应Ⅰ,下列说法正确的有_______(填标号)。
(3)向恒压密闭装置中充入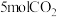 和
和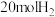 ,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得
,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得 和
和 的物质的量
的物质的量 随温度
随温度 变化关系如图所示。
变化关系如图所示。

①曲线 对应物质为
对应物质为_______ (填化学式)。
② 达平衡时,
达平衡时, 的总转化率为
的总转化率为_______  。
。
③结合图像分析,达平衡时装置中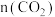 随温度升高的变化趋势为
随温度升高的变化趋势为_______ (填标号)。
A.减小 B.增大 C.先减小后增大 D.先增大后减小
④工业制备 通常控制温度在
通常控制温度在 ℃之间的原因是
℃之间的原因是_______ 。
(4)采用下图装置能实现 电化学法制
电化学法制 ,同时获得副产物
,同时获得副产物 。
。

①铜电极的电极反应式为_______ 。
②每制得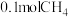 ,理论上
,理论上 电极生成
电极生成_______ 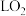 (折算为标准状况)。
(折算为标准状况)。
 加氢制
加氢制 ,为
,为 的减排与再利用提供了一种新策略,该过程中存在如下反应:
的减排与再利用提供了一种新策略,该过程中存在如下反应:反应Ⅰ:

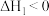
反应Ⅱ:


回答下列问题:
(1)已知:
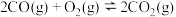

则反应


 、
、 、
、 的代数式表示)。
的代数式表示)。(2)关于反应Ⅰ,下列说法正确的有_______(填标号)。
| A.反应物的键能之和高于生成物的键能之和 |
| B.低温条件有利于该反应自发进行 |
| C.混合气体的平均摩尔质量不再改变,说明反应已达平衡 |
D.恒容条件下,充入更多的 能提高单位体积活化分子的百分数 能提高单位体积活化分子的百分数 |
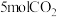 和
和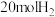 ,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得
,在不同温度下同时发生反应Ⅰ和Ⅱ,达平衡时,测得 和
和 的物质的量
的物质的量 随温度
随温度 变化关系如图所示。
变化关系如图所示。
①曲线
 对应物质为
对应物质为②
 达平衡时,
达平衡时, 的总转化率为
的总转化率为 。
。③结合图像分析,达平衡时装置中
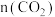 随温度升高的变化趋势为
随温度升高的变化趋势为A.减小 B.增大 C.先减小后增大 D.先增大后减小
④工业制备
 通常控制温度在
通常控制温度在 ℃之间的原因是
℃之间的原因是(4)采用下图装置能实现
 电化学法制
电化学法制 ,同时获得副产物
,同时获得副产物 。
。
①铜电极的电极反应式为
②每制得
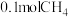 ,理论上
,理论上 电极生成
电极生成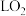 (折算为标准状况)。
(折算为标准状况)。
您最近一年使用:0次
解题方法
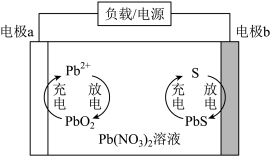
10 . 一种由我国科学家研发的水系 电池的结构及工作原理如图所示,其中电极
电池的结构及工作原理如图所示,其中电极 为碳电极,电极
为碳电极,电极 为掺有硫单质的碳电极。下列说法不正确的是
为掺有硫单质的碳电极。下列说法不正确的是
 电池的结构及工作原理如图所示,其中电极
电池的结构及工作原理如图所示,其中电极 为碳电极,电极
为碳电极,电极 为掺有硫单质的碳电极。下列说法不正确的是
为掺有硫单质的碳电极。下列说法不正确的是
A.放电时,电极 为负极 为负极 |
B.充电时,电极 发生反应: 发生反应: |
C.放电时,电极 附近溶液的 附近溶液的 逐渐减小 逐渐减小 |
D.充电时,每转移 电子,阴极质量理论上减少 电子,阴极质量理论上减少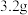 |
您最近一年使用:0次



