1 . 以原油为原料生产聚烯烃的几个步骤如下:
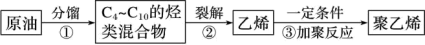
(1)步骤①使用的方法是分馏,分馏是利用原油中各组分的______ 不同进行分离的过程。
(2)步骤①所得C4~C10的烃类混合物中所含的物质超过 7 种。请以C4H10为例说明其原因______ 。
(3)步骤③中,聚烯烃的合成反应与聚乙烯的相同,该反应类型是_____ 。生产的聚丙烯可用下图表示,其重复结构单元是_________ 。

(4)乙烯是一种重要的基本化工原料,可制备乙酸乙酯,其转化关系如图。
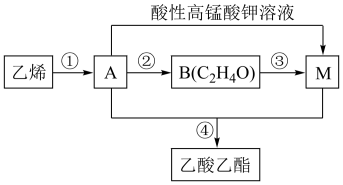
已知:H2C==CHOH 不稳定
I.①的反应类型是______ 。
II.B的结构简式是_______ 。
III.④的化学方程式是_______ 。
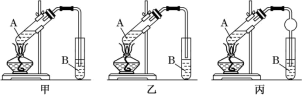
IV.实验室制取乙酸乙酯的装置如图所示。能完成本实验的装置是_____ (填“甲”“乙”或“丙”),试管B 内盛放的液体是___________ 。

(1)步骤①使用的方法是分馏,分馏是利用原油中各组分的
(2)步骤①所得C4~C10的烃类混合物中所含的物质超过 7 种。请以C4H10为例说明其原因
(3)步骤③中,聚烯烃的合成反应与聚乙烯的相同,该反应类型是

(4)乙烯是一种重要的基本化工原料,可制备乙酸乙酯,其转化关系如图。

已知:H2C==CHOH 不稳定
I.①的反应类型是
II.B的结构简式是
III.④的化学方程式是
IV.实验室制取乙酸乙酯的装置如图所示。能完成本实验的装置是

您最近一年使用:0次
2 . 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。加热聚丙烯废塑料得到的产物如下表:

(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物 电石
电石 乙炔
乙炔 聚乙炔
聚乙炔
写出反应②和反应③的化学方程式:_______ 、_______ 。
(2)乙装置试管中收集到的产品的成分为_______ ,最后收集到的气体产物为_______ 。
(3)写出一个丙装置中发生反应的方程式_______ 。属于______ 反应
(4)写出产物中苯与硝酸制备硝基苯的方程式_______ 。属于______ 反应。
(5)下列有关该实验各产物的叙述正确的是
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物
 电石
电石 乙炔
乙炔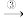 聚乙炔
聚乙炔写出反应②和反应③的化学方程式:
(2)乙装置试管中收集到的产品的成分为
(3)写出一个丙装置中发生反应的方程式
(4)写出产物中苯与硝酸制备硝基苯的方程式
(5)下列有关该实验各产物的叙述正确的是
| A.甲烷的二氯代物(CH2Cl2)有2种 |
| B.装置乙试管中收集到的液体可以使溴水褪色 |
| C.装置丙中试剂吸收气体后所得产物密度均比水小 |
| D.最后收集的气体可以作为清洁燃料使用 |
您最近一年使用:0次
解题方法
3 . 某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
已知: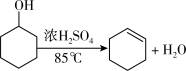
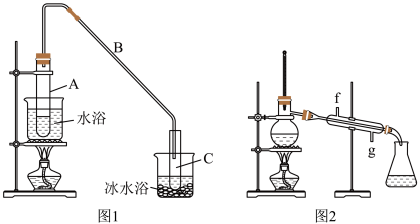
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________ ,导管B除了导气外还具有的作用是____________ ;
②试管C置于冰水浴中的目的是______________________ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环乙烯在______ 层(填上或下),分液后用___________ (填入编号)洗涤。
a.KMnO4溶液b.稀H2SO4c.Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从________ 口进入,收集产品时,控制的温度应在______ 左右。
(3)以下区分环己烯精品和粗品的方法,合理的是_____________ 。
a.用酸性高锰酸钾溶液b.用NaOH溶液c.测定沸点
已知:


| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是
②试管C置于冰水浴中的目的是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环乙烯在
a.KMnO4溶液b.稀H2SO4c.Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从
(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液b.用NaOH溶液c.测定沸点
您最近一年使用:0次
2020-05-18更新
|
214次组卷
|
3卷引用:天津市红桥区2016-2017学年高二下学期期末考试化学试题
天津市红桥区2016-2017学年高二下学期期末考试化学试题辽宁省营口市部分重点高中2017-2018学年高二下学期期中考试化学试题(已下线)1.2.1 有机化合物的分离、提纯(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修3)
解题方法
4 . 已知乙烯能发生如图转化关系:
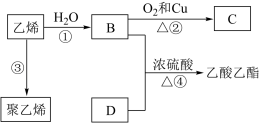
(1)A为乙烯的同系物,相对分子质量比乙烯大14,根据乙烯的性质推测A的性质,下列说法错误 的是_______。
(2)D的结构简式为:_______ 。
(3)写出反应①的反应类型:_______ 。
(4)写出反应②的化学方程式:_______ 。
(5)实验室通过下图装置制备乙酸乙酯,浓硫酸的作用是_______ ,试管b中溶液是_______ ,请指出该装置的一处明显错误_______ 。
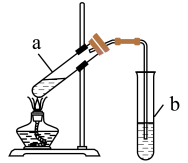
(6)E是乙酸乙酯的同分异构体,且E能与 溶液反应,则E的结构简式可能为(写出1种):
溶液反应,则E的结构简式可能为(写出1种):_______ 。

(1)A为乙烯的同系物,相对分子质量比乙烯大14,根据乙烯的性质推测A的性质,下列说法
A.A与 在一定条件下能发生取代反应 在一定条件下能发生取代反应 |
B.A与溴水反应产物为 |
C.A发生加成聚合产物为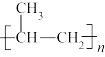 |
| D.A不能使酸性高锰酸钾溶液褪色 |
(2)D的结构简式为:
(3)写出反应①的反应类型:
(4)写出反应②的化学方程式:
(5)实验室通过下图装置制备乙酸乙酯,浓硫酸的作用是

(6)E是乙酸乙酯的同分异构体,且E能与
 溶液反应,则E的结构简式可能为(写出1种):
溶液反应,则E的结构简式可能为(写出1种):
您最近一年使用:0次
名校
5 . 实验室可利用甲醇、空气和铜制备甲醛。甲醇和甲醛的沸点和水溶性见下表:
下图是两个学生设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如(甲)和(乙)所示,试回答:
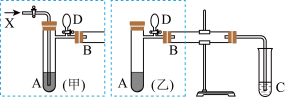
(1)若按(甲)装置进行实验,则通入A管的X是_______ ,B中反应的化学方程式为_______ 。
(2)若按(乙)装置进行实验,则B管中应装_______ 。
(3)C中应装的试剂是_______ ,乙在实验完成时,先打开D处气球的铁夹,再撤去酒精灯,打开铁夹的目的是_______ 。
(4)你认为用甲和乙哪套装置较好,并描述其理由_______ 。
(5)现有两种烯烃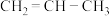 和
和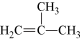 ,它们的混合物在一定条件下发生加聚反应,其产物中可能有
,它们的混合物在一定条件下发生加聚反应,其产物中可能有
①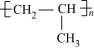 ②
②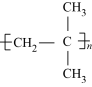 ③
③
④ ⑤
⑤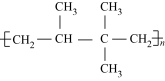 ⑥
⑥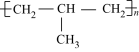
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 混溶 |
| 甲醛 | -21 | 混溶 |

(1)若按(甲)装置进行实验,则通入A管的X是
(2)若按(乙)装置进行实验,则B管中应装
(3)C中应装的试剂是
(4)你认为用甲和乙哪套装置较好,并描述其理由
(5)现有两种烯烃
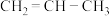 和
和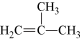 ,它们的混合物在一定条件下发生加聚反应,其产物中可能有
,它们的混合物在一定条件下发生加聚反应,其产物中可能有①
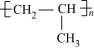 ②
②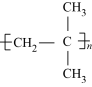 ③
③
④
 ⑤
⑤ ⑥
⑥
| A.全部 | B.只有①②③⑤ | C.只有①②③④ | D.只有③⑤⑥ |
您最近一年使用:0次
名校
解题方法
6 . 如图是异辛烷的球棍模型:

(1)异辛烷与乙烷的关系是_______ 。
(2)写出异辛烷完全燃烧的化学方程式_______ (异辛烷用分子式表示)。1mol异辛烷和1mol正庚烷分别完全燃烧生成水和二氧化碳,消耗氧气的物质的量之差_______ mol。
(3)异辛烷的同分异构体有很多,其中一种同分异构体X的分子结构中含有6个甲基,则X的结构简式为_______ 。
(4)将11.2L(标准状况)乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,原气体混合物中乙烯与乙烷的物质的量之比为_______ 。
(5)实验室制备溴苯的装置如图所示。下列关于实验操作或叙述错误的是_______。


(1)异辛烷与乙烷的关系是
(2)写出异辛烷完全燃烧的化学方程式
(3)异辛烷的同分异构体有很多,其中一种同分异构体X的分子结构中含有6个甲基,则X的结构简式为
(4)将11.2L(标准状况)乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,原气体混合物中乙烯与乙烷的物质的量之比为
(5)实验室制备溴苯的装置如图所示。下列关于实验操作或叙述错误的是_______。

A. 作催化剂,可用铁屑代替 作催化剂,可用铁屑代替 |
| B.装置b的作用是吸收挥发的苯 |
| C.装置c中石蕊溶液变为红色,可证明苯与溴发生取代反应 |
| D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯 |
您最近一年使用:0次
2022-05-06更新
|
125次组卷
|
2卷引用:山东省滕州市2021-2022学年高二下学期期中考试化学试题
名校
解题方法
7 . 实验室用如图所示装置制备乙炔,并验证乙炔的某些化学性质及乙炔相关性质。请回答下列问题:
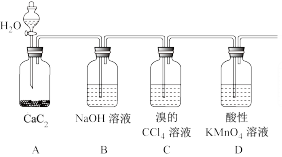
(1)实验室制备乙炔的化学方程式为____ ;为了使产生乙炔的气流平稳,装置A的分液漏斗中常用____ 代替水。
(2)装置B中NaOH溶液的作用是____ ,发生反应的离子方程式为____ 。
(3)①装置C中生成物的名称为_____ 。
②装置D中的反应的类型为____ 。
(4)由乙炔可制备聚乙炔,聚乙炔的结构简式为____ 。乙炔还能低聚成苯,写出苯与液溴反应的化学方程式____ 。
(5)已知: ,如果要合成
,如果要合成 ,所用的原料可以是
,所用的原料可以是____ 。

(1)实验室制备乙炔的化学方程式为
(2)装置B中NaOH溶液的作用是
(3)①装置C中生成物的名称为
②装置D中的反应的类型为
(4)由乙炔可制备聚乙炔,聚乙炔的结构简式为
(5)已知:
 ,如果要合成
,如果要合成 ,所用的原料可以是
,所用的原料可以是| A.1,3—戊二烯和2—丁块 | B.2—甲基—1,3—丁二烯和2—丁炔 |
| C.2,3—二甲基—1,3—戊二烯和乙炔 | D.2,3—二甲基—1,3—丁二烯和1—丙炔 |
您最近一年使用:0次
8 . 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知:
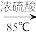
 +H2O
+H2O

(1)制备
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。A中碎瓷片的作用是___________ ,导管B除了导气外还具有的作用是___________ 。
(2)提纯
环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在___________ 层(填“上”或“下”),分液后用___________ (填编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
(3)再将环己烯按如图装置蒸馏,冷却水从g口进入。蒸馏时要加入生石灰,目的是___________ 。

(4)以下区分环己烯精品和粗品的方法,合理的是___________ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
已知:

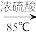
 +H2O
+H2O| 密度(g·cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |

(1)制备
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。A中碎瓷片的作用是
(2)提纯
环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
(3)再将环己烯按如图装置蒸馏,冷却水从g口进入。蒸馏时要加入生石灰,目的是

(4)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
您最近一年使用:0次
名校
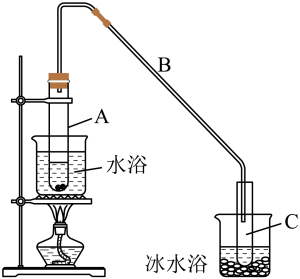
9 . 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知: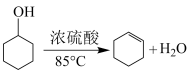
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是___________ ,导管B除了导气外还具有的作用是___________ 。
②试管C置于冰水浴中的目的是_____________ 。
(2)制备精品
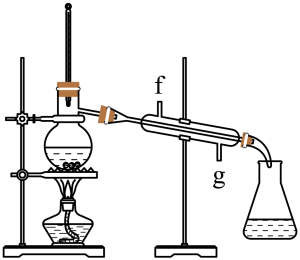
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________ 层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图装置蒸馏,蒸馏时要加入生石灰,目的是__________________ 。
③收集产品时,控制的温度应在_________ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是( )
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点

已知:

| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环乙醇 | 0.96 | 25 | 161 | 能溶于水 |
环乙烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是
②试管C置于冰水浴中的目的是
(2)制备精品

①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图装置蒸馏,蒸馏时要加入生石灰,目的是
③收集产品时,控制的温度应在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
您最近一年使用:0次
2019-03-06更新
|
803次组卷
|
2卷引用:【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二下学期第一次月考(开学)化学试题
名校
解题方法
10 . 1,2-二溴乙烷常用作杀虫剂,某同学用如图装置制备 1,2-二溴乙烷。

实验步骤:按图示连接装置,先将 C 与 D 连接处断开,再对装置 A 中粗砂加热,待温度升到 150 ℃左 右时,连接 C 与 D,并迅速将 A 内反应温度升温至 160~180 ℃,从滴液漏斗中慢慢滴加乙醇和浓硫酸混合液,装置 D 试管中装有 6.0 mL 10 mol/L Br2的 CCl4 溶液,待 Br2的 CCl4 溶液褪色后,经洗涤、干 燥、蒸馏得到 1,2-二溴乙烷 7.896 g。
已知:①CH3CH2OH 在浓硫酸作催化剂条件下迅速加热到 170 ℃会生成乙烯和水
②浓硫酸具有强氧化性,在加热时可能有一部分与乙醇发生氧化还原反应。 完成下列填空:
(1)仪器 F 的名称_____ 。
(2)反应前装置 A 中加入少量粗砂目的是_____ 。
(3)装置 B 的作用是_____ 。
(4)反应一段时间后 C 溶液碱性_____ 。(填“增强”、“减弱”或“不变”)
(5)先将 C 与 D 连接处断开的原因是_________ 。写出 D 装置中生成 1,2-二溴乙烷的化学方程式_____ 。
(6)根据上述实验计算 1,2-二溴乙烷的产率为_________ 。
(7)下列操作中,不会导致产物产率降低的是_________ 。
A.装置 D 中试管内物质换成液溴 B.装置 E 中的 NaOH 溶液用水代替 C.去掉装置 D 烧杯中的冷水 D.去掉装置 C

实验步骤:按图示连接装置,先将 C 与 D 连接处断开,再对装置 A 中粗砂加热,待温度升到 150 ℃左 右时,连接 C 与 D,并迅速将 A 内反应温度升温至 160~180 ℃,从滴液漏斗中慢慢滴加乙醇和浓硫酸混合液,装置 D 试管中装有 6.0 mL 10 mol/L Br2的 CCl4 溶液,待 Br2的 CCl4 溶液褪色后,经洗涤、干 燥、蒸馏得到 1,2-二溴乙烷 7.896 g。
已知:①CH3CH2OH 在浓硫酸作催化剂条件下迅速加热到 170 ℃会生成乙烯和水
②浓硫酸具有强氧化性,在加热时可能有一部分与乙醇发生氧化还原反应。 完成下列填空:
(1)仪器 F 的名称
(2)反应前装置 A 中加入少量粗砂目的是
(3)装置 B 的作用是
(4)反应一段时间后 C 溶液碱性
(5)先将 C 与 D 连接处断开的原因是
(6)根据上述实验计算 1,2-二溴乙烷的产率为
(7)下列操作中,不会导致产物产率降低的是
A.装置 D 中试管内物质换成液溴 B.装置 E 中的 NaOH 溶液用水代替 C.去掉装置 D 烧杯中的冷水 D.去掉装置 C
您最近一年使用:0次



