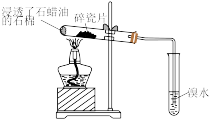
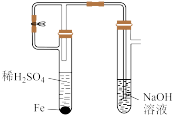
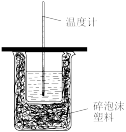
1 . 在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
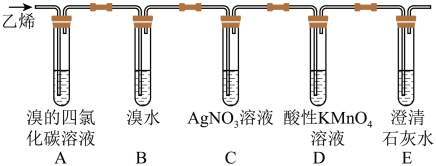
根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是_______ ,B装置中的现象是_______ 。
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为_______ 。
(3)工业上利用乙烯水化制备乙醇,其对应的化学方程式为_______ ;反应类型为_______ 。
(4)丙烯( )与乙烯具有相似的化学性质。
)与乙烯具有相似的化学性质。
①丙烯与溴的加成反应产物为_______ 。
②在一定条件下丙烯与 的加成产物可能
的加成产物可能_______ 。

根据上述装置,回答下列问题:
(1)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是
(2)D装置中溶液由紫色变无色,D装置中发生反应的类型为
(3)工业上利用乙烯水化制备乙醇,其对应的化学方程式为
(4)丙烯(
 )与乙烯具有相似的化学性质。
)与乙烯具有相似的化学性质。①丙烯与溴的加成反应产物为
②在一定条件下丙烯与
 的加成产物可能
的加成产物可能
您最近一年使用:0次
解题方法
2 . 用下列装置和药品进行相应实验,能达到实验目的是
验证 易溶于水且溶液呈碱性 易溶于水且溶液呈碱性 | 证明石蜡油中含有不饱和烃 |
|
|
| A | B |
制备 | 测定中和反应的反应热 |
|
|
| C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 环己基氯为无色液体,不溶于水,常用于合成橡胶防焦剂、杀虫剂三环锡、抗癫痫剂等。请回答下列问题:
Ⅰ.有两种方法可制备环己基氯:
①环己烷氯化法:
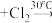
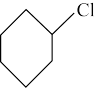
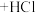 ;
;
②环己烯氯化氢加成法:
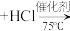
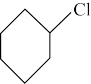 。
。
(1)工业生产多采用方法②制备环己基氯,原因是_______ 。
Ⅱ.某化学兴趣小组用如图所示装置模拟I中方法②制备环己基氯:
步骤如下:在仪器c中加入35mL(0.35mol)环己烯、3g催化剂,搅拌升温。打开仪器a的活塞,向c中加入105mL30%(约1mol)的盐酸,调节反应温度为75℃,搅拌1.5h,待反应结束,冷却,将反应液转移至分液漏斗中,静置分层。弃去水层,分别使用饱和氯化钠溶液和碳酸钠溶液洗涤有机层2次。用无水氯化钙干燥,蒸馏得产品30.81g。
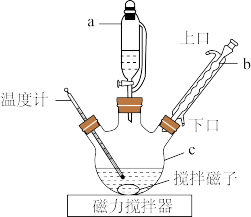
(2)仪器c的名称是_______ ,仪器b的进水口是_______ (填“上口”或“下口”)。
(3)仪器a中支管的作用是_______ 。
(4)使用碳酸钠溶液洗涤的目的是_______ 。
(5)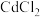 和
和 都可以作该反应的催化剂,但在工业生产中常用
都可以作该反应的催化剂,但在工业生产中常用 ,其原因是
,其原因是_______ (从安全环保角度考虑)。
(6)该实验中环己基氯的产率为_______ (保留三位有效数字)。
Ⅰ.有两种方法可制备环己基氯:
①环己烷氯化法:

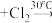

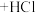 ;
;②环己烯氯化氢加成法:

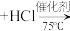
 。
。(1)工业生产多采用方法②制备环己基氯,原因是
Ⅱ.某化学兴趣小组用如图所示装置模拟I中方法②制备环己基氯:
步骤如下:在仪器c中加入35mL(0.35mol)环己烯、3g催化剂,搅拌升温。打开仪器a的活塞,向c中加入105mL30%(约1mol)的盐酸,调节反应温度为75℃,搅拌1.5h,待反应结束,冷却,将反应液转移至分液漏斗中,静置分层。弃去水层,分别使用饱和氯化钠溶液和碳酸钠溶液洗涤有机层2次。用无水氯化钙干燥,蒸馏得产品30.81g。

(2)仪器c的名称是
(3)仪器a中支管的作用是
(4)使用碳酸钠溶液洗涤的目的是
(5)
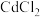 和
和 都可以作该反应的催化剂,但在工业生产中常用
都可以作该反应的催化剂,但在工业生产中常用 ,其原因是
,其原因是(6)该实验中环己基氯的产率为
您最近一年使用:0次
2023-01-18更新
|
498次组卷
|
4卷引用:河北省邯郸市第四中学2022-2023学年高二上学期12月联考 化学试题
河北省邯郸市第四中学2022-2023学年高二上学期12月联考 化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(实验探究题)山东省济南市莱芜第一中学2022-2023学年高二下学期第二次阶段性检测化学试题广东省广州市第十六中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
4 . 氯代环己烷为无色液体,具有窒息性气味,不溶于水,溶于乙醇,可生产农药、橡胶b防焦剂、医药等。请回答下列问题:
Ⅰ.制备氯代环已烷有两种方法:________ 。
(2) 是环已烯的同分异构体,其名称为
是环已烯的同分异构体,其名称为________ 。
Ⅱ.现用如图所示装置模拟方法②制备氯代环已烷,具体操作步骤如下:在250mL三口烧瓶中加入35mL(0.35mol)环已烯,3g催化剂,搅拌升温,打开仪器a的活塞向三口烧瓶中加入100mL30%(约0.95mol)的盐酸,调节反应温度为75℃,搅拌反应1.5小时,待反应结束,冷却静置。分别使用饱和氯化钠溶液和碳酸钠溶液洗涤有机层3次,再向有机层中加入适量无水硫酸镁后蒸馏,得产品31g。________ 。
(4)该实验中合适的加热方式是________ 。
(5)使用碳酸钠溶液洗涤有机层的目的是:________ 。
(6)加入适量无水硫酸镁的目的是:________ 。
(7)该实验氯代环已烷的产率为________ 。(结果保留三位有效数字)
Ⅰ.制备氯代环已烷有两种方法:
①环己烷氯化法:
②环己烯氯化氢加成法:
(2)
 是环已烯的同分异构体,其名称为
是环已烯的同分异构体,其名称为Ⅱ.现用如图所示装置模拟方法②制备氯代环已烷,具体操作步骤如下:在250mL三口烧瓶中加入35mL(0.35mol)环已烯,3g催化剂,搅拌升温,打开仪器a的活塞向三口烧瓶中加入100mL30%(约0.95mol)的盐酸,调节反应温度为75℃,搅拌反应1.5小时,待反应结束,冷却静置。分别使用饱和氯化钠溶液和碳酸钠溶液洗涤有机层3次,再向有机层中加入适量无水硫酸镁后蒸馏,得产品31g。

(4)该实验中合适的加热方式是
(5)使用碳酸钠溶液洗涤有机层的目的是:
(6)加入适量无水硫酸镁的目的是:
(7)该实验氯代环已烷的产率为
您最近一年使用:0次
7日内更新
|
85次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高二下学期期中联考化学试卷B
5 . 烃是一类重要有机化合物,回答下列有关问题。
(1)甲烷分子的空间构型是_______ 。甲烷与氯气光照下反应生成产物共 ____ 种。
(2)甲烷和氯气在光照条件下发生取代反应的装置如图所示。______ 。
(3)下列各烷烃的沸点由低到高的顺序为_____(用序号表示)。
(4) 某烷烃完全燃烧时消耗氧气的物质的量为
某烷烃完全燃烧时消耗氧气的物质的量为 ,其化学式为
,其化学式为________ ,若其结构中含有 个
个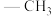 ,其结构简式为
,其结构简式为_______ 。
(5)聚乙烯可用于制造食品包装袋,由乙烯制备聚乙烯的化学方程式为_______ 。写出丙烯CH3CH=CH2发生加聚反应的化学方程式:______ 。
(1)甲烷分子的空间构型是
(2)甲烷和氯气在光照条件下发生取代反应的装置如图所示。
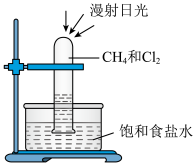
(3)下列各烷烃的沸点由低到高的顺序为_____(用序号表示)。
| A.异丁烷 | B.异戊烷 | C.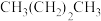 | D. |
 某烷烃完全燃烧时消耗氧气的物质的量为
某烷烃完全燃烧时消耗氧气的物质的量为 ,其化学式为
,其化学式为 个
个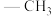 ,其结构简式为
,其结构简式为(5)聚乙烯可用于制造食品包装袋,由乙烯制备聚乙烯的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装置图,图中分液漏斗和烧瓶a中分别装有浓 和无水乙醇,d装置试管中装有液溴。
和无水乙醇,d装置试管中装有液溴。

相关数据列表如表:
(1)装置a中发生主要反应的方程式为:_______ 。为防止副反应发生,实验中的具体操作为:_______ 。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装置中导管是否发生堵塞,如果实验时d装置中导管堵塞,你认为可能的原因:_______ ;安全瓶b还可以起到的作用是:_______ 。
(3)容器c、e中都盛有 溶液,c中
溶液,c中 溶液的作用是
溶液的作用是_______ 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比理论值超过许多,如果装置的气密性没有问题,试分析可能的原因:_______ 、_______ (写出两条即可)。
(5)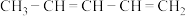 与溴发生加成反应,可以得到
与溴发生加成反应,可以得到_______ 种有机产物。
(6)用系统法命名:
_______
 和无水乙醇,d装置试管中装有液溴。
和无水乙醇,d装置试管中装有液溴。
相关数据列表如表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/ | 0.79 | 2.18 | 0.71 | 3.10 |
| 沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
| 熔点/℃ | 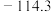 | 9.79 | 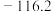 | 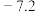 |
| 水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)装置a中发生主要反应的方程式为:
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装置中导管是否发生堵塞,如果实验时d装置中导管堵塞,你认为可能的原因:
(3)容器c、e中都盛有
 溶液,c中
溶液,c中 溶液的作用是
溶液的作用是(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比理论值超过许多,如果装置的气密性没有问题,试分析可能的原因:
(5)
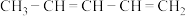 与溴发生加成反应,可以得到
与溴发生加成反应,可以得到(6)用系统法命名:

您最近一年使用:0次
7 . 在实验室利用下列装置,可制备某些气体并验证其化学性质。
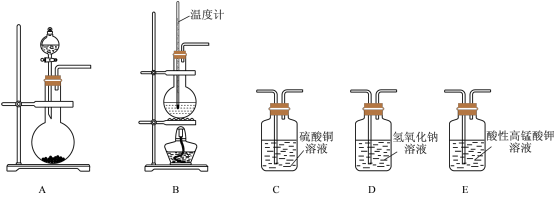
(1)填空,完成下列表格:
(2)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):反应4的化学方程式是___________ 。
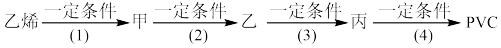
(3)下列说法正确的是___________。
(4)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42.以A为原料,利用下述反应合成甘油 (丙三醇),在方框内填上中间体的结构简式。___________ 、___________ 。
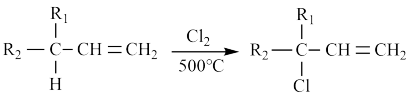


(1)填空,完成下列表格:
| 序号 | 气体 | 装置连接顺(填字母) | 制备反应的化学方程式 |
| ① | 乙烯 | B→D→E | |
| ② | 乙炔 |  |
(2)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):反应4的化学方程式是
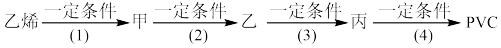
(3)下列说法正确的是___________。
| A.乙烯可以作为植物生长调节剂 | B.PVC不能使酸性高锰酸钾溶液褪色 |
| C.PVC中的官能团是碳碳双键和氯原子 | D.PVC可用作食品包装袋 |
(4)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42.以A为原料,利用下述反应合成甘油 (丙三醇),在方框内填上中间体的结构简式。
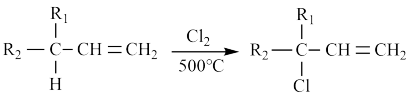

您最近一年使用:0次
8 . 有机物是生命产生的物质基础,其种类繁多。经研究发现白蚁信息素有:A.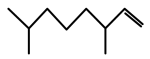 ;B
;B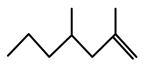 ;家蚕的信息素为:
;家蚕的信息素为: 。回答下列问题:
。回答下列问题:
(1)下列说法正确的是___________(填字母)。
(2)用系统命名法命名:信息素A的名称为___________ ;信息素B与氢气加成产物的名称为___________ 。
(3)下列区分苯和信息素A的实验方法和判断都正确的是___________。
(4)烯烃C是信息素A的一种同分异构体,C与氢气加成得到烷烃D,D的一氯代物只有2种,则C的结构简式为___________ ;烯烃E是信息素B的一种同分异构体,E与足量氢气加成得到烷烃F,F的一氯代物也只有2种,F的结构简式为___________ 。
(5)天然橡胶为顺式聚异戊二烯,杜仲胶为反式聚异戊二烯,则反式聚异戊二烯的结构简式为___________ 。其能发生的反应有___________ (填字母)。
A.加成反应 B.氧化反应 C.消去反应
2-氯乙醇是 一种重要的有机化工原料,乙烯制备2-氯乙醇的装置如图所示。
一种重要的有机化工原料,乙烯制备2-氯乙醇的装置如图所示。
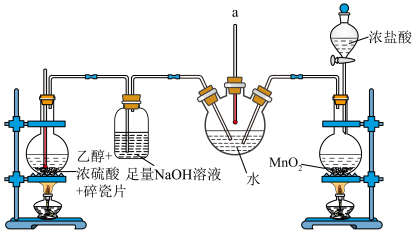
请回答下列问题:
(6)装置A中碎瓷片的作用是___________ 。装置B中 溶液的作用是
溶液的作用是___________ 。
(7)装置C中发生的有机反应的化学方程式为___________ 。
 ;B
;B ;家蚕的信息素为:
;家蚕的信息素为: 。回答下列问题:
。回答下列问题:(1)下列说法正确的是___________(填字母)。
| A.信息素A、B互为同分异构体 |
| B.以上三种信息素均能发生加聚反应 |
| C.信息素A、B互为同系物 |
D. 家蚕信息素与 家蚕信息素与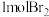 的加成产物只有一种 的加成产物只有一种 |
(2)用系统命名法命名:信息素A的名称为
(3)下列区分苯和信息素A的实验方法和判断都正确的是___________。
| A.分别点燃,无黑烟生成的是苯 |
| B.分别加入溴水,振荡,静置后分层,上层为红棕色,下层无色的是信息素A |
| C.分别加入溴水,振荡,静置后分层,上、下两层橙红色均消失的是信息素A |
D.分别加入酸性 溶液,振荡,静置后分层且水层紫红色消失的是苯 溶液,振荡,静置后分层且水层紫红色消失的是苯 |
(4)烯烃C是信息素A的一种同分异构体,C与氢气加成得到烷烃D,D的一氯代物只有2种,则C的结构简式为
(5)天然橡胶为顺式聚异戊二烯,杜仲胶为反式聚异戊二烯,则反式聚异戊二烯的结构简式为
A.加成反应 B.氧化反应 C.消去反应
2-氯乙醇是
 一种重要的有机化工原料,乙烯制备2-氯乙醇的装置如图所示。
一种重要的有机化工原料,乙烯制备2-氯乙醇的装置如图所示。
请回答下列问题:
(6)装置A中碎瓷片的作用是
 溶液的作用是
溶液的作用是(7)装置C中发生的有机反应的化学方程式为
您最近一年使用:0次
名校
9 . 。部分实验中涉及到的物质的熔沸点如表所示。
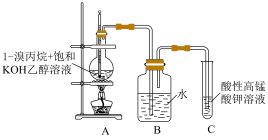
完成下列填空:
(1)写出1-溴丙烷制备丙烯的化学方程式___________ 。
(2)A装置中的导气管较长,可以起到使反应物________ 的作用。若导管的长度太长,C中酸性高锰酸钾溶液褪色时间会延后,可能的原因是________ 。B装置是洗气装置,可以除去从A中导出气体中的杂质_________ 、_______ 。
(3)该实验小组查阅了相关资料后发现,1-溴丙烷制备丙烯的反应需要在65℃以上才能发生。为了更好地达到控温的效果,可以采取_____ 的方式进行加热,这种加热方式除了方便控温外这还具有______ 的优势。加热时将温度控制在65-70℃之间,请结合表中数据阐释选择该温度范围的原因___________ 。
(4)溶液的碱性越强,该反应越容易发生。NaOH与KOH都是常见的水溶液中的强碱,但是经实验测定NaOH在乙醇中的碱性弱于KOH在乙醇中的碱性,这是因为根据元素周期律,Na的______ (选填“金属性”或“非金属性”)______ (选填“强于”或“弱于”)K。结合题目及题干信息,阐释实验采用饱和的KOH乙醇溶液而不采用饱和的NaOH乙醇溶液的原因___________ 。
(5)可以采用溴的四氯化碳溶液吸收生成的丙烯,写出溴的四氯化碳溶液与丙烯反应的化学方程式_______ 。若反应前量取了9.1mL的1-溴丙烷,充分反应后溴的四氯化碳溶液质量增加了0.336g,则丙烯的产率为______ ,请提出一个产率偏低的可能原因___________ 。
| 熔点(℃) | 沸点(℃) | 密度(g·ml-1) | |
| 1-溴丙烷 | -110 | 71 | 1.354 |
| 乙醇 | -114 | 78 | 0.79 |
| 丙烯 | -185 | -47 | |
| NaBr | 755 | 1390 | |
| 饱和KOH乙醇溶液 | 116 | ||
| 饱和NaOH乙醇溶液 | 85 |

完成下列填空:
(1)写出1-溴丙烷制备丙烯的化学方程式
(2)A装置中的导气管较长,可以起到使反应物
(3)该实验小组查阅了相关资料后发现,1-溴丙烷制备丙烯的反应需要在65℃以上才能发生。为了更好地达到控温的效果,可以采取
(4)溶液的碱性越强,该反应越容易发生。NaOH与KOH都是常见的水溶液中的强碱,但是经实验测定NaOH在乙醇中的碱性弱于KOH在乙醇中的碱性,这是因为根据元素周期律,Na的
(5)可以采用溴的四氯化碳溶液吸收生成的丙烯,写出溴的四氯化碳溶液与丙烯反应的化学方程式
您最近一年使用:0次
10 . 在炽热条件下,将石蜡油分解产生的乙烯持续地通入下列各试管里,装置如图所示。

根据上述装置,回答下列问题:
(1)C装置的作用是________________________________ 。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是_____________________ ,B装置中的现象是_____________________ 。分离A装置中产物的操作名称是____________ ,分离B装置中产物需要的玻璃仪器名称是烧杯、________ 。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为_________________ 。用溴的四氯化碳溶液替代溴水与乙烯反应更好,其原因是_______________________________ 。
(4)写出A装置中发生反应的化学方程式______________________________ ,反应类型为_________ 。E装置的作用是______________________ ,当观察到___________________ 现象时能验证E装置功能。
(5)做乙烯燃烧实验之前必须进行的操作是_______________________________ ,可能观察到的现象是_______________________________ 。
(6)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质。丙烯与溴的加成反应产物为_______________________________ (用结构简式回答,下同)。

根据上述装置,回答下列问题:
(1)C装置的作用是
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:A装置中的现象是
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为
(4)写出A装置中发生反应的化学方程式
(5)做乙烯燃烧实验之前必须进行的操作是
(6)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质。丙烯与溴的加成反应产物为
您最近一年使用:0次