解题方法
1 . 实验室用乙醇与浓硫酸共热制乙烯,常因温度过高使溶液中有黑色物质出现,使制得的乙烯气体中含有少量CO2、SO2,某兴趣小组用以下仪器组装(仪器可以重复使用,也可以不选用),进行实验,探究制得的气体中含有乙烯和少量SO2。_______ ;
(2)图中仪器a的名称是_______ ,装置A中碎瓷片的作用是_______ ,装置B的作用是_______ ;
(3)写出乙醇与浓硫酸共热制乙烯的反应方程式_______ ;
(4)以乙烯为原料生产环氧乙烷通常有2种方法。
①以乙烯为原料生产环氧乙烷的方法是:
Ⅰ:氯代乙醇法
CH2=CH2+Cl2+H2O→ClCH2CH2OH+HCl_______ 。方法Ⅱ与方法Ⅰ比较,优点是_______ (写一条)。
②已知环氧丙烷与二氧化碳在催化剂作用下发生加聚反应生成全降解塑料——聚碳酸丙烯酯(PPC)的结构简式如图所示,写出反应方程式_______ 。
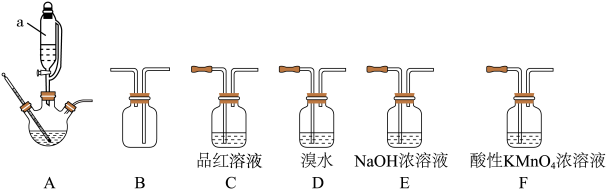
(2)图中仪器a的名称是
(3)写出乙醇与浓硫酸共热制乙烯的反应方程式
(4)以乙烯为原料生产环氧乙烷通常有2种方法。
①以乙烯为原料生产环氧乙烷的方法是:
Ⅰ:氯代乙醇法
CH2=CH2+Cl2+H2O→ClCH2CH2OH+HCl
ClCH2CH2OH+Ca(OH)2→CaCl2+H2O+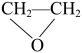
②已知环氧丙烷与二氧化碳在催化剂作用下发生加聚反应生成全降解塑料——聚碳酸丙烯酯(PPC)的结构简式如图所示,写出反应方程式
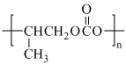
您最近一年使用:0次
2 . 为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(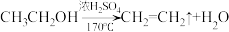 ),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:
),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:
(1)甲同学设计的实验___  填“能”或“不能”
填“能”或“不能” 验证乙烯与溴水发生了加成反应,其理由是
验证乙烯与溴水发生了加成反应,其理由是____  填字母
填字母 。
。
A.使溴水褪色的反应,未必是加成反应 B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯 D.使溴水褪色的物质,就是乙烯
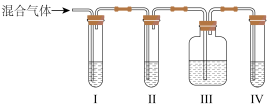
(2)乙同学推测此乙烯中必定含有一种杂质气体是_______ ,它与溴水反应的化学方程式是_______ ,在验证过程中必须全部除去。为此乙同学设计了如图所示的实验装置:_______ Ⅱ_______ Ⅲ_______ Ⅳ_______  选填序号
选填序号 。
。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液。
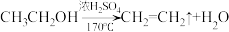 ),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:
),生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。请回答下列问题:(1)甲同学设计的实验
 填“能”或“不能”
填“能”或“不能” 验证乙烯与溴水发生了加成反应,其理由是
验证乙烯与溴水发生了加成反应,其理由是 填字母
填字母 。
。A.使溴水褪色的反应,未必是加成反应 B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯 D.使溴水褪色的物质,就是乙烯
(2)乙同学推测此乙烯中必定含有一种杂质气体是
 选填序号
选填序号 。
。A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液。
您最近一年使用:0次
解题方法
3 . 苯乙醛是一种具有优雅香气的香料,是调和多种花香香精的重要香料之一,也是合成药物、食品添加剂等精细化学品的重要原料。某同学在实验室设计如图装置模拟工业制备苯乙醛。

催化剂实验原理: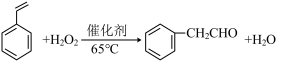
相关数据如表:
实验步骤:
Ⅰ.将一定量的催化剂(白色固体)、10.4 g苯乙烯、69.6 g丙酮加入250 mL的仪器A中,将17 g 30%的双氧水置于滴液漏斗中,开启磁力搅拌器(600转每分钟),加热至65℃,滴加双氧水。
Ⅱ.反应完成后,将反应液过滤,将滤液置于分液漏斗中,加入等量的水,充分振荡后静置分层,弃去水层。有机层先用适量氢氧化钠溶液洗涤,分液后再用少量水洗。
Ⅲ.将Ⅱ中所得有机层倒入干燥的小锥形瓶中,加入1~2 g无水CaCl2进行干燥。
Ⅳ.将干燥后的产物滤入蒸馏瓶中,加入几粒沸石,蒸馏。称重得产品9.9 g。
回答下列问题:
(1)仪器A的名称为___________ ,冷凝管中的水应从___________ (填“上”或“下”)口进入。
(2)滴液漏斗上支管的作用是___________ 。
(3)控制反应温度为65℃,最好用水浴加热,水浴加热的优点是___________ 。若温度过高,则会导致苯乙醛的产率降低,其原因可能为___________ 。
(4)加入适量氢氧化钠溶液的目的为___________ 。
(5)蒸馏时收集产物应控制温度为___________ ℃。
(6)实验测定最佳苯乙烯和H2O2的物质的量之比为1∶1.5,H2O2的用量过少或过多都会影响苯乙醛的产率,试分析其原因:___________ 。
(7)本实验中苯乙醛的产率为___________ %。

催化剂实验原理:

相关数据如表:
| 药品名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g·mL-1) | 溶解度 |
| 苯乙醛 | 120 | -10 | 194 | 1.08 | 难溶于水,溶于有机溶剂 |
| 苯乙烯 | 104 | -30.6 | 146 | 0.91 | 不溶于水,溶于有机溶剂 |
| 苯乙酸 | 136 | 76.5 | 265.5 | 1.09 | 微溶于冷水,易溶于热水 |
| 丙酮 | -95 | 56.5 | 与水互溶 |
Ⅰ.将一定量的催化剂(白色固体)、10.4 g苯乙烯、69.6 g丙酮加入250 mL的仪器A中,将17 g 30%的双氧水置于滴液漏斗中,开启磁力搅拌器(600转每分钟),加热至65℃,滴加双氧水。
Ⅱ.反应完成后,将反应液过滤,将滤液置于分液漏斗中,加入等量的水,充分振荡后静置分层,弃去水层。有机层先用适量氢氧化钠溶液洗涤,分液后再用少量水洗。
Ⅲ.将Ⅱ中所得有机层倒入干燥的小锥形瓶中,加入1~2 g无水CaCl2进行干燥。
Ⅳ.将干燥后的产物滤入蒸馏瓶中,加入几粒沸石,蒸馏。称重得产品9.9 g。
回答下列问题:
(1)仪器A的名称为
(2)滴液漏斗上支管的作用是
(3)控制反应温度为65℃,最好用水浴加热,水浴加热的优点是
(4)加入适量氢氧化钠溶液的目的为
(5)蒸馏时收集产物应控制温度为
(6)实验测定最佳苯乙烯和H2O2的物质的量之比为1∶1.5,H2O2的用量过少或过多都会影响苯乙醛的产率,试分析其原因:
(7)本实验中苯乙醛的产率为
您最近一年使用:0次
名校
4 . 在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。

根据上述装置,回答下列问题:
已知:1,2—二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:
(1)B装置中的现象是_____ 。D装置中溶液由紫色变无色,D装置中发生反应的类型为_____ 。
(2)写出A装置中发生反应的化学方程式_____ ,反应类型为_____ ,E装置的作用是_____ 。
(3)下列化合物中,能发生原子利用率100%反应的是_____。
(4)丙烯与乙烯( )具有相似的化学性质(写结构简式)
)具有相似的化学性质(写结构简式)
①丙烯与 的加成产物为
的加成产物为_____ 。(写一个)
②丙烯的加聚反应方程式为_____ 。

根据上述装置,回答下列问题:
已知:1,2—二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。
预测:
(1)B装置中的现象是
(2)写出A装置中发生反应的化学方程式
(3)下列化合物中,能发生原子利用率100%反应的是_____。
| A.甲烷 | B.氯乙烯 | C.丙烷 | D.聚乙烯 |
 )具有相似的化学性质(写结构简式)
)具有相似的化学性质(写结构简式)①丙烯与
 的加成产物为
的加成产物为②丙烯的加聚反应方程式为
您最近一年使用:0次
5 . Ⅰ.有人设计了如图所示实验,以确认某混合气体中含有 和
和 。
。

实验中提供的试剂有:A.品红溶液 B. 溶液 C.浓硫酸 D.酸性
溶液 C.浓硫酸 D.酸性 溶液。
溶液。
试回答下列问题:
(1)写出图中①②③④装置盛放试剂的顺序为(将上述有关试剂的序号填入空格内,试剂可重复使用)___________ 。
(2)能确定混合气体中存在乙烯的现象是___________ 。
(3)乙烯与溴水反应的化学方程式为___________ ,该反应的反应类型为___________ 。
(4)关于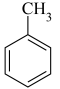 分子有下列问题:
分子有下列问题:
①分子中同一平面的原子最多有___________ 个。
②若用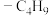 取代
取代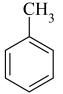 上的一个H原子,得到的有机物的同分异构体共有
上的一个H原子,得到的有机物的同分异构体共有___________ 种。
 和
和 。
。
实验中提供的试剂有:A.品红溶液 B.
 溶液 C.浓硫酸 D.酸性
溶液 C.浓硫酸 D.酸性 溶液。
溶液。试回答下列问题:
(1)写出图中①②③④装置盛放试剂的顺序为(将上述有关试剂的序号填入空格内,试剂可重复使用)
(2)能确定混合气体中存在乙烯的现象是
(3)乙烯与溴水反应的化学方程式为
(4)关于
 分子有下列问题:
分子有下列问题:①分子中同一平面的原子最多有
②若用
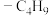 取代
取代 上的一个H原子,得到的有机物的同分异构体共有
上的一个H原子,得到的有机物的同分异构体共有
您最近一年使用:0次
名校
解题方法
6 . 乙烯是一种重要的化工原料,工业上可用石蜡油制得,某实验小组用下列装置模拟该工业过程制备乙烯,并探究它的化学性质。

(1)加入药品之前的操作为___________ 。
(2)B装置中发生反应的方程式为___________ ,产物的名称是___________ 。
(3)C装置中的现象是___________ ,D中的离子方程式为___________ 。
(4)通过上述实验探究可知,除去甲烷中乙烯的方法是___________。
(5)乙烯相互加成可以制得日常生活使用的高分子塑料PE,写出其反应的化学方程式___________ 。

(1)加入药品之前的操作为
(2)B装置中发生反应的方程式为
(3)C装置中的现象是
(4)通过上述实验探究可知,除去甲烷中乙烯的方法是___________。
| A.将气体通入水中 |
| B.将气体通过装溴水的洗气瓶 |
| C.将气体通过装酸性高锰酸钾溶液的洗气瓶 |
| D.将气体通入氢氧化钠溶液中 |
您最近一年使用:0次
7 . 在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
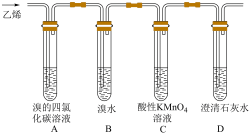
请回答下列问题:
(1)写出乙烯的电子式______ ,C装置中溶液由紫色变为无色,C装置中发生反应的类型为______ 。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:A装置中的现象是______ ,B装置中的现象是______ 。
(3)写出A装置中发生反应的化学方程式______ ,D装置的作用是______ ,当观察到_______ 时能验证D装置功能。
(4)做乙烯燃烧实验之前必须进行的操作是______ ,最后燃烧可能观察到的现象是______ 。
(5)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质。
①写出丙烯发生加聚反应的化学方程式______ 。
②在一定条件下丙烯与H2O(g)的加成产物可能为______ (写结构简式)。

请回答下列问题:
(1)写出乙烯的电子式
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:A装置中的现象是
(3)写出A装置中发生反应的化学方程式
(4)做乙烯燃烧实验之前必须进行的操作是
(5)丙烯(CH2=CHCH3)与乙烯具有相似的化学性质。
①写出丙烯发生加聚反应的化学方程式
②在一定条件下丙烯与H2O(g)的加成产物可能为
您最近一年使用:0次
2023-05-24更新
|
157次组卷
|
2卷引用:江西省抚州市三校2022-2023学年高一下学期第二次月考化学试题
名校
8 . 乙烯是石油化工的基本原料,其产量可以衡量一个国家石油化学工业的发展水平。工业上常用裂解石油分馏产物获得,某同学利用裂解石蜡油(主要成分正二十二烷和正二十八烷)设计实验制取部分烯烃(乙烯、丙烯等),实验装置如图所示。回答下列问题:

(1)写出正二十二烷的分子式:______ 。
(2)下列关于乙烯的说法正确的是______ (填字母)。
(3)装置B中的实验现象为______ ,乙烯与装置B中溶液发生反应的化学方程式为______ 。
(4)装置D中澄清石灰水变浑浊,说明酸性高锰酸钾溶液可以将乙烯氧化为______ (填分子式)。
(5)乙烯的同系物丙烯(CH3-CH=CH2)也是一种生产塑料的重要原料,写出丙烯与水发生加成反应的化学方程式:______ 。

(1)写出正二十二烷的分子式:
(2)下列关于乙烯的说法正确的是
| A.乙烯为不饱和烃 |
| B.乙烯与苯均含有碳碳双键 |
| C.乙烯在空气中燃烧火焰明亮并伴有黑烟 |
| D.除去乙烷中混有的乙烯,可在催化剂加热条件下向混合气中通入过量氢气 |
(4)装置D中澄清石灰水变浑浊,说明酸性高锰酸钾溶液可以将乙烯氧化为
(5)乙烯的同系物丙烯(CH3-CH=CH2)也是一种生产塑料的重要原料,写出丙烯与水发生加成反应的化学方程式:
您最近一年使用:0次
9 . Ⅰ.如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为
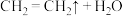 ,回答下列问题:
,回答下列问题:
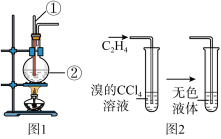
(1)图1中仪器①、②的名称分别为___________ 、___________ 。
(2)收集乙烯气体最好的方法是___________ 。
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应的化学方程式为___________ 。
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:
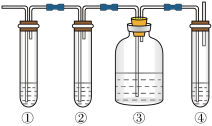
(4)图中①、②、③、④装置盛放的试剂是下列中的___________(将正确选项填入空格内):
①:A;②___________ ;③___________ ;④:D。
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(5)能说明二氧化硫气体存在的现象是___________ 。
(6)使用装置③的目的是___________ 。
(7)确认含有乙烯的现象是___________ 。

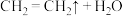 ,回答下列问题:
,回答下列问题:
(1)图1中仪器①、②的名称分别为
(2)收集乙烯气体最好的方法是
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应的化学方程式为
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:

(4)图中①、②、③、④装置盛放的试剂是下列中的___________(将正确选项填入空格内):
①:A;②
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(5)能说明二氧化硫气体存在的现象是
(6)使用装置③的目的是
(7)确认含有乙烯的现象是
您最近一年使用:0次
解题方法
10 . 乙烯的产量是衡量一个国家石油化工发展水平的重要标志。如图所示是某校化学实验兴趣小组在实验室组装的一套制取乙烯并验证乙烯具有还原性的实验装置。请回答下列问题:
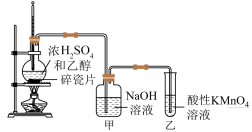
(1)请写出圆底烧瓶中发生反应的化学方程式:_______ ,反应类型是_______ 。该反应中浓硫酸的作用是_______ 。
(2)能够说明乙烯具有还原性的现象是_______ ;装置甲的作用是_______ 。
(3)若无装置甲,是否也能检验乙烯的还原性,请简述你的理由:_______ 。

(1)请写出圆底烧瓶中发生反应的化学方程式:
(2)能够说明乙烯具有还原性的现象是
(3)若无装置甲,是否也能检验乙烯的还原性,请简述你的理由:
您最近一年使用:0次



