2024·黑龙江·模拟预测
解题方法
1 . 下列叙述中,事实与对应解释错误的是
| 事实 | 解释 | |
| A | 酸性:HCOOH > CH3COOH | H3C-是推电子基团,使羧基中羟基的极性减小 |
| B | 在水中的溶解度:乙醇 > 戊醇 | 乙醇分子结构与水具有相似性,而戊醇分子结构与水的相似性较小 |
| C | 硬度:金刚石>石墨 | 金刚石属于共价晶体只含共价键,石墨属于混合型晶体,既存在共价键又存在范德华力 |
| D | 热稳定性:H2O>H2S | 水分子间存在氢键作用 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三·全国·专题练习
2 . 有机物的结构影响了有机物的性质。下列关于性质与结构的说法错误的是
| A.甲苯能使酸性高锰酸钾溶液褪色而乙烷不能,是由于苯环使甲苯中-CH3更活泼 |
| B.苯酚呈酸性而乙醇没有酸性,是由于苯酚中-OH使苯环上的H原子更活泼 |
| C.CCl3COOH的酸性强于乙酸,是由于Cl3C-使羧基更易电离出H+ |
| D.CH3COCH3中碳氧双键上氧的电负性大,与HCN加成时,H原子进攻O生成-OH |
您最近半年使用:0次
名校
3 . 淄博烧烤红遍全国,用嫩肉粉腌制后烤出的肉串鲜香滑嫩,嫩肉粉的有效成分为木瓜蛋白酶,其结构简式如下,下列说法正确的是
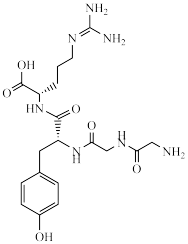
| A.1mol该分子最多消耗5molNaOH | B.该分子中含有4种含氧官能团 |
| C.该分子中碳原子的杂化方式有3种 | D.该分子可以发生消去反应 |
您最近半年使用:0次
昨日更新
|
292次组卷
|
3卷引用:2024届河北省雄安新区雄安部分高中高三下学期一模化学试题
4 . 酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所示:___________ 。
(2)酮基布洛芬官能团的名称为___________ ,D→E的反应类型为___________ 。
(3)写出C的结构简式:___________ ;A~G中含有手性碳原子的物质有___________ 种。
(4)请写出B在NaOH水溶液中加热的化学方程式:___________ 。
(5)H为酮基布洛芬的同分异构体,则符合下列条件的H有___________ 种。
(6)以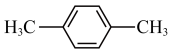 、苯和
、苯和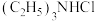 为原料(无机试剂任选),设计制
为原料(无机试剂任选),设计制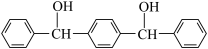 的一种合成路线
的一种合成路线____ 。

(2)酮基布洛芬官能团的名称为
(3)写出C的结构简式:
(4)请写出B在NaOH水溶液中加热的化学方程式:
(5)H为酮基布洛芬的同分异构体,则符合下列条件的H有
①含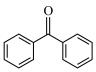 的酯类化合物
的酯类化合物
(6)以
 、苯和
、苯和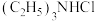 为原料(无机试剂任选),设计制
为原料(无机试剂任选),设计制 的一种合成路线
的一种合成路线
您最近半年使用:0次
5 . 物质的结构决定其性质。下列物质性质差异与其结构因素不相符的是
| 选项 | 性质差异 | 结构因素 |
 | 沸点:邻羟基苯甲醛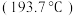 低于对羟基苯甲醛 低于对羟基苯甲醛 | 氢键类型 |
 | 熔点: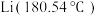 高于 高于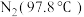 | 价层电子数 |
 | 熔点: 远高于( 远高于( 升华) 升华) | 晶体类型 |
 | 酸性: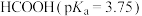 强于乙酸 强于乙酸 | 羟基的极性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
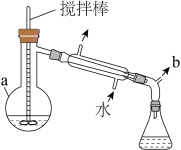
6 . 伊贝沙坦是一种新型的抗高血压药物,环戊酮是合成伊贝沙坦的中间体,实验室以如下图装置制备环戊酮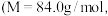 ,加热及夹持装置已省略),其反应原理:
,加热及夹持装置已省略),其反应原理: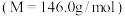 熔点为
熔点为 左右能升华并开始分解;环戊酮沸点
左右能升华并开始分解;环戊酮沸点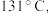 着火点30℃。
着火点30℃。
步骤如下:
I.将29.2g己二酸和适量Ba(OH)₂置于右图仪器a中,维持温度285~290℃,加热20分钟;
II.在馏出液中加入适量的 浓溶液,振荡锥形瓶、分液除去水层;将有机层转移至干燥锥形瓶,再次加入
浓溶液,振荡锥形瓶、分液除去水层;将有机层转移至干燥锥形瓶,再次加入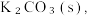 ,振荡分离出有机层;
,振荡分离出有机层;
III.组装蒸馏装置,对II所得有机层进行蒸馏,收集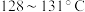 的馏分,称量获得产品12.6g,计算产率。
的馏分,称量获得产品12.6g,计算产率。
回答下列问题:
(1)步骤II中第一次加入K₂CO₃的作用是减小环戊酮的溶解性及_______ ,第二次加入 的作用是
的作用是_______ 。
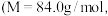 ,加热及夹持装置已省略),其反应原理:
,加热及夹持装置已省略),其反应原理: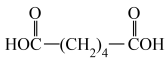

 +CO2↑+H2O↑。
+CO2↑+H2O↑。
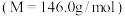 熔点为
熔点为 左右能升华并开始分解;环戊酮沸点
左右能升华并开始分解;环戊酮沸点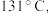 着火点30℃。
着火点30℃。步骤如下:
I.将29.2g己二酸和适量Ba(OH)₂置于右图仪器a中,维持温度285~290℃,加热20分钟;
II.在馏出液中加入适量的
 浓溶液,振荡锥形瓶、分液除去水层;将有机层转移至干燥锥形瓶,再次加入
浓溶液,振荡锥形瓶、分液除去水层;将有机层转移至干燥锥形瓶,再次加入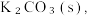 ,振荡分离出有机层;
,振荡分离出有机层;III.组装蒸馏装置,对II所得有机层进行蒸馏,收集
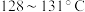 的馏分,称量获得产品12.6g,计算产率。
的馏分,称量获得产品12.6g,计算产率。回答下列问题:
(1)步骤II中第一次加入K₂CO₃的作用是减小环戊酮的溶解性及
 的作用是
的作用是
您最近半年使用:0次
7 . 柠檬酸铁铵[(NH4)3Fe(C6H5O7)2]易溶于水,不溶于乙醇等有机溶剂,是一种含铁量较高的补铁剂.实验室利用柠檬酸(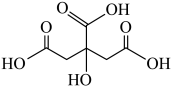 )制备柠檬酸铁铵的实验步骤如下:
)制备柠檬酸铁铵的实验步骤如下:
ii.降温至40℃,滴加一定量的氨水充分反应,生成柠檬酸亚铁铵(NH4FeC6H5O7)。
iii.控温40℃,缓慢滴加一定量的双氧水充分反应,经一系列操作,得到产品。
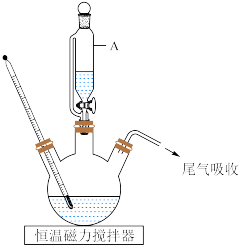
回答下列问题:
(1)仪器A的名称是
(2)步骤i中,若柠檬酸加入量逐渐增多,最终会导致柠檬酸铁铵的含铁量逐渐减少,可能的原因是
(3)步骤ii、iii中均需控温40℃的原因是
(4)步骤iii中制备柠檬酸铁铵的化学方程式
(5)为了测定产品的纯度,实验的基本原理是将Fe3+还原成Fe2+后,采用分光光度法来测定纯度.实验时测得样品的纯度显著偏低,检查实验发现配制样品溶液时少加了一种还原试剂,该试剂应为
您最近半年使用:0次
解题方法
8 . 呋喃甲酸(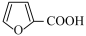 )是一种重要的有机合成中间体。实验室用呋喃甲醛(
)是一种重要的有机合成中间体。实验室用呋喃甲醛(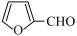 )制备呋喃甲酸,并获得副产品呋喃甲醇。
)制备呋喃甲酸,并获得副产品呋喃甲醇。
I.反应原理: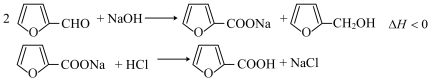
Ⅱ.实验装置: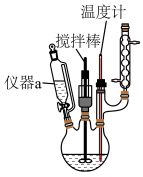
| 物质 | 相对分子质量 | 状态 | 熔点 | 沸点 | 溶解性 |
| 呋喃甲醛 | 96 | 油状液体 | 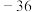 | 161.7 | 微溶于冷水,溶于热水、乙醇、乙醚 |
| 呋喃甲酸 | 112 | 白色晶体 | 130 | 易升华 | 难溶于冷水,易溶于乙醇、乙醚 |
| 呋喃甲醇 | 98 | 液体 |  | 171 | 溶于水,乙醇、乙醚 |
①向三颈烧瓶中加入
 呋喃甲醛,滴加
呋喃甲醛,滴加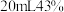 的
的 溶液,充分搅拌,保持反应温度在
溶液,充分搅拌,保持反应温度在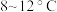 ,持续回流
,持续回流 。
。②冷却后,向三颈烧瓶中加入适量水使其完全溶解。
③将溶液转入分液漏斗中,少量多次加入乙醚萃取,合并乙醚萃取液,得到有机相(乙醚萃取液)和水相。
④向有机相中加入无水硫酸镁固体,再进一步分离乙醚和呋喃甲醇。
⑤向水相中滴加浓盐酸,冷却,结晶,抽滤,洗涤得到粗品
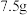 。
。回答下列问题:
(1)仪器a的名称为
A.
 B.
B. C.
C. D.
D.
(2)步骤①中反应温度保持在
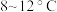 ,温度不宜过低的原因是
,温度不宜过低的原因是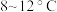 ,应采取的措施为
,应采取的措施为(3)步骤③中少量多次加入乙醚的目的是
(4)步骤④中加入硫酸镁固体的作用是
(5)纯度测定:称取
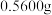 粗产品,配成
粗产品,配成 溶液。量取
溶液。量取 溶液,用
溶液,用 的
的 标准溶液滴定,三次滴定平均消耗
标准溶液滴定,三次滴定平均消耗 的
的 标准溶液。该产品中呋喃甲酸的纯度为
标准溶液。该产品中呋喃甲酸的纯度为
您最近半年使用:0次
9 . 宇航员王亚平曾在天宫课堂直播泡腾片水球实验。泡腾片中含有柠檬酸(结构简式如图)下列有关柠檬酸的说法不正确的是
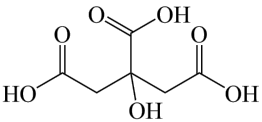
| A.柠檬酸的分子式为C6H8O7 | B.柠檬酸有两种不同的官能团 |
| C.柠檬酸分子中有手性碳原子 | D.1mol该有机物最多与3molNaOH反应 |
您最近半年使用:0次
10 . 脱落酸是一种能促进叶子脱落、提高植物的抗旱和耐盐力的植物激素,其结构简式如图所示。下列有关该化合物的叙述中错误的是
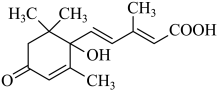
| A.该物质的分子式为C15H20O4 |
| B.该物质的同分异构体中含有芳香族化合物 |
| C.1mol该物质最多能与含2molNaOH的溶液反应 |
| D.1mol该物质最多能与4molH2反应 |
您最近半年使用:0次



