解题方法
1 . 东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___________ ,3d能级上的未成对电子数为___________ 。
(2)硫酸镍溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中
中 的空间立体构型是
的空间立体构型是___________ 。
②在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为___________ 。
③氨的沸点___________ (填“高于”或“低于”)膦( ),原因是
),原因是___________ 。氨分子中,中心原子的轨道杂化类型为___________ 。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成
 蓝色溶液。
蓝色溶液。①
 中
中 的空间立体构型是
的空间立体构型是②在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为③氨的沸点
 ),原因是
),原因是
您最近一年使用:0次
2 . 开发新型储氢材料是开发利用氢能的重要研究方向。
(1) ,是一种储氢材料,可由
,是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态 原子中,电子占据的最高能级符号为
原子中,电子占据的最高能级符号为___________ ,原子核外电子有___________ 种空间运动状态。
② 、B、H元素的电负性由大到小的排列顺序为
、B、H元素的电负性由大到小的排列顺序为___________ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
① 中,离子半径:
中,离子半径:
___________ (填“>”“=”或“<”) ,原因是
,原因是___________ 。
②某储氢材料是短周期金属元素M的氢化物。M原子的部分电离能如表所示:
则M是___________ (填元素名称)。下列状态的粒子中,电离出最外层一个电子所需能量最大的是___________ (填字母)。

A. B.
B. C.
C.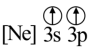 D.
D.
(3)碳有很多同素异形体, 就是其中一种,可用作储氢材料。已知金刚石为立体网状结构,其
就是其中一种,可用作储氢材料。已知金刚石为立体网状结构,其 键的键长为
键的键长为 ,
, 分子中
分子中 键键长为
键键长为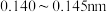 ,有同学据此认为
,有同学据此认为 的熔点高于金刚石,你认为是否正确?
的熔点高于金刚石,你认为是否正确?___________ ,阐述理由:___________ 。
(1)
 ,是一种储氢材料,可由
,是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态
 原子中,电子占据的最高能级符号为
原子中,电子占据的最高能级符号为②
 、B、H元素的电负性由大到小的排列顺序为
、B、H元素的电负性由大到小的排列顺序为(2)金属氢化物是具有良好发展前景的储氢材料。
①
 中,离子半径:
中,离子半径:
 ,原因是
,原因是②某储氢材料是短周期金属元素M的氢化物。M原子的部分电离能如表所示:
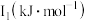 | 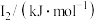 | 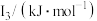 | 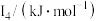 | 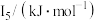 |
| 738 | 1451 | 7733 | 10540 | 13630 |
则M是

A.
 B.
B. C.
C. D.
D.
(3)碳有很多同素异形体,
 就是其中一种,可用作储氢材料。已知金刚石为立体网状结构,其
就是其中一种,可用作储氢材料。已知金刚石为立体网状结构,其 键的键长为
键的键长为 ,
, 分子中
分子中 键键长为
键键长为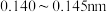 ,有同学据此认为
,有同学据此认为 的熔点高于金刚石,你认为是否正确?
的熔点高于金刚石,你认为是否正确?
您最近一年使用:0次
名校
解题方法
3 . 我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”、“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其成分主要为BaCuSi4O10、BaCuSi2O6。
(1)“中国蓝”、“中国紫”中均有Cun+离子,n=___________ ,基态时该阳离子的价电子排布式为___________ 。
(2)“中国蓝”的发色中心是以Cun+为中心离子的配位化合物,其中提供孤对电子的是____ 元素。
(3)已知Cu、Zn的第二电离能分别为1957.9 kJ·mol-1、1733.3 kJ·mol-1,前者高于后者的原因是________________________________________ 。
(4)铜常用作有机反应的催化剂。例如,2CH3CH2OH+O2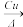 2CH3CHO+2H2O。
2CH3CHO+2H2O。
①乙醇的沸点高于乙醛,其主要原因是_________________________________ ;乙醛分子中π键与σ键的个数比为___________ 。
②乙醛分子中碳原子的杂化轨道类型是___________ 。
(5)铜的晶胞如图所示。铜银合金是优质的金属材料,其晶胞与铜晶胞类似,银位于顶点,铜位于面心。
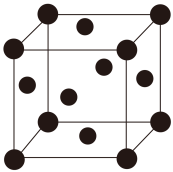
①该铜银合金的化学式是___________________ 。
②已知:该铜银晶胞参数为a cm,晶体密度为ρ g·cm-3。则阿伏加 德罗常数(NA)为_______ mol-1(用代数式表示,下同)。
③若Ag、Cu原子半径分别为b cm、c cm,则该晶胞中原子空间利用率φ为___________ 。(提示:晶胞中原子空间利用率=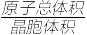 ×100%)
×100%)
(1)“中国蓝”、“中国紫”中均有Cun+离子,n=
(2)“中国蓝”的发色中心是以Cun+为中心离子的配位化合物,其中提供孤对电子的是
(3)已知Cu、Zn的第二电离能分别为1957.9 kJ·mol-1、1733.3 kJ·mol-1,前者高于后者的原因是
(4)铜常用作有机反应的催化剂。例如,2CH3CH2OH+O2
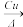 2CH3CHO+2H2O。
2CH3CHO+2H2O。①乙醇的沸点高于乙醛,其主要原因是
②乙醛分子中碳原子的杂化轨道类型是
(5)铜的晶胞如图所示。铜银合金是优质的金属材料,其晶胞与铜晶胞类似,银位于顶点,铜位于面心。

①该铜银合金的化学式是
②已知:该铜银晶胞参数为a cm,晶体密度为ρ g·cm-3。则阿伏加 德罗常数(NA)为
③若Ag、Cu原子半径分别为b cm、c cm,则该晶胞中原子空间利用率φ为
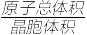 ×100%)
×100%)
您最近一年使用:0次
2020-05-28更新
|
1376次组卷
|
6卷引用:河南省原阳县第一高级中学2021-2022学年高三上学期开学适应性考试理综化学试题
4 . 以黄铜矿(主要成分为铁、铜、硫三种元素组成的化合物)为基本原料,通过一系列的冶炼可得到铜、铁、SO2、SO3、H2SO4等物质,回答下列问题:
(1)基态铁原子价层电子排布式为____________ ,基态硫原子的核外电子共有_______ 种不同的能量。硫元素所在周期的非金属元素第一电离能由大到小的顺序为__________ 。
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是________ ,SO2的分子构型是____________ ,属于非极性分子的氧化物是___________ 。
(3)在溶液中Cu2+易与水形成[Cu(H2O)6]2+而显蓝色,向相应的溶液中加入足量的氨水可得到[Cu(NH3)4(H2O)2]2+,则[Cu(NH3)4(H2O)2]2+中Cu2+的配位数是________________ ,氧铜配位键与氮铜配位键相比,较稳定的是___________________ 。
(4)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,试解释导致这种差异最可能的原因是___________ 。
(5)由铁、铜、硫形成的某种化合物的晶胞是一个长方体,结构如图所示,则该化合物的化学式为____________ 。若晶体密度为dg·cm﹣3,则晶胞的高h=_______ pm(写出简化后的计算式即可)。

(1)基态铁原子价层电子排布式为
(2)SO2、SO3、H2SO4中,硫原子的杂化轨道类型为sp3的物质是
(3)在溶液中Cu2+易与水形成[Cu(H2O)6]2+而显蓝色,向相应的溶液中加入足量的氨水可得到[Cu(NH3)4(H2O)2]2+,则[Cu(NH3)4(H2O)2]2+中Cu2+的配位数是
(4)氧化铜的熔点为1326℃、沸点为1800℃;氧化亚铜的熔点为1235℃、沸点为1100℃,试解释导致这种差异最可能的原因是
(5)由铁、铜、硫形成的某种化合物的晶胞是一个长方体,结构如图所示,则该化合物的化学式为

您最近一年使用:0次
2020-03-17更新
|
640次组卷
|
3卷引用:河南省确山县第二高级中学2021-2022学年高三上学期期中考试化学试题



