名校
1 . 表为周期表的一部分,其中的编号代表对应的元素,请用元素符号 回答下列问题
(1)上述元素中,属于ds区的是_______ (填元素符号)。
(2)不能 说明⑨的金属性比⑩强的是_______ 。
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是_______ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ 分子的空间构型为_______ 。
(4)元素⑫与 可形成
可形成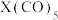 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于_______ 晶体(填晶体类型)。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ⑪ | ⑫ | ⑬ | ⑭ |
(2)
A.⑨与稀盐酸反应比⑩与同条件稀盐酸反应剧烈;
B.⑨单质的熔、沸点比⑩的低;
C.⑨的最高价氧化物对应水化物的碱性比⑩的最高价氧化物对应水化物的碱性强;
D.与非金属单质反应时,⑨原子失电子数目比⑩原子失电子数目少;
(3)④与元素①形成的最简单化合物X是
(4)元素⑫与
 可形成
可形成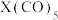 型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
2021-04-28更新
|
657次组卷
|
4卷引用:专题4 综合检测(基础卷)
专题4 综合检测(基础卷)(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测天津市耀华中学2020-2021学年高二下学期期中检测化学试题天津北京师范大学静海附属学校2021-2022学年高二下学期期中考试化学试题
2 . 下列有关元素周期表和元素周期律的说法,不正确的是
①元素周期表中s区、d区和ds区的元素都是金属元素
②d区元素最后一个核外电子一定填充在s能级上
③同一主族从上到下,元素的电负性依次增大
④同一主族从上到下,元素的第一电离能依次增大
①元素周期表中s区、d区和ds区的元素都是金属元素
②d区元素最后一个核外电子一定填充在s能级上
③同一主族从上到下,元素的电负性依次增大
④同一主族从上到下,元素的第一电离能依次增大
| A.只有①②③ | B.只有②③ | C.只有③④ | D.①②③④ |
您最近一年使用:0次
2021-04-24更新
|
1063次组卷
|
3卷引用:第一章原子结构与性质(提升卷)
第一章原子结构与性质(提升卷)辽宁省盘锦市第二高级中学2020-2021学年高二下学期第一阶段考试化学试题(已下线)第1章 原子结构与性质(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)
名校
解题方法
3 . 下列关于Na、Mg、Al元素及其化合物的说法正确的是
| A.Mg在周期表中位于p区 |
| B.原子半径:r(Na)<r(Mg)<r(Al) |
| C.第一电离能:I1(Na)<I1(Al)<I1(Mg) |
| D.最高价氧化物的水化物的碱性:NaOH<Mg(OH)2<Al(OH)3 |
您最近一年使用:0次
2021-03-27更新
|
815次组卷
|
10卷引用:专题1~2 综合检测(基础卷)
专题1~2 综合检测(基础卷)海南省海南鑫源高级中学2020-2021学年高二下学期第一次月考化学试题河北省石家庄市第二中学2020-2021学年高二4月月考化学试题江苏省镇江市镇江中学2020-2021学年高二下学期期中考试化学试题海南省三亚华侨学校(南新校区)2020-2021学年高二下学期期中考试化学试题河北省沧州市肃宁一中2020-2021学年高二下学期4月月考化学试题南京市第一中学2021-2022学年高二下学期3月阶段检测化学试题江苏省南京市盐城市2021届高三第二次模拟考试化学试题(已下线)2022年江苏卷高考真题变式题1-13(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题1-5)
4 . 元素周期表中某区域的一些元素多用于制造半导体材料,它们是
| A.左下方区域的金属元素 |
| B.右上方区域的非金属元素 |
| C.金属元素和非金属元素分界线附近的元素 |
| D.稀有气体元素 |
您最近一年使用:0次
2021-03-25更新
|
2484次组卷
|
95卷引用:2017秋季学期人教版高二化学必修2 第一单元检测试题B
2017秋季学期人教版高二化学必修2 第一单元检测试题B(已下线)2010年河北省唐山一中高二上学期期中考试化学卷黑龙江省青冈县一中2018-2019学年高二上学期开学考试化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高二下学期3月月考化学试题贵州省遵义航天高级中学2019-2020学年高二上学期期中考试化学(文)试题(已下线)山西省原平市范亭中学2018-2019学年高二4月月考化学试题广西壮族自治区贺州市中学2020-2021学年高二上学期第二次月考化学试题海南省三亚华侨学校(南新校区)2020-2021学年高二下学期期中考试化学试题(已下线)第四章 物质结构 元素周期律(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)09—10年海南嘉积中学高一下学期期末考试化学卷(文科)(已下线)2010年河北省蔚县一中高一下学期期末考试化学试题(已下线)2010-2011学年吉林省延吉市汪清六中高一下学期期中考试化学试卷(已下线)2010-2011学年吉林省汪清中学高一下学期期中考试化学试卷(已下线)2010-2011学年云南省武定一中高一下学期期中考试化学试卷(已下线)2011-2012学年四川省金堂中学高一下学期期中考试化学试卷(已下线)2011-2012学年贵州省遵义四中高一下学期期中考试化学试卷(已下线)2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(已下线)2013-2014甘肃省肃南县第一中学高一下学期期末考试化学试卷(已下线)2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷2014-2015广西桂林市第十八中学高一下学期期中考试化学试卷2015-2016学年河北省定兴三中高一下3月月考(文)化学试卷2015-2016学年吉林省汪清六中高一3月月考化学试卷2015-2016学年江苏省盐城中学高一下学期期中化学试卷2015-2016学年安徽黄山屯溪一中高一下期中化学试卷2015-2016学年湖南省娄底市双峰县高一下期中化学试卷2015-2016学年贵州凯里一中高一下期中文科化学试卷2015-2016学年贵州凯里一中高一下期中理科化学试卷2015-2016学年重庆四十二中高一下期中化学试卷2015-2016学年广东省广州市南沙区高一下学期期末考试化学试卷2016-2017学年湖北省孝感市七校教学联盟高一下学期期中考试化学试卷湖南省师范大学附属中学2016-2017学年高一下学期期中考试化学试题(已下线)北京市第四中学2016-2017学年高一下学期期中考试化学试题河南省林州一中分校(林虑中学)2017-2018学年高一下学期开学考试化学试题(已下线)【段考模拟】高一化学下学期第一次月考(3月)原创B卷辽宁省大连市渤海高级中学2017-2018学年高一4月月考(文)化学试题西藏林芝二中2017-2018学年高一下学期期末考试化学试题【全国百强校】辽宁省实验中学2016-2017学年高一下学期期中考试文科反向理科综合化学试题【全国百强校】吉林省实验中学2019届高三上学期第四次模拟考试化学试题福建省华安县第一中学2019届高三上学期第二次(12月)月考化学试题湖北省宜昌市葛洲坝中学2018-2019学年高一下学期期中考试化学试题【全国百强校】吉林省长春市外国语学校2018-2019学年高一下学期期中考试化学试题河南省永城市实验高级中学2018-2019学年高一下学期期中考试化学试题黑龙江省绥滨县第一中学2018-2019学年高一(文)下学期期中考试化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高一下学期期中考试化学试题甘肃省东乡族自治县第二中学2017-2018学年高一下学期期中考试化学试题江苏省苏州市张家港高级中学2018-2019学年高一下学期期中考试化学试题天津市部分区2018-2019学年高一下学期期末考试化学试题新疆乌鲁木齐市第四中学2018-2019学年高一下学期期中考试化学试题湖南省常德市淮阳中学2019-2020学年高一上学期期中考试化学试题湖南省怀化市第三中学2018-2019学年高一下学期3月月考化学试题山东省青岛平度市2019-2020学年高一下学期线上阶段测试化学试题湖南省怀化市2019-2020学年高一上学期入学考试化学试题(已下线)专题5.2 元素周期律和元素周期表(练)——2020年高考化学一轮复习讲练测陕西省咸阳市实验中学2019-2020学年高一下学期第二次月考化学试题安徽省桐城市第八中学2019-2020学年高一下学期期中考试化学试题四川省成都外国语学校2019-2020学年高一下学期期末考试化学(文)试题重庆市巴蜀中学2019-2020学年高一下学期期末考试化学试题四川省都江堰市第三中学2019-2020学年高一下学期期末复习测试文科化学试题西藏自治区林芝市第二高级中学2019-2020学年高一下学期第二学段考试(期末)化学试题黑龙江省牡丹江市海林林业局第一中学2019-2020学年高一阶段性测试化学试题河南省开封市2019-2020学年高一下学期期末调研考试化学试题吉林省吉林市2020-2021学年高一上学期期末调研测试化学试题湖南省长沙市周南中学2020-2021学年高一上学期期末考试化学试题河北省张家口宣化一中2020-2021学年高一下学期3月月考化学试题内蒙古集宁二中2020-2021学年高一下学期第一次月考化学试题(已下线)【浙江新东方】双师189高一下广西平果市第二中学2020-2021学年高一下学期期中考试化学(文)试题广东省珠海市艺术高级中学2020-2021学年高一下学期期中考试化学试题新疆阿克苏沙雅县沙雅一中2020-2021学年高一下学期期中考试化学试题甘肃省玉门市第一中学2020-2021学年高一下学期期中考试化学试题广西南宁市宾阳县宾阳中学2020-2021学年高一下学期期中考试化学(文)试题甘肃省静宁县第一中学2020-2021学年高一下学期第二次月考化学(普通班)试题河南省许昌市2020-2021学年高一下学期期末质量检测化学试题云南省曲靖市罗平县第二中学2020-2021学年高一下学期6月月考文科化学试题广东省茂名市电白区2021-2022学年高一上学期期末考试化学试题新疆吐鲁番市2021-2022学年高一上学期期末考试化学试题广东省汕头市潮南区2021-2022学年高一上学期期末考试化学试题甘肃省民乐县第一中学2021-2022学年高一下学期3月第一次月考化学试题云南省昆明市第一中学2021-2022学年高一上学期期末考试化学试题(已下线)4.2.2 元素周期表和元素周期律的应用-2021-2022学年高一化学课后培优练(人教版2019必修第一册)新疆喀什地区普通高中2021-2022学年高一上学期期末考试化学试题广东省广州市黄浦区2021-2022学年高一上学期期末考试化学试题陕西省西安市鄠邑区第二中学2021-2022学年高一下学期第一次月考化学试题河南省平顶山市蓝天高级中学2021-2022学年高一上学期期末考试化学试题广东省广州市第八十九中学2022-2023学年高一上学期期末考试化学试题天津市河北区 2022-2023 学年高一上学期期末质量检测化学试题广东省江门市第一中学2022-2023学年高一上学期期末考试化学试题河南省洛阳市2022-2023学年高一上学期期末考试化学试题甘肃省民勤县第一中学2022-2023学年度高一下学期期中考试(选考)化学试题广东省广州市白云中学2022-2023学年高一上学期期末考试化学试题天津市红桥区2022-2023学年高一上学期期末考试化学试题广东省广州市黄广中学2023-2024学年高一上学期期末错题专项考化学试卷广东省汕头市金山中学2023-2024学年高一上学期期末考试 化学试题 河南省开封市联考2023-2024学年高一上学期1月期末化学试题湖南省娄底市涟源市行知高级中学2023-2024学年高一上学期1月期末化学试题
20-21高二·全国·单元测试
解题方法
5 . I.元素在周期表中的位置反映了元素的原子结构和性质。请回答下列有关硼(B)元素的问题:
(1)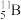 原子核内的中子数为
原子核内的中子数为________ 。
(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为___________ 。
(3)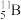 的原子半径比
的原子半径比 的原子半径
的原子半径__________ (填“大”或“小”)。
(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性_______ (填“强”或“弱”)。
II.如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
请回答下列问题:
(1)元素②的原子结构示意图是_______________ 。
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为_________ (填离子符号)。
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为___________________ 。
(4)⑧与⑩两种元素非金属较强的是_______ (填元素符号)。
(1)
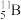 原子核内的中子数为
原子核内的中子数为(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为
(3)
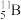 的原子半径比
的原子半径比 的原子半径
的原子半径(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性
II.如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)元素②的原子结构示意图是
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为
(4)⑧与⑩两种元素非金属较强的是
您最近一年使用:0次
6 . 下表列出了某短周期元素R的各级电离能数据(用I表示,单位为kJ·mol-l)。下列关于元素R的判断中一定正确的是( )
电离能 | I1 | I2 | I3 | I4 | …… |
E | 740 | 1 500 | 7700 | 10500 | …… |
| A.R的最高正价为+3价 |
| B.R元素的原子最外层共有4个电子 |
| C.R元素位于元素周期表中ⅡA族 |
| D.R 元素基态原子的电子排布式为1s22s2 |
您最近一年使用:0次
20-21高二·全国·单元测试
解题方法
7 . 下表是元素周期表短周期的一部分:
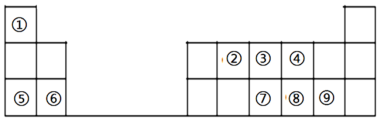
请按要求用化学用语 回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为______ ;
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程______ ;
(3)比元素⑦的原子序数多17的元素在周期表的位置为______ ;
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式______ ,若将其溶于水,破坏了其中的______ (填“离子键”、“共价键”或“离子键和共价键”);

请按要求
(1)元素④、⑥、⑨的离子半径由大到小的顺序为
(2)用电子式表示元素④与元素⑥形成的化合物的形成过程
(3)比元素⑦的原子序数多17的元素在周期表的位置为
(4)写出由①④⑤三种元素组成的一种离子化合物的电子式
您最近一年使用:0次
名校
8 . 下表是元素周期表的前三周期。表中所列的字母分别代表某一种化学元素。下列说法正确的是


A.沸点: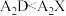 |
B. 分子是非极性分子 分子是非极性分子 |
C.C形成的单质中 键与π键的个数之比为1:2 键与π键的个数之比为1:2 |
| D.B、C、D的简单氢化物的空间结构相同 |
您最近一年使用:0次
2021-02-19更新
|
617次组卷
|
5卷引用:第二章 分子结构与性质(A卷)
9 . 如图是元素周期表的一部分,图中所列的字母分别代表某一化学元素。
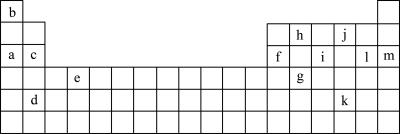
(1)下列______ (填序号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子失去核外不同电子所需的能量/( )
)
①X可能为图中13种元素中的______ (填字母)。用元素符号表示X和j形成的化合物的化学式:______ 。
②Y是周期表中第______ 族的元素。
③图中13种元素中,______ (填字母)元素原子失去核外第1个电子需要的能量最多。

(1)下列
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子失去核外不同电子所需的能量/(
 )
)| 元素 | 锂 | X | Y |
| 失去第1个电子 | 519 | 502 | 580 |
| 失去第2个电子 | 7296 | 4570 | 1820 |
| 失去第3个电子 | 11799 | 6920 | 2750 |
| 失去第4个电子 | — | 9550 | 11600 |
②Y是周期表中第
③图中13种元素中,
您最近一年使用:0次
2021-02-06更新
|
697次组卷
|
2卷引用:第一章 原子结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)
10 . 下列有关原子结构与性质的叙述中,不正确的是
| A.2p和3p轨道形状均为哑铃形 |
| B.第三周期元素中第一电离能介于Mg和S之间的元素只有1种 |
| C.第四能层有4个能级,最多容纳36个电子 |
| D.主族元素处于元素周期表的s区和p区 |
您最近一年使用:0次
2021-01-20更新
|
451次组卷
|
4卷引用:专题2 原子结构与元素性质 本专题达标检测
专题2 原子结构与元素性质 本专题达标检测辽宁省锦州市2020-2021学年高二上学期期末考试化学试题(已下线)1.2 原子结构与元素的性质(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)福建省厦门市翔安第一中学2020-2021学年高二下学期期中考试化学试题



