21-22高二下·全国·单元测试
1 . 元素周期表的基本结构
(1)周期元素种数的确定
第一周期从_______ 开始,以_______ 结束,只有两种元素。其余各周期总是从_______ 能级开始,以_______ 结束,从ns能级开始以np结束递增的_______ (或电子数)就等于每个周期里的元素数目。
(2)元素周期表的形成
若以一个方格代表一种元素,每个_______ 排一个横排,并按s、p、d、f分段,左侧对齐,可得到如图元素周期表:
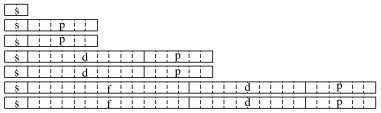
若将p段与p段对齐,d段与d段对齐、f段单独列出,将_______ 与p段末端对齐,则得到书末的元素周期表:
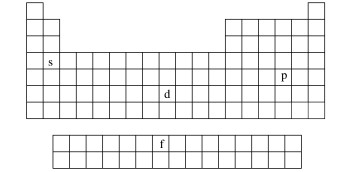
(1)周期元素种数的确定
第一周期从
| 周期 | ns~np | 电子数 | 元素数目 |
| 一 | 1s1~2 | ||
| 二 | 2s1~22p1~6 | ||
| 三 | 3s1~23p1~6 | ||
| 四 | 4s1~23d1~104p1~6 | ||
| 五 | 5s1~24d1~105p1~6 | ||
| 六 | 6s1~24f1~145d1~106p1~6 | ||
| 七 | 7s1~25f1~146d1~107p1~6 |
(2)元素周期表的形成
若以一个方格代表一种元素,每个

若将p段与p段对齐,d段与d段对齐、f段单独列出,将

您最近一年使用:0次
21-22高二下·全国·单元测试
2 . 元素周期表探究
①元素周期表的结构

②元素周期表的分区
i.根据核外电子的排布分区
按电子排布式中最后填入电子的_______ 符号可将元素周期表分为s、p、d、f 4个区,而ⅠB、ⅡB族这2个纵行的元素的核外电子因先填满了_______ 能级而后再填充ns能级而得名_______ 区。5个区的位置关系如图所示。
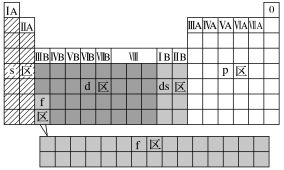
ii.根据元素的金属性和非金属性分区
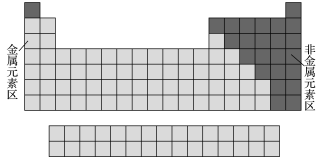
①元素周期表的结构

②元素周期表的分区
i.根据核外电子的排布分区
按电子排布式中最后填入电子的

ii.根据元素的金属性和非金属性分区

您最近一年使用:0次
解题方法
3 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:_______ 周期_______ 族。
(2)X原子在第二电子层上只有一个空轨道,则X是_______ ;其轨道表示式为_______ 。
(3)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:_______ 。
(4)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:_______ 。
(5)写出3p轨道上有2个未成对电子的元素符号:_______ 。
(6)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:_______ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)X原子在第二电子层上只有一个空轨道,则X是
(3)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(4)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:
(5)写出3p轨道上有2个未成对电子的元素符号:
(6)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:
您最近一年使用:0次
2022-12-20更新
|
290次组卷
|
2卷引用:山东省威海市文登新一中2021-2022学年高二上学期期中考试化学试题
22-23高一上·全国·课时练习
4 . 原子结构特点(F→I)
(1)相似性:最外层电子数均为_______ 。
(2)递变性:电子层数逐渐_______ ,原子半径逐渐_______ 。
(1)相似性:最外层电子数均为
(2)递变性:电子层数逐渐
您最近一年使用:0次
22-23高一上·全国·课时练习
5 . 元素周期表和元素周期律的应用
(1)根据同周期、同主族元素性质的递变规律判断元素性质的_______________ 。
(2)应用于_______________ 元素的相互推断。
(3)预测新元素
为新元素的发现及预测它们的_______________ 提供线索。
(4)寻找新物质
①在金属与非金属分界线附近寻找_______________ 。
②研究_______________ 附近元素,制造新农药。
③在_______________ 中寻找催化剂和耐高温、耐腐蚀的合金材料。
(1)根据同周期、同主族元素性质的递变规律判断元素性质的
(2)应用于
(3)预测新元素
为新元素的发现及预测它们的
(4)寻找新物质
①在金属与非金属分界线附近寻找
②研究
③在
您最近一年使用:0次
6 . 数量关系

(1)列序数与族序数的关系
①列序数<8,主族和副族的族序数=__________ ;
②列序数=8或9或10,为第Ⅷ族;
③列序数>10,主族和副族的族序数=_____________ (0族除外)。
(2)三个定量关系
①周期序数=______________ 。
②主族序数=______________ 。
③原子序数=_______________________________________ 。
(3)原子序数的定量关系
①同周期,IIA与IIIA族原子序数差可能为_________________ ;
②同族,相邻周期原子序数差:IA~IIA:_________________ ;
IIIA~0族:_________________ 。如Na与K相差8,Cl与Br相差18。

(1)列序数与族序数的关系
①列序数<8,主族和副族的族序数=
②列序数=8或9或10,为第Ⅷ族;
③列序数>10,主族和副族的族序数=
(2)三个定量关系
①周期序数=
②主族序数=
③原子序数=
(3)原子序数的定量关系
①同周期,IIA与IIIA族原子序数差可能为
②同族,相邻周期原子序数差:IA~IIA:
IIIA~0族:
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
7 . 元素周期表的结构
(1)编排原则

(2)元素周期表的结构

②族的分类

③常见族的别称:第IA族(除氢外)—__________ ,VIIA—__________ ,0族—________________ ,IVA、VA、VIA族依次又叫_______________________ 。
(1)编排原则

(2)元素周期表的结构

②族的分类

③常见族的别称:第IA族(除氢外)—
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
8 . 原子序数
(1)含义:按照元素在周期表中的_______ 给元素编号。
(2)原子序数与元素的原子结构之间存在的关系:原子序数=__________________ 。
(1)含义:按照元素在周期表中的
(2)原子序数与元素的原子结构之间存在的关系:原子序数=
您最近一年使用:0次
解题方法
9 . 元素周期律和元素周期表对深入认识物质的性质具有重要的作用,有利于将零散的元素及其化合物的知识整合起来形成知识网络。通过本章的学习,你是否对学习过的元素及其化合物的知识进行了整合?请尝试用图示的方式进行总结,并与同学们交流分享,示例如下:
李明打开元素周期表,看到元素符号“N”,便按照以下思路回顾和整理了关于氮元素的相关知识。
(1)氮元素的原子结构示意图_____ 、元素符号_____ 。
(2)氮元素所在周期的元素性质递变规律_____ 。
(3)氮元素所在主族的元素性质递变规律_____ 。
(4)含有氮元素的常见物质的性质及它们之间的转化关系_____ 。
李明打开元素周期表,看到元素符号“N”,便按照以下思路回顾和整理了关于氮元素的相关知识。
(1)氮元素的原子结构示意图
(2)氮元素所在周期的元素性质递变规律
(3)氮元素所在主族的元素性质递变规律
(4)含有氮元素的常见物质的性质及它们之间的转化关系
您最近一年使用:0次
10 . 请回答下列问题。
(1)下列叙述中,正确的是_______
(2)请利用原子结构知识对下列结论进行说明和论证。
结论1:同周期的主族元素,从左到右,元素原子失电子能力越来越弱。______ 。
结论2:碱金属元素,从上到下,元素原子失电子能力越来越强。______ 。
(1)下列叙述中,正确的是_______
| A.同周期元素中,ⅦA族元素的原子半径最大 |
| B.ⅥA族元素的原子,其原子半径越大,越容易得到电子 |
| C.常温时,0族元素的单质都是气体 |
| D.在元素周期表中,从ⅢB族到ⅡB族10个纵列的元素都是金属元素 |
结论1:同周期的主族元素,从左到右,元素原子失电子能力越来越弱。
结论2:碱金属元素,从上到下,元素原子失电子能力越来越强。
您最近一年使用:0次



