2024高一上·全国·专题练习
1 . 下图是元素周期表的一部分。
(1)①-⑩元素中最稳定的原子是___________ (填元素符号);形成的气态氢化物稳定性最强的是___________ (填氢化物的化学式)。
(2)①和⑦金属性相似,①的最高价氧化物对应的水化物与KOH溶液反应的离子方程式为___________ 。
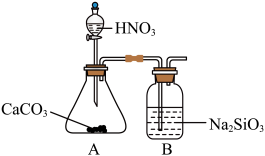
(3)某同学设计了如下实验证明非金属性③>②>⑧。已知H2SiO3是不溶于水的白色胶状沉淀,HNO3易挥发。___________ (答“合理”或“不合理”),原因是___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)①-⑩元素中最稳定的原子是
(2)①和⑦金属性相似,①的最高价氧化物对应的水化物与KOH溶液反应的离子方程式为
(3)某同学设计了如下实验证明非金属性③>②>⑧。已知H2SiO3是不溶于水的白色胶状沉淀,HNO3易挥发。
您最近一年使用:0次
名校
2 . 下表是部分元素周期表的结构图,请根据要求回答下列问题。
(1)以上元素的最高价氧化物对应的水化物中,酸性最强的酸是_______ (填化学式)。
(2)元素④、⑤所形成的简单离子半径较大的是_______ (用化学符号表示)。
(3)由①、③、⑧三种元素以原子个数比4:1:1形成的化合物中含有的化学键类型是_____ 。
(4)A、B均为以上某两种元素组成的含四个原子核的分子,A中有10个电子,B中有18个电子,则A的电子式_____ ,B的结构式_____ 。
(5)元素⑤、⑥的最高价氧化物对应水化物之间反应的离子方程式_______ 。
(6)已知周期表中存在对角相似规则,如Li与Mg在周期表中处于对角线位置则化学性质相似。根据“对角线规则”,铍(Be)的性质与上述六种元素中的_______ (填名称)相似,能溶于氢氧化钠溶液,请写出氢氧化铍与氢氧化钠溶液反应的化学方程式_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素④、⑤所形成的简单离子半径较大的是
(3)由①、③、⑧三种元素以原子个数比4:1:1形成的化合物中含有的化学键类型是
(4)A、B均为以上某两种元素组成的含四个原子核的分子,A中有10个电子,B中有18个电子,则A的电子式
(5)元素⑤、⑥的最高价氧化物对应水化物之间反应的离子方程式
(6)已知周期表中存在对角相似规则,如Li与Mg在周期表中处于对角线位置则化学性质相似。根据“对角线规则”,铍(Be)的性质与上述六种元素中的
您最近一年使用:0次
2024-05-07更新
|
197次组卷
|
2卷引用:广西柳州高级中学2023-2024学年高一上学期寒假月考化学试题(二)
名校
3 . I.请用下列10种物质的序号填空。
①N2 ②NH4Cl ③RbOH ④ ⑤ KCl ⑥
⑤ KCl ⑥ ⑦
⑦ ⑧H2SO4 ⑨
⑧H2SO4 ⑨ ⑩氦气
⑩氦气
(1)既含离子键又含共价键的是___________ ;只含共价键的的是___________ ;④的电子式为___________ ;⑦的空间构型为:___________ 。
II.下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑭回答下列问题。
(2)i.⑪~⑭元素的非金属性由强到弱的顺序为:___________ (填元素符号)。
ii.能作为卤素非金属性递变规律的判断依据的是:___________ 。
A.⑪~⑭元素形成的单质熔点逐渐升高
B.⑪~⑭元素形成的简单离子还原性逐渐增强
C.⑪~⑭元素形成的气态氢化物稳定性逐渐减弱
D.⑪~⑭元素形成的无氧酸酸性逐渐增强
iii.从原子结构角度解释卤素非金属性递变的原因___________ 。
(3)下列关于②~⑤元素叙述正确的是___________。
(4)③⑧⑩元素最高价氧化物对应的水化物之间可以两两发生反应,其中能体现水化物呈“两性”的离子方程式分别为___________ 、___________ 。
(5)上述元素形成的最高价氧化物的水化物中酸性最强的是___________ (用化学式表示)。
(6)元素④⑦⑩⑫对应的具有稳定结构的简单离子的半径由大到小的排序为___________ (用相应的离子符号排序)。
(7)用电子式表示①和⑦形成化合物的过程___________ ,该化合物与水反应的化学方程式是___________ 。
①N2 ②NH4Cl ③RbOH ④
 ⑤ KCl ⑥
⑤ KCl ⑥ ⑦
⑦ ⑧H2SO4 ⑨
⑧H2SO4 ⑨ ⑩氦气
⑩氦气(1)既含离子键又含共价键的是
II.下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
| 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ⑨ | ⑪ | |||||
| 3 | ③ | ⑥ | ⑧ | ⑩ | ⑫ | |||
| 4 | ④ | ⑦ | ⑬ | |||||
| 5 | ⑤ | ⑭ |
(2)i.⑪~⑭元素的非金属性由强到弱的顺序为:
ii.能作为卤素非金属性递变规律的判断依据的是:
A.⑪~⑭元素形成的单质熔点逐渐升高
B.⑪~⑭元素形成的简单离子还原性逐渐增强
C.⑪~⑭元素形成的气态氢化物稳定性逐渐减弱
D.⑪~⑭元素形成的无氧酸酸性逐渐增强
iii.从原子结构角度解释卤素非金属性递变的原因
(3)下列关于②~⑤元素叙述正确的是___________。
| A.从上到下②~⑤单质与水反应越来越剧烈 |
| B.②~⑤单质与氧气反应均可生成过氧化物 |
| C.从上到下②~⑤单质熔沸点逐渐升高 |
| D.②~⑤元素的最高价氧化物的水化物碱性增强 |
(5)上述元素形成的最高价氧化物的水化物中酸性最强的是
(6)元素④⑦⑩⑫对应的具有稳定结构的简单离子的半径由大到小的排序为
(7)用电子式表示①和⑦形成化合物的过程
您最近一年使用:0次
解题方法
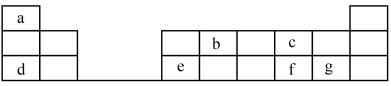
4 . 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分。______ (金属或非金属)元素;元素b在元素周期表中的位置为______ 。
(2)元素c的原子结构示意图_______ ;元素f的元素符号为______ ;元素c和f的原子半径大小关系为c____ f(>或<)
(3)元素d和元素g形成的盐的电子式为_______ 。
(4)第一电离能a___ d(>或<),非金属性c___ f(>或<)。
(2)元素c的原子结构示意图
(3)元素d和元素g形成的盐的电子式为
(4)第一电离能a
您最近一年使用:0次
5 . 按要求回答下列问题:
(1)消毒液的组成元素中,基态O原子的电子排布式是______ ,基态Cl原子未成对电子数为_____ 个。
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为_______ (填元素符号),氧元素和氮元素的非金属性的大小顺序为________ (填元素符号)
(3)某元素原子的最外层电子构型为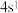 ,元素周期表的位置第
,元素周期表的位置第____ 周期,第_____ 族,它属于____ 区元素。
(1)消毒液的组成元素中,基态O原子的电子排布式是
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为
(3)某元素原子的最外层电子构型为
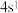 ,元素周期表的位置第
,元素周期表的位置第
您最近一年使用:0次
解题方法
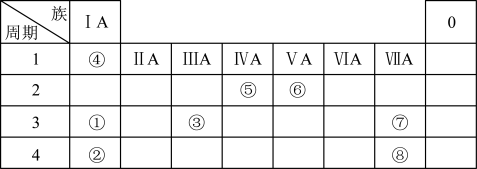
6 . 下表是元素周期表的一部分。请按要求回答下列问题:___________ ,⑦的最高价氧化物对应水化物的化学式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是___________ (填化学式)。
(3)写出由上述所列元素形成的18电子的双原子分子的化学式___________ 。
(4)下列说法不正确的是___________。
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式___________ 。
(2)上述所列元素最高价氧化物对应水化物碱性最强的是
(3)写出由上述所列元素形成的18电子的双原子分子的化学式
(4)下列说法不正确的是___________。
| A.⑥形成的最简单氢化物比⑤形成的最简单氢化物的稳定性高 |
| B.元素最高正价与最低负价绝对值相等的元素一定处于第ⅣA族 |
| C.第5周期第ⅦA族元素的原子序数为53 |
| D.周期表中当某元素的周期序数大于其主族序数时,该元素可能属于金属或非金属 |
(5)BrCl属于卤素互化物,性质与Cl2相似。写出BrCl与氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
解题方法
7 . 回答下列问题。
(1)氮元素在元素周期表中的位置是第___________ 周期,第___________ 族。
(2) 是元素周期表中第
是元素周期表中第___________ 号元素。
(3) 的M能层电子排布式是
的M能层电子排布式是___________ ,价层电子排布图是___________ ,原子结构示意图是___________ 。
(1)氮元素在元素周期表中的位置是第
(2)
 是元素周期表中第
是元素周期表中第(3)
 的M能层电子排布式是
的M能层电子排布式是
您最近一年使用:0次
8 . 请按照要求填写:
(1)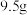 某二价金属氯化物
某二价金属氯化物 中含有
中含有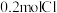 ,则
,则 的摩尔质量是
的摩尔质量是___________ 。
(2)除去镁粉中的铝粉,所选试剂为___________ ,相关的离子反应方程式为___________ 。
(3)配平离子方程式:___________ 。
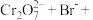 ___________=___________
___________=___________ ___________
___________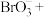 ___________
___________
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂 的一种制备方法如下。
的一种制备方法如下。___________ ;
② 的结构式是
的结构式是___________ ;
③反应Ⅰ的离子方程式是___________ 。
(1)
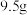 某二价金属氯化物
某二价金属氯化物 中含有
中含有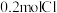 ,则
,则 的摩尔质量是
的摩尔质量是(2)除去镁粉中的铝粉,所选试剂为
(3)配平离子方程式:
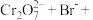 ___________=___________
___________=___________ ___________
___________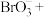 ___________
___________
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂
 的一种制备方法如下。
的一种制备方法如下。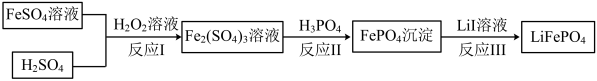
②
 的结构式是
的结构式是③反应Ⅰ的离子方程式是
您最近一年使用:0次
9 . 下表列出了A~R九种元素在元素周期表中的位置:
(1)A的最高价氧化物对应水化物的电子式___________ ,核内有10个中子的F的核素表示为___________ ;H的最高价氧化物对应水化物的化学式___________ ,以上元素其中化学性质最不活泼的是___________ (填元素符号)。
(2)A、B、C三种元素按原子半径由大到小的顺序排列为___________ (用元素符号表示)。
(3)E、F元素最简单氢化物中稳定性最强的化学式是___________ ,该氢化物在常温下跟A发生反应的化学方程式是___________ 。
(4)D、B两种元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(5)关于元素周期表、周期律,下列说法正确的是___________(填字号)
| 周期 | IA | IIA | IIIA | IV A | VA | VIA | VIIA | 0 | |
| 族 | |||||||||
| 2 | E | F | |||||||
| 3 | A | C | D | G | H | R | |||
| 4 | B |
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
(3)E、F元素最简单氢化物中稳定性最强的化学式是
(4)D、B两种元素的最高价氧化物对应的水化物发生反应的离子方程式是
(5)关于元素周期表、周期律,下列说法正确的是___________(填字号)
| A.在金属和非金属分界处可以找到半导体材料 |
| B.在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素 |
| C.通常农药所含有的元素位于元素周期表左下方区域 |
| D.稀有气体原子都满足8电子稳定结构 |
您最近一年使用:0次
2024-04-15更新
|
73次组卷
|
2卷引用:云南省腾冲市第八中学2023-2024学年高一下学期开学化学试题
10 . 下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
(1)⑧的最高价氧化物的水化物的化学式是___________ 。
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序___________ (写离子符号)。
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是___________ (填化学式)。
(4)⑤和⑦的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(5)晒(Se)位于第四周期,与④同主族。下列推断正确的是___________ 。
a. 只具有还原性
只具有还原性
b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比 强
强
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是
(4)⑤和⑦的最高价氧化物的水化物之间发生反应的离子方程式为
(5)晒(Se)位于第四周期,与④同主族。下列推断正确的是
a.
 只具有还原性
只具有还原性 b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比
 强
强
您最近一年使用:0次
2024-04-13更新
|
126次组卷
|
2卷引用:安徽省舒城育才学校2023-2024学年高一上学期期末考试化学试题



