名校
解题方法
1 . 海洋是资源的宝库,蕴藏着丰富的氯、溴、碘等元素。氯、溴、碘是典型的非金属元素,都能与大多数金属化合生成盐,故统称为卤素;卤素单质都具有氧化性。
(1)氯在元素周期表中的位置___________
(2)氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2.写出该电解过程的离子方程式___________
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为: 。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式
。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式___________ 。
(4)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应: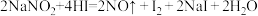
Ⅰ.上述反应的还原剂是___________
Ⅱ.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有___________ (填字母)。
A.③⑤ B.①②⑤ C.①②④
Ⅲ.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是___________ 。(填字母)
A.NaCl B. C.
C. D.浓
D.浓
(1)氯在元素周期表中的位置
(2)氯气是重要的化工产品,工业可以由电解氯化钠溶液得到,同时还生成NaOH和H2.写出该电解过程的离子方程式
(3)氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱顺序为:
 。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式
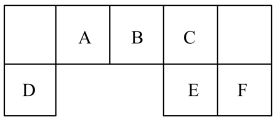
。试写出:在NaBr和KSCN的混合溶液中滴加少量(CN)2,请写出发生反应的离子方程式(4)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:
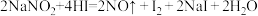
Ⅰ.上述反应的还原剂是
Ⅱ.根据上述反应,鉴别某白色固体是NaNO2还是NaCl。可选用的物质有:①水 ②淀粉碘化钾试纸 ③淀粉溶液 ④白酒 ⑤食醋(稀的醋酸溶液),你认为必须选用的物质有
A.③⑤ B.①②⑤ C.①②④
Ⅲ.某厂废液中,含有2%~5%的NaNO2直接排放会造成污染,下列试剂能使NaNO2转化为N2防止污染的是
A.NaCl B.
 C.
C. D.浓
D.浓
您最近一年使用:0次
名校
2 . 短周期主族元素A、B、C、D、E、F在元素周期表中的位置如下图所示,其中元素F是同周期元素原子半径最小的;请回答下列问题:
(1)F在周期表中的位置___________ ;
(2)比较B、C、D元素简单离子半径的大小顺序___________ (填写离子符号);
(3)F的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________ ;
(4)要比较元素E与F非金属性的强弱,正确合理的实验操作与现象是______________________ ;
(5)用高能射线照射液态水时,一个水分子能释放一个电子,同时产生一种具有较强氧化性阳离子,该阳离子中存在的化学键有______ ,并写出该阳离子与E的氢化物的水溶液反应的离子方程式________________ 。

(1)F在周期表中的位置
(2)比较B、C、D元素简单离子半径的大小顺序
(3)F的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为
(4)要比较元素E与F非金属性的强弱,正确合理的实验操作与现象是
(5)用高能射线照射液态水时,一个水分子能释放一个电子,同时产生一种具有较强氧化性阳离子,该阳离子中存在的化学键有
您最近一年使用:0次
名校
3 . Ⅰ.铁原子结构示意图及元素周期表中铁元素的部分信息如图。
(1)下列有关说法正确的是_______ 。
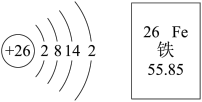
a.铁元素位于元素周期表的第六周期 b.Fe3+的电子数为24
c.1 mol铁的质量为55.85 g e.加热下,铁与硫反应生成Fe2S3
Ⅱ.碱式氯化铜[CuaClb(OH)c∙xH2O]制备需要的CuCl2可用Fe3+作催化剂得到,其催化原理如图所示。

(2)上述转化过程中Cu2+与O2个数比______ 。
(3)图中M、N分别为______ ,______ 。
(4)a、b、c之间的等式关系式为_________ 。
(5)N参加的反应离子方程式为_________ 。
(1)下列有关说法正确的是
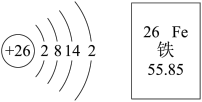
a.铁元素位于元素周期表的第六周期 b.Fe3+的电子数为24
c.1 mol铁的质量为55.85 g e.加热下,铁与硫反应生成Fe2S3
Ⅱ.碱式氯化铜[CuaClb(OH)c∙xH2O]制备需要的CuCl2可用Fe3+作催化剂得到,其催化原理如图所示。

(2)上述转化过程中Cu2+与O2个数比
(3)图中M、N分别为
(4)a、b、c之间的等式关系式为
(5)N参加的反应离子方程式为
您最近一年使用:0次
名校
4 . 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
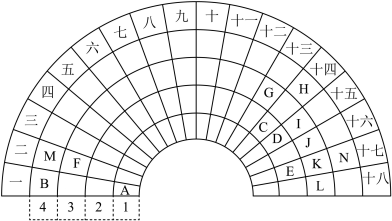
(1)表中用字母标出的14种元素中,化学性质最不活泼的是___________ (用元素符号表示,下同);常温常压下其单质为液态的非金属元素是___________ 。
(2)N的基态原子的价层电子排布式为___________ ,属于___________ 区元素。
(3)这14种元素中第一电离能最小的是___________ (用元素符号表示,下同),电负性最大的是___________ 。
(4)这些元素中的第三周期主族元素中,原子半径最小的是___________ (填元素符号),简单离子半径最小的是___________ 。(填离子符号)

(1)表中用字母标出的14种元素中,化学性质最不活泼的是
(2)N的基态原子的价层电子排布式为
(3)这14种元素中第一电离能最小的是
(4)这些元素中的第三周期主族元素中,原子半径最小的是
您最近一年使用:0次
名校
解题方法
5 . 若某非金属元素X的最高价氧化物对应的水化物的化学式为HnXOm,则X元素的族序数为______ ,它的最高价氧化物的化学式为______ ,氢化物的化学式为______ 。
您最近一年使用:0次
6 . 元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①~⑧分别代表一种元素。回答下列问题:
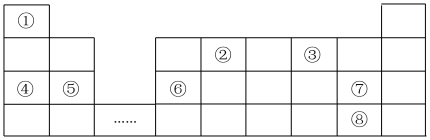
(1)元素①含2个中子的核素为_____ (填符号)。
(2)元素②、③形成的化合物_____ (填“属于”或“不属于”)电解质。
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为_____ (用离子符号填空)。
(4)元素④、⑤、⑥金属性由强到弱的顺序为_____ ,元素④和⑥的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为_____ ,该反应的离子方程式为_____ 。

(1)元素①含2个中子的核素为
(2)元素②、③形成的化合物
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为
(4)元素④、⑤、⑥金属性由强到弱的顺序为
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为
您最近一年使用:0次
名校
7 . 现代化学在材料、资源、能源、环境、医药、信息技术等领域均有重大应用。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:
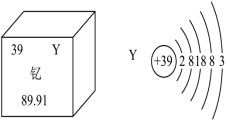
(1)钇原子核内有___________ 个质子,图中89.91表示的是___________ 。
(2)钇元素形成氧化物的化学式是___________ 。
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态
(3)上述物质中属于电解质的是___________ 。(填序号)
(4)属于非电解质的是___________ 。(填序号)
(5)能导电的纯净物是___________ 。(填序号)
(6)写出⑦在水中的电离方程式___________ 。
(7)写出①和⑥的反应方程式___________ 。
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式___________ 。
I.新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:

(1)钇原子核内有
(2)钇元素形成氧化物的化学式是
II.电解质是维持人体生理活动的基础之一、请回答下列问题:
①CO2 ②Al ③乙醇 ④Fe(OH)3胶体 ⑤熔融BaSO4 ⑥KOH溶液 ⑦固态

(3)上述物质中属于电解质的是
(4)属于非电解质的是
(5)能导电的纯净物是
(6)写出⑦在水中的电离方程式
(7)写出①和⑥的反应方程式
(8)请写出实验室中制备Fe(OH)3胶体的化学反应方程式
您最近一年使用:0次
解题方法
8 . 下表列出了A~R9种元素在周期表中的位置:
请回答下列问题。
(1)这些元素分别为:A___________ ,B___________ ,C___________ ,D___________ ,E___________ ,F___________ ,G___________ ,R___________ ,其中化学性质最不活泼的是___________ (用元素符号表示)。
(2)画出G的原子结构示意图___________ 。
(3)元素周期表共有___________ 个周期___________ 个族,18纵行元素化合价通常表现为___________ 价所以称为0族元素,又叫惰性气体元素。A位于___________ 周期___________ 族
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(1)这些元素分别为:A
(2)画出G的原子结构示意图
(3)元素周期表共有
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈
您最近一年使用:0次
2024-01-05更新
|
150次组卷
|
2卷引用:贵州省清镇市博雅实验学校2023-2024学年高一上学期第四次月考化学试卷
名校
9 . 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图___________ 。
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是___________ 。
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为___________ 。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为
您最近一年使用:0次
名校
10 . 肼(N2H4)是重要的化工原料,能与水、乙醇等混溶;它是一种二元弱碱,在水中的电离方式与氨相似,室温下电离常数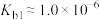 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。
(1)写出N元素在元素周期表中的位置___________ 。
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式___________ 。
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步: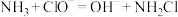
①写出第二步反应的离子方程式___________ 。
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)___________ 。
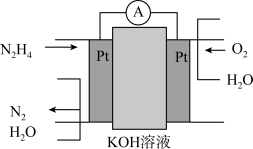
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________ 。
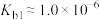 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。(1)写出N元素在元素周期表中的位置
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步:
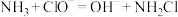
①写出第二步反应的离子方程式
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为

您最近一年使用:0次



