名校
1 . 。部分实验中涉及到的物质的熔沸点如表所示。
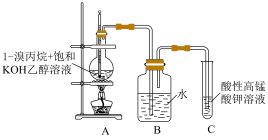
完成下列填空:
(1)写出1-溴丙烷制备丙烯的化学方程式___________ 。
(2)A装置中的导气管较长,可以起到使反应物________ 的作用。若导管的长度太长,C中酸性高锰酸钾溶液褪色时间会延后,可能的原因是________ 。B装置是洗气装置,可以除去从A中导出气体中的杂质_________ 、_______ 。
(3)该实验小组查阅了相关资料后发现,1-溴丙烷制备丙烯的反应需要在65℃以上才能发生。为了更好地达到控温的效果,可以采取_____ 的方式进行加热,这种加热方式除了方便控温外这还具有______ 的优势。加热时将温度控制在65-70℃之间,请结合表中数据阐释选择该温度范围的原因___________ 。
(4)溶液的碱性越强,该反应越容易发生。NaOH与KOH都是常见的水溶液中的强碱,但是经实验测定NaOH在乙醇中的碱性弱于KOH在乙醇中的碱性,这是因为根据元素周期律,Na的______ (选填“金属性”或“非金属性”)______ (选填“强于”或“弱于”)K。结合题目及题干信息,阐释实验采用饱和的KOH乙醇溶液而不采用饱和的NaOH乙醇溶液的原因___________ 。
(5)可以采用溴的四氯化碳溶液吸收生成的丙烯,写出溴的四氯化碳溶液与丙烯反应的化学方程式_______ 。若反应前量取了9.1mL的1-溴丙烷,充分反应后溴的四氯化碳溶液质量增加了0.336g,则丙烯的产率为______ ,请提出一个产率偏低的可能原因___________ 。
| 熔点(℃) | 沸点(℃) | 密度(g·ml-1) | |
| 1-溴丙烷 | -110 | 71 | 1.354 |
| 乙醇 | -114 | 78 | 0.79 |
| 丙烯 | -185 | -47 | |
| NaBr | 755 | 1390 | |
| 饱和KOH乙醇溶液 | 116 | ||
| 饱和NaOH乙醇溶液 | 85 |

完成下列填空:
(1)写出1-溴丙烷制备丙烯的化学方程式
(2)A装置中的导气管较长,可以起到使反应物
(3)该实验小组查阅了相关资料后发现,1-溴丙烷制备丙烯的反应需要在65℃以上才能发生。为了更好地达到控温的效果,可以采取
(4)溶液的碱性越强,该反应越容易发生。NaOH与KOH都是常见的水溶液中的强碱,但是经实验测定NaOH在乙醇中的碱性弱于KOH在乙醇中的碱性,这是因为根据元素周期律,Na的
(5)可以采用溴的四氯化碳溶液吸收生成的丙烯,写出溴的四氯化碳溶液与丙烯反应的化学方程式
您最近一年使用:0次
2 . 下表是元素周期表的一部分,请按要求回答问题:
请回答下列问题:
(1)元素③周期表中的位置是___________ 。
(2)可利用一个化学反应比较⑥⑦非金属性的强弱,写出该反应的化学方程式___________ 。
(3)②和④可形成一种化合物,能作呼吸面具中的供氧剂的。写出该化合物的电子式___________ 。
(4)元素④的最高价氧化物对应水化物中含有的化学键类型为___________ 。
(5)比较元素⑤⑥的最高价氧化物对应的水化物的酸性强弱___________ (用化学式表示)。
(6)比较元素③和④的简单离子半径大小___________ (用离子符号表示)。
(7)锗为第四周期与硅同主族,根据元素周期率推测其单质、化合物的性质正确的是___________。(填字母)
| ① | ② | ③ | |||||
| ④ | ⑤ | ⑥ | ⑦ | ||||
| ⑧ | |||||||
(1)元素③周期表中的位置是
(2)可利用一个化学反应比较⑥⑦非金属性的强弱,写出该反应的化学方程式
(3)②和④可形成一种化合物,能作呼吸面具中的供氧剂的。写出该化合物的电子式
(4)元素④的最高价氧化物对应水化物中含有的化学键类型为
(5)比较元素⑤⑥的最高价氧化物对应的水化物的酸性强弱
(6)比较元素③和④的简单离子半径大小
(7)锗为第四周期与硅同主族,根据元素周期率推测其单质、化合物的性质正确的是___________。(填字母)
| A.锗的金属性比⑧强 | B.锗的原子半径比①大 |
| C.锗的单质可用于制半导体 | D.锗的最高正价为+3 |
您最近一年使用:0次
名校
解题方法
3 . 下图是元素周期表的一部分,根据①~⑨在周期表中的位置按题目要求回答:
(1)在元素①~⑨中,金属性最强的元素是___________ (填元素符号)。
(2)画出元素④的原子结构示意图___________ 。
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,甲物质的电子式为___________ ,其化学键类型为___________ 共价键(填“极性”或“非极性”)。
(4)元素③⑤对应的最高价氧化物的水化物,它们相互之间能发生反应的离子方程式为___________ 。
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程___________ 。
(6)②与⑥分别形成的氢化物中,稳定性较高的是___________ (填化学式),⑥和⑦的最高价氧化物的水化物酸性___________ 
___________ (填化学式)。
| 族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ | ||||||
(2)画出元素④的原子结构示意图
(3)①与②形成的一种化合物甲,甲在大气含量过高会产生温室效应,甲物质的电子式为
(4)元素③⑤对应的最高价氧化物的水化物,它们相互之间能发生反应的离子方程式为
(5)元素⑦和⑨形成的化合物乙,请用电子式表示物质乙的形成过程
(6)②与⑥分别形成的氢化物中,稳定性较高的是

您最近一年使用:0次
2023-04-07更新
|
231次组卷
|
2卷引用:天津市东丽区2021-2022学年高一上学期期末质量检测化学试题
4 . 下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题:
(1)①~⑩中,金属性最强的元素的最高价氧化物的水化物是_______ (填化学式),非金属性最强的元素是_______ (填元素符号),最高价氧化物对应的水化物酸性最强的是_______ (填化学式)。
(2)①、③、⑧的简单离子,其半径由大到小的分别为_______ (填离子符号)。
(3)④、⑦的最高价氧化物的水化物,其酸性较弱的是_______ (填化学式)。
(4)④、⑥、⑦元素的非金属性由强到弱的分别为:_______ (填元素符号)。
(5)在短周期的元素中,最高价氧化物对应的水化物中,碱性最强的是_______ (填化学式),该碱与⑨的单质反应的离子方程式为_______ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑥ | ④ | ⑨ | ||
| 4 | ② | |||||||
(2)①、③、⑧的简单离子,其半径由大到小的分别为
(3)④、⑦的最高价氧化物的水化物,其酸性较弱的是
(4)④、⑥、⑦元素的非金属性由强到弱的分别为:
(5)在短周期的元素中,最高价氧化物对应的水化物中,碱性最强的是
您最近一年使用:0次
名校
5 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表是5种元素的相关信息,W、X都位于第三周期。
(1)W的最高价氧化物对应的水化物的化学式是_______ 。
(2)元素W和X可以形成化合物WX,是_______ (填“离子”“共价”)化合物。
(3)比较W、X、Y的离子半径大小_______ (用离子符号表示)。
(4)X单质与水反应的离子方程式是_______ 。
(5)比较X和Y最高价氧化物的水化物的碱性_______ (用化学式表示);比较W和Z离子的还原性:_______ (用离子符号表示)。
(6)下列对于Z及其化合物的推断中,正确的是_______ (填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应
| 元素 | 信息 |
| W | 最高化合价为 价 价 |
| X | 最高价氧化物对应的水化物在其所在周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃观察)火焰呈紫色 |
| Z | 原子结构示意图为: |
(2)元素W和X可以形成化合物WX,是
(3)比较W、X、Y的离子半径大小
(4)X单质与水反应的离子方程式是
(5)比较X和Y最高价氧化物的水化物的碱性
(6)下列对于Z及其化合物的推断中,正确的是
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应
您最近一年使用:0次
名校
解题方法
6 . 元素周期表是许多科学家共同努力的结晶。如图是元素周期表的一部分。
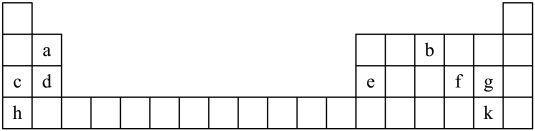
请回答下列问题:
(1)a元素的名称是_______ ,f在周期表中的位置________ 。
(2)e、f、g三种元素的简单离子半径由大到小的顺序是__________ (用元素符号表示)。
(3)f、g的最高价氧化物的水化物的酸性:______________ >_______________ (填化学式)
(4)e的最高价氧化物与h的最高价氧化物对应的水化物反应的离子方程式为______________ 。
(5)b的简单氢化物沸点高于同主族相邻周期元素的简单氢化物,其原因是______________ 。
(6)写出c单质在空气中燃烧产物的电子式______________ 。
(7)用电子式表示由d和g两种元素形成的原子个数比为1:2的化合物的形成过程:_______

请回答下列问题:
(1)a元素的名称是
(2)e、f、g三种元素的简单离子半径由大到小的顺序是
(3)f、g的最高价氧化物的水化物的酸性:
(4)e的最高价氧化物与h的最高价氧化物对应的水化物反应的离子方程式为
(5)b的简单氢化物沸点高于同主族相邻周期元素的简单氢化物,其原因是
(6)写出c单质在空气中燃烧产物的电子式
(7)用电子式表示由d和g两种元素形成的原子个数比为1:2的化合物的形成过程:
您最近一年使用:0次
7 . 下表为元素周期表的一部分,请参照给定元素的位置,回答下列问题:
(1)元素④、⑤、⑥的原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为_______ 。(用化学式表示)
(3)碱性强弱比较:元素⑤的氢氧化物_______ ⑥的氢氧化物(用<、=、>填空);两者相互反应的离子方程式为_______ 。
(4)由元素①⑧形成的化合物A和由元素④⑤⑧的化合物B,可相互反应产生黄绿色气体单质,该反应的离子方程式为_______ ;该黄绿色气体单质会使得湿润淀粉碘化钾试纸变蓝色,表明生成了碘单质(I2),由此推测这两种元素的气态氢化物的稳定性强弱顺序为:_______ 。(用化学式表示)
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为
(3)碱性强弱比较:元素⑤的氢氧化物
(4)由元素①⑧形成的化合物A和由元素④⑤⑧的化合物B,可相互反应产生黄绿色气体单质,该反应的离子方程式为
您最近一年使用:0次
2023-01-10更新
|
68次组卷
|
2卷引用:四川省天府新区太平中学2022-2023学年高一上学期期末考试化学试题
解题方法
8 . 下表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑧的元素符号分别是_______ 和_______ 。
(2)表中最活泼的金属是_______ ,非金属性最强的元素是_______ (填写元素符号)。
(3)表中能形成两性氢氧化物的元素是_______ ,分别写出该元素的氢氧化物与⑥最高价氧化物的水化物反应的化学方程式:_______ 。
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:
您最近一年使用:0次
9 . 已知:X、Y、Z、W是1~18号元素中的四种常见元素,其相关信息见下表:
请根据表中相关信息,回答下列问题:
(1)Y位于元素周期表第_______ 周期第_______ 族,Y和Z的最高价氧化物对应水化物的酸性较强的是_______ (填化学式)。
(2)Z的简单阴离子的电子式为_______ 。
(3)请用电子式描述W与X形成碱性氧化物的过程:_______ 。
(4)Y的氧化物与气态氢化物可发生归中反应,请写出相关化学反应方程式:_______ 。
| 元素 | 相关信息 |
| X | X元素原子的最外层电子数是次外层电子数的3倍 |
| Y | Y元素的最高正价与最低负价的代数和为4 |
| Z | Z和Y同周期,Z的非金属性大于Y |
| W | W的一种核素的质量数为23,中子数为12 |
(1)Y位于元素周期表第
(2)Z的简单阴离子的电子式为
(3)请用电子式描述W与X形成碱性氧化物的过程:
(4)Y的氧化物与气态氢化物可发生归中反应,请写出相关化学反应方程式:
您最近一年使用:0次
22-23高一上·全国·课时练习
10 . 下图是元素①~⑤在元素周期表中的位置。
(1)②在周期表中的位置是第_______ 周期第_______ 族,其淡黄色氧化物与CO2反应的化学方程式是_______ 。
(2)③的一种核素的中子数是10,表示该核素的符号是_______ 。
(3)非金属性:④_______ ⑤(填“>”或“<”),从原子结构角度解释其原因:_______ 。
(4)下列关于①的说法正确的是_______ 。
a.原子结构示意图为
b.其单质可以和水反应生成H2
c.在同主族的元素中,①的金属性最强
| ① | ③ | ④ | |||||
| ② | ⑤ |
(2)③的一种核素的中子数是10,表示该核素的符号是
(3)非金属性:④
(4)下列关于①的说法正确的是
a.原子结构示意图为

b.其单质可以和水反应生成H2
c.在同主族的元素中,①的金属性最强
您最近一年使用:0次



