名校
1 . 2017年5月9日,我国正式向社会发布113号、115号、117号、118号元素的中文名称,至此,全部完成了1~118号元素的中文命名。已知115号元素的中文名为“镆”,它有多种原子,如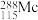 、
、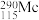 等。下列说法不正确的是
等。下列说法不正确的是
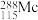 、
、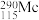 等。下列说法不正确的是
等。下列说法不正确的是A.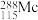 和 和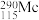 的化学性质几乎相同 的化学性质几乎相同 |
B. 位于周期表的第七周期第VA族 位于周期表的第七周期第VA族 |
C.在镆原子中,最后填入电子的轨道能级符号是f,故 位于周期表中的f区 位于周期表中的f区 |
| D.在周期表中,假设第八周期按照现有规则填满,则115号元素正下方的将是165号元素 |
您最近一年使用:0次
2024-02-17更新
|
161次组卷
|
3卷引用:湖北省荆州市荆州中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 如图所示的两种化合物可应用于阻燃材料和生物材料的合成,其中W、X、Y、Z为原子序数依次增大的短周期元素,Y与W同主族。下列说法正确的是


| A.X的最高正价为+7 |
| B.原子半径:Y<Z |
| C.简单氢化物的沸点:W>X |
| D.H与W、X三种元素可形成离子化合物 |
您最近一年使用:0次
3 . 五种短周期元素X、Y、Z、W、M的原子序数依次增大且位于不同的主族,Y的最外层电子数是次外层的2倍,M的原子序数等于Y和W的原子序数之和,只有Y、Z、W同周期。下列说法错误的是
A.简单离子半径: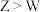 | B.X、Y、W三种元素可形成多种化合物 |
| C.M的最高价氧化物对应的水化物为强酸 | D.Y、Z、M均可与X形成电子数相等的分子 |
您最近一年使用:0次
2022-05-21更新
|
235次组卷
|
2卷引用:湖北省新高考部分校2021-2022学年高三下学期5月质量检测化学试题
名校
4 . 锗和硅同一主族,也是重要的半导体材料,应用于航空航天测控、光纤通讯等领域。一种以铅锌矿含锗烟尘(主要含GeO2、ZnO 、SiO2)为原料制备GeO2的工艺如下:

已知:①GeO2为两性氧化物;
②H4SiO4和H2GeO3在高酸度时易聚合形成多聚硅酸和多聚锗酸;
③GeCl4易水解。
试回答下列问题:
(1)锗的原子序数为32 ,在元素周期表中的位置为___________ 。
(2)第①步为提高稀硫酸的浸出效果可以采取的措施有___________ (任写一条)。
(3)第①步所得滤液中锗以Ge4+存在,写出其水解的离子方程式___________ 。
(4)测得锗的浸出率(%)与硫酸的物质的量浓度(mol/L)的关系如图所示:

浸出率高时的硫酸浓度为___________ mol/L,的原因是___________ 。
(5)工业上与蒸馏操作相关的设备有___________(填选项)。
(6)第⑤步发生的化学反应方程式为___________ 。

已知:①GeO2为两性氧化物;
②H4SiO4和H2GeO3在高酸度时易聚合形成多聚硅酸和多聚锗酸;
③GeCl4易水解。
试回答下列问题:
(1)锗的原子序数为32 ,在元素周期表中的位置为
(2)第①步为提高稀硫酸的浸出效果可以采取的措施有
(3)第①步所得滤液中锗以Ge4+存在,写出其水解的离子方程式
(4)测得锗的浸出率(%)与硫酸的物质的量浓度(mol/L)的关系如图所示:

浸出率高时的硫酸浓度为
(5)工业上与蒸馏操作相关的设备有___________(填选项)。
| A.蒸馏釜 | B.离心萃取机 | C.冷凝塔 | D.加压过滤机 |
您最近一年使用:0次
2022-04-01更新
|
368次组卷
|
4卷引用:湖北省襄阳市第五中学2022 届高三适应性考试(三)化学试题
湖北省襄阳市第五中学2022 届高三适应性考试(三)化学试题湖北省襄阳市第五中学2022届高三下学期5月适应性考试(三)化学试题湖南省衡阳市2022届高三下学期联考(一)(3月一模)化学试题(已下线)化学-2022年高考押题预测卷03(山东卷)
5 . 下列关于元素周期表的说法错误的是
| A.共有7个周期、16个族 |
| B.元素原子的电子层数等于其所在周期的周期序数 |
| C.元素原子的最外层电子数等于其所在族的序数 |
| D.元素周期表是元素按原子序数大小排列而成的 |
您最近一年使用:0次
名校
6 . 我国科学家使用某种电解液提高了水系锌锰电池的性能。该电解液阴离子结构如图所示,其中 、
、 、
、 、
、 为原子半径依次增大的短周期元素,且最外层电子数之和为23.下列说法正确的是
为原子半径依次增大的短周期元素,且最外层电子数之和为23.下列说法正确的是
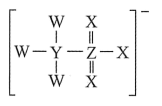
 、
、 、
、 、
、 为原子半径依次增大的短周期元素,且最外层电子数之和为23.下列说法正确的是
为原子半径依次增大的短周期元素,且最外层电子数之和为23.下列说法正确的是 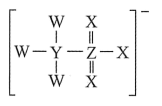
A.元素的非金属性: |
B.该离子中 都满足8电子稳定结构 都满足8电子稳定结构 |
C.最高价氧化物水化物的酸性 强于 强于 |
D. 单质不能通过置换反应生成 单质不能通过置换反应生成 单质 单质 |
您最近一年使用:0次
2021-04-24更新
|
328次组卷
|
3卷引用:湖北省武汉市2020-2021学年高三下学期4月质量检测化学试题
解题方法
7 . 下列有关碱金属元素、卤素结构和性质的描述正确的有
①卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的主要原因是随着核电荷数增加,电子层数增多,原子半径增大
②F、Cl、Br、I的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
④根据同族元素性质的递变规律推测,At2与H2化合较难,砹化银也难溶于水
⑤根据Cl、Br、I的非金属性递减,可推出HCl、HBr、HI的酸性依次增强,而热稳定性依次减弱
⑥碱金属都应保存在煤油中
①卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的主要原因是随着核电荷数增加,电子层数增多,原子半径增大
②F、Cl、Br、I的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
④根据同族元素性质的递变规律推测,At2与H2化合较难,砹化银也难溶于水
⑤根据Cl、Br、I的非金属性递减,可推出HCl、HBr、HI的酸性依次增强,而热稳定性依次减弱
⑥碱金属都应保存在煤油中
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
解题方法
8 . 我国拥有自主知识产权的铷(Rb)原子钟,每3000万年误差仅1秒。Rb是第五周期第ⅠA族元素,下列关于37Rb的说法不正确的是( )
A.中子数为50的Rb的核素: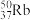 |
| B.元素的金属性:Rb>K |
| C.与同周期元素53I的原子半径比:I<Rb |
| D.最高价氧化物对应的水化物的碱性:KOH<RbOH |
您最近一年使用:0次
名校
解题方法
9 . 科学家预测,月球的土壤中吸附着数百万吨  e,100 吨
e,100 吨  e 核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是
e 核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是
 e,100 吨
e,100 吨  e 核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是
e 核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是A. 的最外层电子数为 2,具有较强的金属性 的最外层电子数为 2,具有较强的金属性 |
B. e位于周期表第二周期第ⅡA 族 e位于周期表第二周期第ⅡA 族 |
| C.其原子核中质子数为 2、中子数为 1 |
| D.核聚变是化学反应 |
您最近一年使用:0次
2020-08-28更新
|
329次组卷
|
5卷引用:湖北省武汉市第三中学2019-2020学年高一下学期期中考试化学试题
10 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于____ 区。
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素的中文名称,分别为“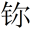 (nǐ)”“镆(mò)”“
(nǐ)”“镆(mò)”“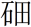 (tián)”“
(tián)”“ (ào)”,则下列说法正确的是
(ào)”,则下列说法正确的是___ (填字母序号)。
a.115号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的___ ,该元素M能层上具有____ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D___ E(填“>”“<”或“=”)。
②气态氢化物的沸点:B___ F(填“>”“<”或“=”),理由是___ 。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素的中文名称,分别为“
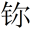 (nǐ)”“镆(mò)”“
(nǐ)”“镆(mò)”“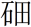 (tián)”“
(tián)”“ (ào)”,则下列说法正确的是
(ào)”,则下列说法正确的是a.115号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次



