1 . W、X、Y、Z是元素周期表中的四种短周期元素,其相关信息及原子半径与原子序数的关系如表所示。请回答下列问题:
(1)W在元素周期表中的位置是___ ,W与X形成的含有共价键的常见化合物的电子式为___ 。
(2)X、Z的简单离子的半径大小为__ (用离子符号表示)。
(3)Y的最高价氧化物与单质碳在高温下反应的化学方程式为__ ;Z的简单氢化物与X的最高价氧化物对应的水化物反应的离子方程式为__ 。
(4)最高价氧化物对应水化物的酸性:Y__ (填“大于”或“小于”,下同)磷;第一电离能:Y__ 磷。
| 元素 | 相关信息 | 原子半径与原子序数的关系 |
| W | 其一种核素的质量数为18,中子数为10 |  |
| X | 其原子与电子排布式为1s22s22p6的原子的核外电子数相差1 | |
| Y | 其单质是一种常见的半导体材料 | |
| Z | 电负性在同周期元素中最大 |
(2)X、Z的简单离子的半径大小为
(3)Y的最高价氧化物与单质碳在高温下反应的化学方程式为
(4)最高价氧化物对应水化物的酸性:Y
您最近一年使用:0次
2021-04-14更新
|
520次组卷
|
2卷引用:辽宁省阜新市第二高级中学2020-2021学年高二下学期第一次月考化学试题
名校
2 . 短周期元素M的原子核外有n个电子层上排布了电子,最外层电子数为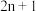 .下列有关M的说法中,不一定正确的是
.下列有关M的说法中,不一定正确的是
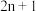 .下列有关M的说法中,不一定正确的是
.下列有关M的说法中,不一定正确的是| A.M是非金属元素 |
| B.M的气态氢化物是电解质 |
| C.M的常见单质在常温下为气态 |
| D.M的最高价氧化物对应的水化物是强酸 |
您最近一年使用:0次
2021-04-14更新
|
578次组卷
|
3卷引用:河北省石家庄市第二中学2020-2021学年高二4月月考化学试题
20-21高二·全国·课时练习
3 . A、B、C都是短周期元素。B、C的离子核外电子排布相同,组成B2C型离子化合物。A、B元素的化合价相同,A、C元素组成的化合物中,A占11.1%,在标准状况下,0.04 mol B元素的单质与水完全反应放出448 mL H2。
(1)写出各元素的符号:A是______ ,B是______ ,C是______ 。
(2)写出A元素组成的单质的电子式:______ ,分子中的化学键有______ 。
(3)写出A和C组成的化合物的电子式:______ 。
(4)A、C还可以形成另一种化合物,该化合物是一种氧化剂,其溶液有弱酸性,试写出其电子式:______ 。分子中的化学键有______ 共价键和______ 共价键。
(1)写出各元素的符号:A是
(2)写出A元素组成的单质的电子式:
(3)写出A和C组成的化合物的电子式:
(4)A、C还可以形成另一种化合物,该化合物是一种氧化剂,其溶液有弱酸性,试写出其电子式:
您最近一年使用:0次
20-21高二·全国·课时练习
4 . 元素X和Y属于同一主族。负二价的元素X和氢的化合物在通常状况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%。
(1)确定X、Y两种元素在周期表中的位置分别为________________ 、________________ 。
(2)在元素X和元素Y两种元素形成的化合物中,写出X质量分数为50%的化合物的化学式_______ ;该分子的中心原子以_______ 杂化,分子构型为_______ 。
(3)写出X的质量分数为60%的化合物的化学式________________ ;该分子的中心原子以________ 杂化,分子构型为________ 。
(4)由氢元素与X元素形成的化合物中,含有非极性键的是________ (写分子式),分子构型为V形的是________ (写分子式)。
(1)确定X、Y两种元素在周期表中的位置分别为
(2)在元素X和元素Y两种元素形成的化合物中,写出X质量分数为50%的化合物的化学式
(3)写出X的质量分数为60%的化合物的化学式
(4)由氢元素与X元素形成的化合物中,含有非极性键的是
您最近一年使用:0次
20-21高二·全国·课时练习
解题方法
5 . 处于同一周期的A、B、C、D四种短周期元素,其气态原子获得一个电子所放出的能量A>B>C>D.下列关于A、B、C、D四种元素的说法中,可能正确的是
| A.元素的非金属性依次增强 |
| B.元素的电负性依次减小 |
| C.元素的第一电离能依次增大 |
| D.最高价的大小关系是A<B<C<D |
您最近一年使用:0次
20-21高二·全国·单元测试
6 . 短周期元素W、X、Y、Z的原子序数依次增大。n、p、q、s是由这些元素组成的二元化合物,常温常压下s为液体,其余均为无色气体。r是元素X的单质,是空气的主要成分之一,n物质能使湿润的红色石蕊试纸变蓝,单质m常用于自来水的杀菌消毒。上述物质的转化关系如图所示。下列说法错误的是
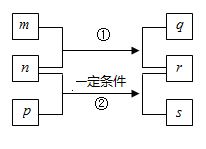

| A.原子半径:W<Y<X<Z |
| B.非金属性:X<Y<Z |
| C.配平反应①后氧化剂和氧化产物的物质的量之比为1:3 |
| D.W分别与X、Y可形成相同电子的共价化合物 |
您最近一年使用:0次
20-21高二·全国·课时练习
解题方法
7 . 主族元素A、B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的价电子数都是1,C原子最外层电子数比B原子少2个,且最外层电子数是次外层电子数的2倍。A、B的单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下为液体。此液体与D单质能剧烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。试回答下列问题:
(1)写出元素符号:B___________ ,D___________ 。
(2)写出元素原子的价电子排布:A___________ ,C___________ 。
(3)B与C在高温下完全反应后的生成物的化学式为___________ ,它是由___________ (填“极性”或“非极性”)键形成的___________ 分子,分子的空间构型呈___________ 。
(4)A与B的单质以体积比2∶1形成的化合物的中心原子的杂化方式为___________ ,分子的空间构型呈___________ 。
(1)写出元素符号:B
(2)写出元素原子的价电子排布:A
(3)B与C在高温下完全反应后的生成物的化学式为
(4)A与B的单质以体积比2∶1形成的化合物的中心原子的杂化方式为
您最近一年使用:0次
20-21高二·全国·单元测试
解题方法
8 . 现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图_______ 。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式_______ 。
(3)写出Z与Y的电子排布式_______ 、_______ 。
(4)元素T与氯元素相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 。
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两单质在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是_______ (填元素符号),理由是_______ 。
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式
(3)写出Z与Y的电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性和稳定性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两单质在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
您最近一年使用:0次
20-21高二·全国·课时练习
解题方法
9 . 甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出):
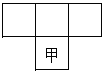
已知①四种元素的原子最外层电子数之和为24;
②甲的原子序数与乙、丙原子序数之和相等。
请回答下列问题:
(1)甲元素在周期表中的位置为_______ 。
(2)丙和丁可形成多种共价化合物,在这些化合物中丙表现正化合价,其中丙具有相同化合价的物质有两种,这两种化合物能够相互转化,反应方程式为_______ 。
(3)甲、乙、丙、丁四种元素的单质均可与H2反应生成氢化物,其中沸点最高的是_______ (写化学式),丙的氢化物溶于丁的氢化物中所形成的溶液滴入酚酞显红色,则丙的氢化物空间构型为_______ 。
(4)乙单质与丁的氢化物能发生置换反应,写出该反应的化学方程式_______ 。
(5)甲的最高价氧化物的水化物的浓溶液在加热条件下能和甲单质反应,写出该反应的化学方程式_______ 。

已知①四种元素的原子最外层电子数之和为24;
②甲的原子序数与乙、丙原子序数之和相等。
请回答下列问题:
(1)甲元素在周期表中的位置为
(2)丙和丁可形成多种共价化合物,在这些化合物中丙表现正化合价,其中丙具有相同化合价的物质有两种,这两种化合物能够相互转化,反应方程式为
(3)甲、乙、丙、丁四种元素的单质均可与H2反应生成氢化物,其中沸点最高的是
(4)乙单质与丁的氢化物能发生置换反应,写出该反应的化学方程式
(5)甲的最高价氧化物的水化物的浓溶液在加热条件下能和甲单质反应,写出该反应的化学方程式
您最近一年使用:0次
20-21高二·全国·单元测试
解题方法
10 . 短周期主族元素W、X、Y、Z的原子序数依次增大。工业上以金红石(主要成分是TiO2)为原料制备金属钛的步骤:①在高温下,向金红石与W的单质组成的混合物中通入黄绿色气体单质Z,得到化合物甲和化学式为WX的气体乙,气体乙会与血红蛋白结合导致人体中毒;②金属Y形成的淡黄色氧化物可用于呼吸面具。在稀有气体环境和加热条件下,用Y的金属单质与甲反应可得钛。下列说法不正确的是
| A.W的氢化物的沸点一定小于X的氢化物 |
| B.简单离子半径:Z>Y>X |
| C.W与Z形成的化合物可用做工业上的重要有机溶剂 |
| D.含Z元素的某种盐具有强氧化性,可用于饮用水消毒 |
您最近一年使用:0次



