1 . 已知A、B、C、D、E是短周期中原子序数依次增大的主族元素,其中A、E的单质在常温下呈气态,B的原子最外层电子数是其电子层数的2倍,C是同周期的主族元素中原子半径最大的元素,D是地壳中含量最多的金属元素。下列说法正确的是
A.1mol由元素A、B组成的化合物一定含有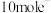 |
| B.元素C、D的简单离子半径:C<D |
| C.C与A形成的化合物是离子化合物 |
| D.化合物AE与CE含有相同类型的化学键 |
您最近一年使用:0次
名校
2 . 有7种短周期元素,其原子半径及主要化合价如下:完成下列填空:
(1)A在元素周期表中的位置是_______ ,当配制150mL实验所需的0.1 mol∙L−1 A最高价氧化物的水合物的溶液,用到的玻璃仪器有_______ ,下列操作可能造成此次配制溶液浓度偏低的有_______ 。
A.用蒸馏水洗净容量瓶未干燥,直接配制新溶液
B.量筒未干燥
C.溶解后将溶液未冷却直接进行后续操作
D.溶解后洗涤烧杯和玻璃棒的洗涤液未全部转移至容量瓶中
E.定容时俯视液面
F.定容时不小心加蒸馏水超过刻度线,用胶头滴管迅速吸出多余的水
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)写出B单质与烧碱溶液反应的离子方程式,并用单线桥法表示出电子转移_______ 。
(4)甲是由G、H两种元素组成的18e-分子,甲中滴入E单质的水溶液,有无色气体产生,写出反应离子方程式:_______ 。
(5)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,−2 | +7,−1 | +5,−3 | −2 | +1 |
A.用蒸馏水洗净容量瓶未干燥,直接配制新溶液
B.量筒未干燥
C.溶解后将溶液未冷却直接进行后续操作
D.溶解后洗涤烧杯和玻璃棒的洗涤液未全部转移至容量瓶中
E.定容时俯视液面
F.定容时不小心加蒸馏水超过刻度线,用胶头滴管迅速吸出多余的水
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)写出B单质与烧碱溶液反应的离子方程式,并用单线桥法表示出电子转移
(4)甲是由G、H两种元素组成的18e-分子,甲中滴入E单质的水溶液,有无色气体产生,写出反应离子方程式:
(5)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次
解题方法
3 . 已知X、Y、Z为三种原子序数相邻的主族元素,其最高价氧化物对应水化物的酸性相对强弱是: 。下列说法
。下列说法不正确 的是
 。下列说法
。下列说法A.电负性: | B.气态氢化物的稳定性: |
C.原子半径: | D.单质的氧化性: |
您最近一年使用:0次
4 . 回答下列问题:
(1)氟原子激发态的电子排布式有______ ,其中能量较高的是______ 。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的______ 区,写出该基态原子电子排布式为______ 。
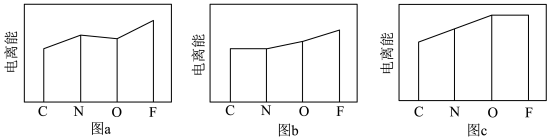
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是______ (填标号),判断的根据是______ ;第三电离能的变化图是______ (填标号)。
(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
①元素的电负性:Z______ W(填“大于”“小于”或“等于”)。
②简单离子半径:W______ Y(填“大于”“小于”或“等于”)。
③氢化物的稳定性:X______ Z(填“大于”“小于”或“等于”)。
(1)氟原子激发态的电子排布式有
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | H3ZO4 | |||
| 0.1 mol∙L−1溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
2023-01-03更新
|
421次组卷
|
2卷引用:天津市和平区2022-2023学年高二上学期期末质量调查化学试卷
名校
5 . 矩周期元素X、Y、Z、W分属三个周期,且原子序数依次增大。其中Y与X、Z均可形成 或
或 的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是
的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是
 或
或 的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是
的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是A.Y与X形成 化合物的电子式为: 化合物的电子式为: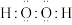 |
B.Y原子的电子排布图: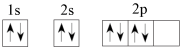 |
C.Z元素在周期表中的位置: 区、第三周期、第IA族 区、第三周期、第IA族 |
D.W原子价层电子排布式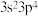 |
您最近一年使用:0次
2022-12-15更新
|
221次组卷
|
2卷引用:天津市南开中学2022-2023学年高二上学期期末考试化学试题
名校
6 . 短周期的三种元素a、b、c在周期表中的位置关系如图所示,下列有关这三种元素的叙述中,正确的是
a | ||
b | ||
c |
| A.非金属性a>b>c |
| B.b的最高价氧化物对应水化物是一种强酸 |
| C.氢化物稳定性:c的氢化物>b的氢化物 |
| D.c的一种氧化物具有漂白性 |
您最近一年使用:0次
7 . X、Y、Z、Q、R是五种短周期主族元素,原子序数依次增大。X是原子半径最小的元素,且X、Y最高正价与最低负价之和均为0, Q与X同主族,Z的氧化物是大气的主要污染物之一,Z与R的最外层电子数之和为8,下列说法正确的是
| A.原子半径大小顺序为: R>Q>Z>Y>X |
| B.Y的氢化物的沸点一定低于Z的氢化物 |
| C.元素Q、R分别与氯元素形成的化合物均为离子化合物 |
| D.Z、Q、R的最高价氧化物对应的水化物两两之间可以相互反应 |
您最近一年使用:0次
8 . 中国国家航天局公布了由“祝融号”火星车拍摄的科学影像图,发现火星岩石中富含X、Y、Z、W四种元素。已知:X、Y、Z、W为原子序数依次增大的四种短周期元素,Z的原子半径是所有短周期主族元素中最大的,X、W为同一主族元素,Y是地球地壳中含量最高的元素,经测定火星岩石中含有物质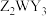 。下列说法错误的是
。下列说法错误的是
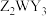 。下列说法错误的是
。下列说法错误的是| A.原子半径:W>Y>X |
| B.W位于元素周期表第三周期IVA族 |
| C.Y和W形成的化合物能与X的单质在一定条件下反应 |
D.化合物Z2Y、Z2Y2中阴阳离子个数比均为 |
您最近一年使用:0次
2022-07-24更新
|
143次组卷
|
2卷引用:陕西省渭南市蒲城县2021-2022学年高二下学期期末对抗赛化学试题
9 . X、Y、Z、R为短周期主族元素,X为原子半径最大的短周期元素,Y的气态氢化物与其最高价氧化物对应的水化物可反应生成离子化合物,Z元素的单质为淡黄色固体,R与Z同周期,R的最低负价和最高正价分别为−1,+7,另有元素W,其原子序数为34。
(1)元素W在周期表中位置为___________ ,原子结构示意图为___________ 。
(2)X、Y、Z、R元素形成的四种简单离子半径由大到小顺序为___________ (用离子符号表示)。
(3)Y的气态氢化物可与R的单质反应产生白烟,该反应的化学方程式为___________ ,Y的某种氢化物电子数目为18,该氢化物的电子式为___________ 。
(4)设计一个简单可行的实验方案验证Z与R的非金属性强弱___________ 。
(1)元素W在周期表中位置为
(2)X、Y、Z、R元素形成的四种简单离子半径由大到小顺序为
(3)Y的气态氢化物可与R的单质反应产生白烟,该反应的化学方程式为
(4)设计一个简单可行的实验方案验证Z与R的非金属性强弱
您最近一年使用:0次
解题方法
10 . X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,最且外层电子数之和为15;X与Z可形成XZ2分子,Y与M形成的气态化合物在标准状态下的密度为0.76g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.简单离子的半径: W>Y>X>Z>M |
| B.由元素X、Y、Z、M共同形成的化合物中一定有共价键,可能有离子键 |
| C.CaM2和CaZ2两种化合物中,阳离子与阴离子个数比均为1:2 |
| D.XZ2、 X2M2、W2Z2均为共价化合物 |
您最近一年使用:0次



