1 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。

回答下列问题:
(1)写出物质R的电子式。_______ 。
(2)下列有关图中所示含N、S物质的叙述,正确的是_______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是_______ 。
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析, 晶体中所含化学键的类型有
晶体中所含化学键的类型有_______ ,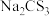 水溶液显
水溶液显_______ (填“酸性”、“碱性”或“中性”)。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: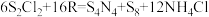 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有_______ ,该反应每生成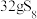 转移电子
转移电子_______  。其中被氧化的元素是
。其中被氧化的元素是_______ (填元素符号)。

回答下列问题:
(1)写出物质R的电子式。
(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与
 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将
 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析,
 晶体中所含化学键的类型有
晶体中所含化学键的类型有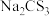 水溶液显
水溶液显(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: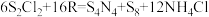 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有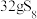 转移电子
转移电子 。其中被氧化的元素是
。其中被氧化的元素是
您最近一年使用:0次
名校
2 . 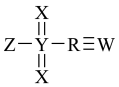 是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
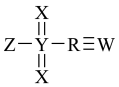 是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是A. 与 与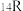 的中子数相同 的中子数相同 |
| B.第一电离能:X>W>R |
| C.简单氢化物还原性:Z>Y |
| D.R、W、X三种元素均能与氢元素形成含非极性键的二元化合物 |
您最近一年使用:0次
解题方法
3 . 盐X只含四种短周期元素,按如下流程进行实验:
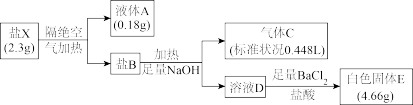
已知:气体C能使湿润红色石蕊变蓝。
请回答:
(1)盐X含_______ (填元素符号),气体C的VSEPR模型为_______ 。
(2)盐X与足量NaOH溶液在加热条件下的离子方程式_______ 。
(3)盐B对应的酸常温常压下为无色结晶性粉末,主要用于氧化剂、磺化剂及硝化反应中的脱水剂,制染料、炸药,石油产品精制和其他有机磺酸化合物。根据以上信息判断,下列物质中一定条件下能与该酸反应的是_______。
(4)工业上盐B重要的用途之一是溶解难溶氧化物生成常见的盐,请写出盐B与 反应的化学方程式
反应的化学方程式_______ 。

已知:气体C能使湿润红色石蕊变蓝。
请回答:
(1)盐X含
(2)盐X与足量NaOH溶液在加热条件下的离子方程式
(3)盐B对应的酸常温常压下为无色结晶性粉末,主要用于氧化剂、磺化剂及硝化反应中的脱水剂,制染料、炸药,石油产品精制和其他有机磺酸化合物。根据以上信息判断,下列物质中一定条件下能与该酸反应的是_______。
| A.甲苯 | B. | C. | D.Cu |
 反应的化学方程式
反应的化学方程式
您最近一年使用:0次
解题方法
4 . X、Y、Z、W是原子序数依次增大的短周期元素,X与W同主族,且W原子核内质子数是X原子核外电子数的两倍,Y是同周期元素中原子半径最大的,Y、Z、W的最高价氧化物对应的水化物可两两反应生成盐和水,甲是Z、W两种元素形成的化合物。下列说法错误的是
| A.X单质的氧化性强于W单质 |
| B.Z的合金在生产生活中用途广泛 |
| C.可以在水溶液中利用复分解反应制备甲 |
| D.离子半径:W>X>Y>Z |
您最近一年使用:0次
解题方法
5 . X、Y、Z、W是原子序数依次增大的短周期元素,X与W同主族,且W原子核内质子数是X原子核外电子数的两倍,Y是同周期元素中原子半径最大的,Y、Z、W的最高价氧化物对应的水化物可两两反应生成盐和水,甲是Z、W两种元素形成的化合物。下列说法错误的是
| A.X单质的氧化性强于W单质 |
| B.可以用电解NaCl溶液制取Y |
| C.Z的合金在生产生活中用途广泛 |
D.存在如下转化关系: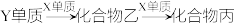 |
您最近一年使用:0次
21-22高一上·辽宁沈阳·阶段练习
名校
6 . 现有四种短周期元素,其有关信息如表所示:
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 第三周期某金属元素 | 氧化物为两性氧化物 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 单质是重要的半导体材料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的单质 | 丁的一种单质与KI溶液反应生成丁的另一种单质 |
| A.乙、甲、丁、丙 | B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 | D.甲、乙、丙、丁 |
您最近一年使用:0次
2021-12-15更新
|
891次组卷
|
3卷引用:第13练 元素周期律-2022年【寒假分层作业】高一化学(人教版2019)
名校
7 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。请回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第____ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ 。
(3)下列有关性质的比较能用元素周期律解释的是____ (填字母,下同)。
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为____ 。
②X的氢化物的电子式:____ 。
③写出Y的最高价氧化物的一种用途____ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3 b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2 d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次
名校
8 . A、B、D、X、Y是原子序数依次增大的五种短周期主族元素。A是地壳中含量最多的元素,A、X是同主族元素;B是短周期中原子半径最大的元素;D的周期序数和族序数相等。用化学用语回答下列问题:
(1)写出X元素的简单离子的结构示意图_______ 。
(2)A、B、D三种元素的简单离子半径从大到小的顺序是_______ (填离子符号)。
(3)B、Y两元素形成的化合物有重要用途,用电子式表示它的形成过程_______ 。
(4)写出B、D两元素的最高价氧化物对应水化物发生反应的离子方程式_______ 。
(5) 与A、X是同一主族的元素,且在元素周期表中与X相邻。
与A、X是同一主族的元素,且在元素周期表中与X相邻。
①根据元素周期律,下列推断正确的是_______ (填字母序号)。
a. 的最高正化合价为
的最高正化合价为 价 b.
价 b. 的还原性比
的还原性比 强
强
c. 的酸性比
的酸性比 强 d.
强 d. 在一定条件下可与
在一定条件下可与 溶液反应
溶液反应
②室温下向 固体表面吹入
固体表面吹入 ,可得到两种单质和
,可得到两种单质和 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(6)将Y的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号_______ 。

(1)写出X元素的简单离子的结构示意图
(2)A、B、D三种元素的简单离子半径从大到小的顺序是
(3)B、Y两元素形成的化合物有重要用途,用电子式表示它的形成过程
(4)写出B、D两元素的最高价氧化物对应水化物发生反应的离子方程式
(5)
 与A、X是同一主族的元素,且在元素周期表中与X相邻。
与A、X是同一主族的元素,且在元素周期表中与X相邻。①根据元素周期律,下列推断正确的是
a.
 的最高正化合价为
的最高正化合价为 价 b.
价 b. 的还原性比
的还原性比 强
强c.
 的酸性比
的酸性比 强 d.
强 d. 在一定条件下可与
在一定条件下可与 溶液反应
溶液反应②室温下向
 固体表面吹入
固体表面吹入 ,可得到两种单质和
,可得到两种单质和 ,该反应的化学方程式为
,该反应的化学方程式为(6)将Y的单质通入石蕊溶液中发生的颜色变化如下图,请在方框内填写出导致该阶段颜色变化的主要粒子符号

您最近一年使用:0次
名校
解题方法
9 . 氢是宇宙中最轻的元素,其单质、化合物有许多独特的功能或用途.
(1)“人造太阳”可为人类提供用之不尽的清洁能源,我国在“人造太阳”领域的研究走在世界的前列,其工作原理可表示为 。下列有关上述变化的说法错误的是_______(填序号)。
。下列有关上述变化的说法错误的是_______(填序号)。
(2)下列五种含氢元素的物质:① 、②
、②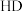 、③
、③ 、④
、④ 、⑤
、⑤ ,其中只含有极性键的物质是
,其中只含有极性键的物质是_______ (填序号,下同),含有共价键的离子化合物是_______ , 的结构式为
的结构式为_______ ,NaH的电子式为_______ 。
(3) 是一种温室气体,热稳定性:
是一种温室气体,热稳定性:
_______  (填“>”或“<”).若将
(填“>”或“<”).若将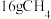 与
与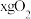 混合点燃,当二者恰好反应完时,得到
混合点燃,当二者恰好反应完时,得到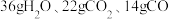 ,写出该燃烧反应的化学方程式:
,写出该燃烧反应的化学方程式:_______ 。
(4)氢元素与X、Y两种短周期主族元素可形成多种三元化合物,已知X、Y的价电子数之和为13且X的原子半径小于Y。写出上述Y呈最高正价时的三元化合物的化学式:_______ ,举例说明非金属性 :
:_______ 。
(1)“人造太阳”可为人类提供用之不尽的清洁能源,我国在“人造太阳”领域的研究走在世界的前列,其工作原理可表示为
 。下列有关上述变化的说法错误的是_______(填序号)。
。下列有关上述变化的说法错误的是_______(填序号)。| A.是化学变化 | B.释放出大量的热量 | C.R是 | D. 是中子 是中子 |
 、②
、②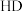 、③
、③ 、④
、④ 、⑤
、⑤ ,其中只含有极性键的物质是
,其中只含有极性键的物质是 的结构式为
的结构式为(3)
 是一种温室气体,热稳定性:
是一种温室气体,热稳定性:
 (填“>”或“<”).若将
(填“>”或“<”).若将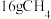 与
与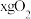 混合点燃,当二者恰好反应完时,得到
混合点燃,当二者恰好反应完时,得到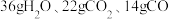 ,写出该燃烧反应的化学方程式:
,写出该燃烧反应的化学方程式:(4)氢元素与X、Y两种短周期主族元素可形成多种三元化合物,已知X、Y的价电子数之和为13且X的原子半径小于Y。写出上述Y呈最高正价时的三元化合物的化学式:
 :
:
您最近一年使用:0次
2022-04-05更新
|
216次组卷
|
2卷引用:河南省商丘市虞城县高级中学2021-2022学年高一上学期期末考试化学试题
解题方法
10 . 已知短周期五种元素X、Y、Z、W、H原子序数依次增大。X、H同主族,Y、Z、W是同周期的相邻元素。W原子的质子数等于X、Z的原子序数之和。X与Z形成的最简单化合物分子中有3个共价键。Y的一种核素被应用于考古。回答下列问题:
(1)Y元素的名称是:_______ 。
(2)H在元素周期表中的位置:_______ ;H与氧形成的一种化合物与Y的最高价氧化物反应生成W单质的化学方程式为_______ 。
(3)由X、Z、W所形成的离子化合物M的化学式是_______ ;写出一种M在农业上的用途:_______ 。
(4)若用Y的最简单氢化物和空气组成燃料电池,则通入空气(氧气的体积分数约为 )的一极为原电池的
)的一极为原电池的_______ 极(填“正”、“负”),理论上消耗32gY的最简单氢化物,需要标准状况下空气_______ L。
(1)Y元素的名称是:
(2)H在元素周期表中的位置:
(3)由X、Z、W所形成的离子化合物M的化学式是
(4)若用Y的最简单氢化物和空气组成燃料电池,则通入空气(氧气的体积分数约为
 )的一极为原电池的
)的一极为原电池的
您最近一年使用:0次



