解题方法
1 . X、Y、Z、M为原子序数依次增大的短周期主族元素,这四种元素原子的最外层电子数之和等于12。A~G是由上述四种元素组成的化合物,其转化关系如图所示,其中C是一种强碱,焰色试验呈黄色。

回答下列问题:
(1)元素Y在元素周期表中的位置是___________ 。
(2)Y、Z、M三种元素的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)能说明Z的非金属性强于Y的依据是___________ (写一点即可)。
(4)写出反应①的离子方程式___________ 。
(5)去除A溶液中混有的少量B的方法是___________ 。
(6)3.9g固体D与足量F反应转移的电子数目为___________ 。
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是___________ (填标号)。
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng

回答下列问题:
(1)元素Y在元素周期表中的位置是
(2)Y、Z、M三种元素的原子半径由大到小的顺序为
(3)能说明Z的非金属性强于Y的依据是
(4)写出反应①的离子方程式
(5)去除A溶液中混有的少量B的方法是
(6)3.9g固体D与足量F反应转移的电子数目为
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng
您最近一年使用:0次
名校
2 . 短周期元素W、X、Y、Z、Q、R的原子序数依次增大,c、d、e、f、h是由这些元素组成的二元化合物,自然界中硬度最大的单质和a都由X组成,b由W、Y、Q三种元素组成,d能使品红溶液褪色,是液体,上述物质的转化关系如下图所示(个别产物略去)。请回答下列问题:
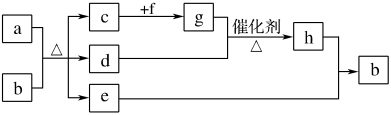
(1)R在元素周期表中的位置:_______ 。
(2)化合物f的电子式:_______ 该化合物存在的化学键种类是:_______ ;化合物c的结构式:_______ 。
(3)用电子式表示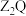 的形成过程为
的形成过程为_______ 。
(4)W、Y、Z、Q四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为_______ 、_______ ,这两种酸式盐相互反应的离子方程式为_______ 。
(5)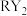 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过 和
和 在稀硫酸酸化的环境中反应制得气体
在稀硫酸酸化的环境中反应制得气体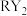 ,试写出该反应的离子反应方程式并配平:
,试写出该反应的离子反应方程式并配平:_______ 。
(6)在100mL 18mol/L b的浓溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是_______(填序号)。

(1)R在元素周期表中的位置:
(2)化合物f的电子式:
(3)用电子式表示
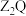 的形成过程为
的形成过程为(4)W、Y、Z、Q四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
(5)
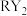 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过 和
和 在稀硫酸酸化的环境中反应制得气体
在稀硫酸酸化的环境中反应制得气体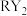 ,试写出该反应的离子反应方程式并配平:
,试写出该反应的离子反应方程式并配平:(6)在100mL 18mol/L b的浓溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是_______(填序号)。
| A.7.32L | B.6.72L | C.20.16L | D.30.24L |
您最近一年使用:0次
名校
解题方法
3 . 元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;N-、Z3+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)R在元素周期表中的位置是____________ ;Z3+的离子结构示意图是____________ 。
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式__________ ;M和N气态氢化物的稳定性大小比较为________ (用化学式和“>”“<”或“=”表示)。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________ .
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_____________________________ 。
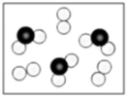
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是__________ (填化学式),示意图中转移电子的数目为______ 。


(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______________________ 。
(1)R在元素周期表中的位置是
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是



(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
2017-12-08更新
|
235次组卷
|
3卷引用: 安徽省舒城中学2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
4 . 元素及其化合物知识在工农业生产、生活中被广泛使用,造福人类。
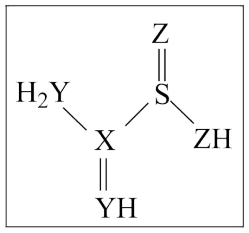
I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为___________ ,该漂白剂所含元素非金属性最强的元素是在元素周期表中的位置为___________ 。
(2)下列说法错误的是___________(选填序号)。
Ⅱ.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为___________ 。图中该氢化物转化为甲的化学方程式___________ 。化合物丁中Y元素的质量分数为___________ %。
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为___________ 。该氢化物与丙的浓溶液反应,出现淡黄色浑浊且有刺激性气体放出。每生成1摩尔沉淀时,转移的电子数目为___________ 。

I.元素X、Y、Z和H、S元素组成的某种化合物(结构如图)常用作丝绸漂白剂,图中所有元素仅X、Y、Z同周期且原子序数依次增大。回答下列问题:
(1)Y元素的原子结构示意图为
(2)下列说法错误的是___________(选填序号)。
| A.原子半径:X>Y>Z | B.简单气态氢化物稳定性:Y<Z |
| C.沸点:H2Z<H2S | D.该化合物中所有原子均为8电子稳定结构 |
Ⅱ.该漂白剂中有两种元素的氢化物均可发生如下转化:

(3)若该氢化物的水溶液呈碱性,写出该氢化物的电子式为
(4)若该化合物的水溶液呈酸性,图中甲转化为乙的化学方程式为
您最近一年使用:0次
解题方法
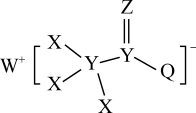
5 . 一种用于合成治疗免疫疾病药物的物质,其结构如图所示,其中X、Y、Z、Q、W为1~20号元素且原子序数依次增大,乙与Q同主族,Q和W的简单离子具有相同的电子层结构。
(1)W在元素周期表中的位置为_______ 。
(2)五种元素原子半径由大到小的顺序为_______ (用元素符号表。示),Z、Q、W的离子半径最小的是_______ (填离子符号)。
(3)元素W、Z可形成化合物 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:_______ (用元素符号表示)。
(4) 的水化物与Al反应的化学方程式为
的水化物与Al反应的化学方程式为_______ 。
(5)元素W的金属性_______ (填“>”或“<”)元素Na的金属性,下列方法可证明这一事实的是_______ (填字母)。
a.比较元素W的单质和Na单质分别与水反应的剧烈程度
b.比较元素W与Na最高价氧化物对应水化物碱性的强弱
c.比较常温下W的单质与Na的单质的物理状态
d.比较二者原子半径的大小

(1)W在元素周期表中的位置为
(2)五种元素原子半径由大到小的顺序为
(3)元素W、Z可形成化合物
 ,用电子式表示
,用电子式表示 的形成过程:
的形成过程:(4)
 的水化物与Al反应的化学方程式为
的水化物与Al反应的化学方程式为(5)元素W的金属性
a.比较元素W的单质和Na单质分别与水反应的剧烈程度
b.比较元素W与Na最高价氧化物对应水化物碱性的强弱
c.比较常温下W的单质与Na的单质的物理状态
d.比较二者原子半径的大小
您最近一年使用:0次
解题方法
6 . 短周期主族元素第一电离能与原子半径的关系如图所示。回答下列问题:

(1)元素⑤在元素周期表中的位置为_______ ;元素②与⑭形成的化合物的电子式为_______ 。
(2)第一电离能在元素⑪处出现齿峰的原因是_______ 。
(3)元素⑩⑪⑫分别与元素①形成的简单化合物中,键角最大的是_______ (用化学式表示)。
(4)元素⑦与⑧的最高价氧化物对应水化物碱性较强的是_______ (用化学式表示)。
(5)元素⑬和⑮二者的最高价氧化物对应的水化物相互反应的离子方程式为_______ 。
(6)海水提溴工艺中,将溴单质吹入吸收塔中,用元素⑩的某种含氧酸盐对溴进行富集,该过程中反应的离子方程式为_______ 。
(7)用一个化学方程式表示元素③与⑩的非金属性强弱_______ 。

(1)元素⑤在元素周期表中的位置为
(2)第一电离能在元素⑪处出现齿峰的原因是
(3)元素⑩⑪⑫分别与元素①形成的简单化合物中,键角最大的是
(4)元素⑦与⑧的最高价氧化物对应水化物碱性较强的是
(5)元素⑬和⑮二者的最高价氧化物对应的水化物相互反应的离子方程式为
(6)海水提溴工艺中,将溴单质吹入吸收塔中,用元素⑩的某种含氧酸盐对溴进行富集,该过程中反应的离子方程式为
(7)用一个化学方程式表示元素③与⑩的非金属性强弱
您最近一年使用:0次
7 . W、X、Y、Z是元素周期表中的四种短周期元素,其相关信息及原子半径与原子序数的关系如表所示。请回答下列问题:
(1)W在元素周期表中的位置是___ ,W与X形成的含有共价键的常见化合物的电子式为___ 。
(2)X、Z的简单离子的半径大小为__ (用离子符号表示)。
(3)Y的最高价氧化物与单质碳在高温下反应的化学方程式为__ ;Z的简单氢化物与X的最高价氧化物对应的水化物反应的离子方程式为__ 。
(4)最高价氧化物对应水化物的酸性:Y__ (填“大于”或“小于”,下同)磷;第一电离能:Y__ 磷。
| 元素 | 相关信息 | 原子半径与原子序数的关系 |
| W | 其一种核素的质量数为18,中子数为10 |  |
| X | 其原子与电子排布式为1s22s22p6的原子的核外电子数相差1 | |
| Y | 其单质是一种常见的半导体材料 | |
| Z | 电负性在同周期元素中最大 |
(2)X、Z的简单离子的半径大小为
(3)Y的最高价氧化物与单质碳在高温下反应的化学方程式为
(4)最高价氧化物对应水化物的酸性:Y
您最近一年使用:0次
2021-04-14更新
|
511次组卷
|
2卷引用:第一章原子结构与性质(提升卷)
名校
解题方法
8 . A是常见的非金属固体单质,F是紫红色的金属单质,B、C是常见的强酸,D、G、I是常见的气体,D与I 的组成元素相同,且D的相对分子质量比I的大16,E是最常见的无色液体。有关物质的转化关系如下图所示(部分生成物与反应条件已略去)。请回答下列问题:
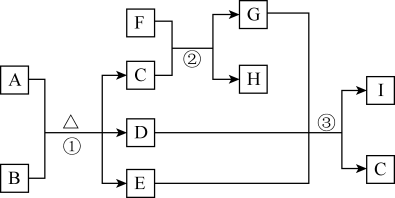
(1)A中所含元素在周期表中的位置___________ ,E的电子式为___________
(2)D、G、I中属于酸性氧化物的是(填化学式)___________
(3)写出反应①的化学方程式:___________
(4)写出反应③的离子方程式:___________
(5)38.4g F跟适量B的浓溶液反应,F完全反应,共收集到气体22.4L(不考虑2NO2⇌N2O4,气体体积已折算为标准状况),反应消耗B的物质的量是___________

(1)A中所含元素在周期表中的位置
(2)D、G、I中属于酸性氧化物的是(填化学式)
(3)写出反应①的化学方程式:
(4)写出反应③的离子方程式:
(5)38.4g F跟适量B的浓溶液反应,F完全反应,共收集到气体22.4L(不考虑2NO2⇌N2O4,气体体积已折算为标准状况),反应消耗B的物质的量是
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E是中学化学中的常见物质,A是空气中含量第二的气体。其转化关系如下:
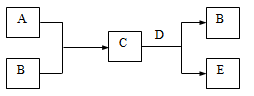
请回答:
(1)若C为红棕色气体,D为无色液体。
①组成A的元素在周期表中的位置是___________ 。
②下列叙述正确的是___________ (填字母)。
a.B、C、E的组成中均含有两种相同元素
b.C与D的反应中,C是氧化剂,D是还原剂
c.E的浓溶液见光易分解,一般保存在棕色试剂瓶中
(2)若B为黄色固体,C是由同主族两种元素组成的物质。D、E均为氢化物。
① C与D反应的化学方程式是___________ 。
② C与D反应中转移0.4 mol电子时,生成B的质量为___________ 。

请回答:
(1)若C为红棕色气体,D为无色液体。
①组成A的元素在周期表中的位置是
②下列叙述正确的是
a.B、C、E的组成中均含有两种相同元素
b.C与D的反应中,C是氧化剂,D是还原剂
c.E的浓溶液见光易分解,一般保存在棕色试剂瓶中
(2)若B为黄色固体,C是由同主族两种元素组成的物质。D、E均为氢化物。
① C与D反应的化学方程式是
② C与D反应中转移0.4 mol电子时,生成B的质量为
您最近一年使用:0次
2021-05-31更新
|
134次组卷
|
2卷引用:北京市第三中学2021-2022学年高一下学期期中测试化学试题



