名校
1 . X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。上述物质有如图转化关系如图所示。
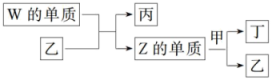
(1)Y、Z元素分别为_______ 、_______ (填元素符号)
(2)丙的水溶液刻蚀玻璃的化学反应方程式是_______
(3)X与Y还可以结合形成Y2X4分子,Y2X4的电子式为_______ ,Y的化合价为_______ 。实验室可用次氯酸钠溶液与甲反应制备Y2X4,反应的化学方程式为_______ 。
(4)下列关于元素及其化合物性质的判断中,正确的是_______ (填序号)
A.元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
B.金属元素A、B能分别形成+2、+3价离子,所以氧化性:A2+<B3+
C.因为 ,所以金属性:Pb>Fe
,所以金属性:Pb>Fe
D.因为 ,所以非金属性:Cl>S
,所以非金属性:Cl>S
E.因为水溶液的酸性:HmA>HnB,所以非金属性:A>B
F.HCl是一元酸,而H2SO4是二元酸,所以酸性:H2SO4>HCl
(5)某同学查阅资料知:甲的分解温度在850℃以上,甲烷(CH4)的分解温度是655℃,据此得出结论:Y元素的非金属性强于碳元素。该同学通过实验间接证明了自己的结论。你认为该同学的实验方案是(请结合离子方程式简要说明):_______ 。

(1)Y、Z元素分别为
(2)丙的水溶液刻蚀玻璃的化学反应方程式是
(3)X与Y还可以结合形成Y2X4分子,Y2X4的电子式为
(4)下列关于元素及其化合物性质的判断中,正确的是
A.元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
B.金属元素A、B能分别形成+2、+3价离子,所以氧化性:A2+<B3+
C.因为
 ,所以金属性:Pb>Fe
,所以金属性:Pb>FeD.因为
 ,所以非金属性:Cl>S
,所以非金属性:Cl>SE.因为水溶液的酸性:HmA>HnB,所以非金属性:A>B
F.HCl是一元酸,而H2SO4是二元酸,所以酸性:H2SO4>HCl
(5)某同学查阅资料知:甲的分解温度在850℃以上,甲烷(CH4)的分解温度是655℃,据此得出结论:Y元素的非金属性强于碳元素。该同学通过实验间接证明了自己的结论。你认为该同学的实验方案是(请结合离子方程式简要说明):
您最近一年使用:0次
名校
解题方法
2 . 部分短周期主族元素的原子半径和主要化合价的关系如图所示,其中E、G、T位于同一周期。回答下列问题:

(1)B位于第_______ 周期第______ 族。
(2)FDB的电子式为_______ ;T的原子结构示意图为_______ 。
(3)设计简单实验证明D的非金属性比C的强:________ 。
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是_______ 。
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ;上述非金属元素的简单氢化物中,沸点最高的是_______ ,还原性最强的是_______ 。
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为_______ 。

(1)B位于第
(2)FDB的电子式为
(3)设计简单实验证明D的非金属性比C的强:
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为
您最近一年使用:0次
2023-10-27更新
|
171次组卷
|
2卷引用:湖南省炎德·英才·名校联考联合体2023-2024学年高三上学期第三次联考化学试题
3 . 如图为从元素周期表截取的短周期主族元素的一部分,Y是所在周期中原子半径最小的元素。下列说法正确的是


| A.Y的最高价氧化物对应的水化物酸性最强 |
| B.X的一种氢化物具有强氧化性 |
| C.W的最高价氧化物分子中所有原子的最外层都达到8电子稳定结构 |
D.简单离子的还原性: |
您最近一年使用:0次
名校
4 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中的位置为_______ ,B的离子结构示意图_______ 。
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)_______ 。C单质与水反应生成的具有漂白性物质的电子式_______
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b.SeO2 既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3
d.非金属性比C元素的强
(4)已知A的某种氢化物相对分子质量为58,写出它的所有可能结构(结构简式):_______ 。
| 元素 | 相关信息 |
| A | 自然界中形成化学物种类最多的元素 |
| B | 单质的焰色反应为黄色 |
| C | 单质是黄绿色气体,可用于自来水消毒 |
| D | −2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中的位置为
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.SeO2 既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3
d.非金属性比C元素的强
(4)已知A的某种氢化物相对分子质量为58,写出它的所有可能结构(结构简式):
您最近一年使用:0次
名校
5 .  、
、 为第三周期元素,
为第三周期元素, 最高正价与最低负价的代数和为6,二者形成的一种化合物能以
最高正价与最低负价的代数和为6,二者形成的一种化合物能以 的形式存在。下列说法错误的是
的形式存在。下列说法错误的是
 、
、 为第三周期元素,
为第三周期元素, 最高正价与最低负价的代数和为6,二者形成的一种化合物能以
最高正价与最低负价的代数和为6,二者形成的一种化合物能以 的形式存在。下列说法错误的是
的形式存在。下列说法错误的是A.原子半径: | B.简单氢化物的还原性: |
C.同周期元素形成的单质中 氧化性最强 氧化性最强 | D.最高价含氧酸的酸性: |
您最近一年使用:0次
名校
解题方法
6 . 短周期元素 X、Y、Z、W 的原子序数依次增加。Y 的简单氢化物常温下呈液态,X 的简单氢化物溶于水,溶液显碱性,Z 是短周期中还原性最强的元素,W 元素的最高价氧 化物的对应水化物是短周期中酸性最强的无机含氧酸。下列说法正确的是
| A.原子半径:W<Z<Y |
| B.X 形成的含氧酸一定是强酸 |
| C.Z 的单质与 CuSO4 溶液反应,可置换出 Cu |
| D.W 元素可形成具有消毒作用的化合物 |
您最近一年使用:0次
2020-12-21更新
|
226次组卷
|
2卷引用:山西省运城市夏县第二中学2021届高三上学期11月联考化学试题
7 . A、B、C、D为核电荷数依次增大的前三周期主族元素,A和C同族,B和D同族,B的简单离子和C的简单离子具有相同的电子层结构,A和B、D均能形成共价化合物,A和B、C分别形成的化合物溶于水均呈碱性。下列说法中错误的 是
| A.4种元素中C的金属性最强 |
| B.简单阳离子氧化性:A>C |
| C.A和C形成的化合物与水反应能生成一种还原性气体 |
| D.最高价氧化物对应的水化物的酸性:D>B |
您最近一年使用:0次
名校
8 . 2019年是元素周期表诞生150周年,元素周期表在学习、研究和生产实践中有很重要的作用。已知 、
、 、
、 、
、 是中学常见的四种元素.原子序数依次增大。
是中学常见的四种元素.原子序数依次增大。 的原子最外层电子数是次外层的2倍。
的原子最外层电子数是次外层的2倍。 的氧化物属于两性氧化物,
的氧化物属于两性氧化物, 、
、 位于同周期,
位于同周期, 、
、 、
、 的原子最外层电子数之和为14,
的原子最外层电子数之和为14, 是人体必需的微量元素,缺乏
是人体必需的微量元素,缺乏 会导致贫血症状。
会导致贫血症状。
(1)硒是人体必需的微量元素。人体内产生的活性氧能加速人体衰老,被称为“生命杀手”。化学家尝试用 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出_______ 性。
(2)下列事实能用元素周期律解释的是_______ (填序号)。
a. 的最高价氧化物对应水化物的碱性弱于
的最高价氧化物对应水化物的碱性弱于
b. 的气态氢化物的稳定性小于
的气态氢化物的稳定性小于
c.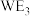 的溶液可用于刻蚀铜制的印刷电路板
的溶液可用于刻蚀铜制的印刷电路板
(3) 的单质可用于处理酸性废水中的
的单质可用于处理酸性废水中的 ,使其转换为
,使其转换为 ,同时生成有磁性的
,同时生成有磁性的 的氧化物
的氧化物 ,再进行后续处理。
,再进行后续处理。
①上述反应的离子方程式为_______ 。
② 的单质与
的单质与 在高温下反应的化学方程式为
在高温下反应的化学方程式为_______ 。
(4)铅和 元素同主族,可发生反应
元素同主族,可发生反应 。请写出草酸的电子式:
。请写出草酸的电子式:_______ 。 与
与 性质相似,
性质相似, 与氢氧化钠溶液反应的离子方程式是
与氢氧化钠溶液反应的离子方程式是_______ 。
(5)金属镓有“电子工业脊梁”的美誉,它与 同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含
同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含 、
、 、
、 杂质,以
杂质,以 水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:
水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为: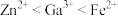 )下列有关电解精炼镓的说法正确的是_______(填序号)。
)下列有关电解精炼镓的说法正确的是_______(填序号)。
 、
、 、
、 、
、 是中学常见的四种元素.原子序数依次增大。
是中学常见的四种元素.原子序数依次增大。 的原子最外层电子数是次外层的2倍。
的原子最外层电子数是次外层的2倍。 的氧化物属于两性氧化物,
的氧化物属于两性氧化物, 、
、 位于同周期,
位于同周期, 、
、 、
、 的原子最外层电子数之和为14,
的原子最外层电子数之和为14, 是人体必需的微量元素,缺乏
是人体必需的微量元素,缺乏 会导致贫血症状。
会导致贫血症状。(1)硒是人体必需的微量元素。人体内产生的活性氧能加速人体衰老,被称为“生命杀手”。化学家尝试用
 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出(2)下列事实能用元素周期律解释的是
a.
 的最高价氧化物对应水化物的碱性弱于
的最高价氧化物对应水化物的碱性弱于
b.
 的气态氢化物的稳定性小于
的气态氢化物的稳定性小于
c.
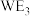 的溶液可用于刻蚀铜制的印刷电路板
的溶液可用于刻蚀铜制的印刷电路板(3)
 的单质可用于处理酸性废水中的
的单质可用于处理酸性废水中的 ,使其转换为
,使其转换为 ,同时生成有磁性的
,同时生成有磁性的 的氧化物
的氧化物 ,再进行后续处理。
,再进行后续处理。①上述反应的离子方程式为
②
 的单质与
的单质与 在高温下反应的化学方程式为
在高温下反应的化学方程式为(4)铅和
 元素同主族,可发生反应
元素同主族,可发生反应 。请写出草酸的电子式:
。请写出草酸的电子式: 与
与 性质相似,
性质相似, 与氢氧化钠溶液反应的离子方程式是
与氢氧化钠溶液反应的离子方程式是(5)金属镓有“电子工业脊梁”的美誉,它与
 同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含
同主族,其氧化物和氢氧化物均为两性化合物。工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含 、
、 、
、 杂质,以
杂质,以 水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:
水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为: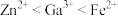 )下列有关电解精炼镓的说法正确的是_______(填序号)。
)下列有关电解精炼镓的说法正确的是_______(填序号)。A.阳极发生氧化反应,其主要电极反应式: |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
C.在阴极除了析出高纯度的镓之外,还可能有 产生 产生 |
D.电解后,电解槽底部的阳极泥中只有 和 和 |
您最近一年使用:0次
解题方法
9 . A、B、C、D、E、F代表6种原子序数依次增大的常见短周期元素。A可与B形成A2B,A2B2,两种物质常温下均为液体;C也可与B形成C2B、C2B2两种离子化合物;室温下,D的单质放在冷的浓硝酸或空气中,表面都生成致密的氧化膜;E与B属于同族元素。回答下列有关问题:
(1)元素D在周期表中的位置是_______ 。
(2)F元素可形成多种含氧酸,其中酸性最强的是_______ 填化学式,下同),氧化性最强的是_______ 。
(3)6种元素最高价氧化物所对应的水化物中,碱性最强的是_______ (填化学式),氢氧化物呈两性的是_______ (填化学式)。
(4)E与F各自形成的简单氢化物中更稳定的是_______ (填化学式)。
(5)B、C、F可形成一种_______ (填“离子”或“共价”)化合物_______ (填化学式),是漂白液的有效成分。
(6)B的简单氢化物比E的简单氢化物的沸点_______ (填“高”或“低”),原因是_______ 。
(1)元素D在周期表中的位置是
(2)F元素可形成多种含氧酸,其中酸性最强的是
(3)6种元素最高价氧化物所对应的水化物中,碱性最强的是
(4)E与F各自形成的简单氢化物中更稳定的是
(5)B、C、F可形成一种
(6)B的简单氢化物比E的简单氢化物的沸点
您最近一年使用:0次
名校
10 . W、X、Y、Z 为原子序数依次增大的短周期元素, W 和 Y同族, X 和Z 同族, X 的简单离子和 Y 的简单离子具有相同的电子层结构, W 和 X、Z 能分别形成分子式为 XW3、 ZW3 的共价化合物,这两种共价化合物溶于水均呈碱性。下列说法不正确的是
| A.四种元素中Y 的金属性最强 |
| B.最高价氧化物对应水化物的酸性: Z > X |
| C.简单阳离子的氧化性: W>Y |
| D.化合物 YW 与水反应能生成还原性气体 |
您最近一年使用:0次
2020-07-03更新
|
195次组卷
|
3卷引用:四川省成都市第七中学家2019-2020学年高一下学期6月考试化学试题



