1 . 短周期主族元素R、X、Y、Z的原子序数依次增大,R和Y位于同主族。Z的气态氢化物为M,0.01mol·L-1的M溶液的pH=2。R、X、Z能组成一种化合物,其球棍模型如图所示。下列说法正确的是
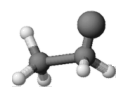

| A.原子半径:R<X<Y<Z |
| B.Z的最高价氧化物对应水化物的酸性一定比X的强 |
| C.R与X形成的化合物均为气态 |
| D.工业上电解YZ的水溶液制备Y的单质 |
您最近一年使用:0次
2 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其次外层电子数的3倍,Z可与X形成淡黄色化合物Z2X2,Y、W的最外层电子数相同。下列说法正确的是
| A.简单离子半径:Y>Z |
| B.Y单质能从溶液中置换出W单质 |
| C.非金属性:W>X |
| D.Z2X2只有氧化性,没有还原性 |
您最近一年使用:0次
解题方法
3 . W、X、Y、Z为原子序数依次增大的短周期主族元素,短周期主族元素中W的原子半径最大,X的单质可用作生产计算机芯片的材料,水体中Y元素含量高会导致水体富营养化,Z的最外层电子数比次外层少1。回答下列问题:
(1)W在周期表中的位置为_______ 。
(2)W、Y、Z形成的简单离子半径从大到小的顺序为_______ (用离子符号表示)。
(3)Y的最简单氢化物的电子式为_______ ,YZ3中所含化学键类型为_______ (填“离子键”或“共价键”)。
(4)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为_______ (填化学式)。
(5)实验室中制备Z单质的离子反应方程式为_______ 。
(1)W在周期表中的位置为
(2)W、Y、Z形成的简单离子半径从大到小的顺序为
(3)Y的最简单氢化物的电子式为
(4)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为
(5)实验室中制备Z单质的离子反应方程式为
您最近一年使用:0次
2021-07-08更新
|
101次组卷
|
2卷引用:河南省濮阳市元龙高级中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
4 . 有A、B、C、D、E五种元素,其原子序数依次递减,其中A元素的单质是一种有刺激性气味的深红棕色液体,B、C、D、E元素均为短周期元素,B原子核内的质子数正好等于D原子核内的质子数的2倍,而它们最外电子层上的电子数恰好相等。C元素能与D元素形成C2D和C2D2两种化合物,C单质与冷水能发生剧烈反应生成碱和可燃性气体,该气体为E的单质。请回答下列问题:
(1)A元素位于周期表中位置__ ,A的一种同位素含有46个中子,使用原子符号表示该核素__ 。
(2)C2D2的电子式是____ ,该固体中存在的化学键是___ 。
(3)A单质与冷的NaOH溶液反应的化学方程式是____ 。
(4)均由B、C、D、E四种元素形成的两种化合物在水溶液中反应的离子方程式____ 。
(1)A元素位于周期表中位置
(2)C2D2的电子式是
(3)A单质与冷的NaOH溶液反应的化学方程式是
(4)均由B、C、D、E四种元素形成的两种化合物在水溶液中反应的离子方程式
您最近一年使用:0次
2021-04-28更新
|
166次组卷
|
2卷引用:河南省濮阳市第一高级中学2021-2022学年高一下学期第一次质量检测化学试题



