解题方法
1 . 如图转化关系中,A、B、C、D是二元化合物,A与C均含有10个电子。甲、乙、丙是三种常见的非金属单质,下列说法不正确的是


| A.化合物A与丙可直接生成D |
| B.单质乙有多种同素异形体,均具有高熔点、高沸点、硬度大的性质 |
| C.稳定性:A<C |
| D.组成上述转化关系中的物质的元素种类共有三种 |
您最近半年使用:0次
名校
2 . 中国国家航天局探测发现火星富含四种短周期元素R、X、Y、Z原子半径依次增大。R是地壳中含量最多的元素,X、Y是同族元素,Y最外层电子数是次外层的一半,Y与Z的最外层电子数之和等于R的最外层电子数,下列判断正确的是
| A.Y是最早使用的半导体材料 | B.离子半径R<Z |
| C.简单气态氢化物的稳定性R<Y | D.Z的单质能通过置换反应生成X的单质 |
您最近半年使用:0次
2022-11-11更新
|
161次组卷
|
2卷引用:安徽省安庆市第二中学2022-2023学年高三上学期11月月考化学试题
解题方法
3 . W、X、Y、Z是原子序数依次增大的短周期主族元素,W与Z元素的原子序数之和等于X与Y元素的质子数之和,W是地壳中含量最多的元素,W与Z同主族,Y的氧化物具有两性。下列说法错误的是
A.原子半径: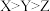 |
| B.W与X形成的化合物中都含离子键、共价键 |
| C.W与Z在自然界中均能以游离态存在 |
D.工业上电解熔融的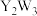 制备Y的单质 制备Y的单质 |
您最近半年使用:0次
解题方法
4 . D、E、X、Y、Z为原子序数依次增大的短周期主族元素,它们的简单氢化物分子的空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为_______ 。
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是_______ ,该元素的任意3种含氧酸的化学式为_______ 。
(3)D和Y形成的化合物,其分子的空间结构为_______ 。
(4)D和X形成的化合物,其化学键类型属于_______ (填“共价键”或“离子键”)。
(5)金属镁和E的单质在高温下反应得到的产物是_______ (写化学式)。该产物与水反应生成两种碱,反应的化学方程式是_______ 。
(1)Y的最高价氧化物的化学式为
(2)上述五种元素中,能形成酸性最强的含氧酸的元素是
(3)D和Y形成的化合物,其分子的空间结构为
(4)D和X形成的化合物,其化学键类型属于
(5)金属镁和E的单质在高温下反应得到的产物是
您最近半年使用:0次
名校
解题方法
5 . X、Y、Z、W、R为短周期的主族元素,其原子序数依次增大。Y、Z、W、R位于同一周期。X元素形成的单质是自然界中含量最多的气体,1molY的单质分别与足量盐酸和氢氧化钠溶液反应生成的气体在标准状况下均为33.6L。W的原子最外层电子数与核外电子总数之比为3:8,X的原子序数是Z的原子序数的一半。
(1)Z在元素周期表中的位置为____ ,W与R可形成原子个数比为1:2的化合物,其电子式为_____ 。
(2)经测定,在2.5×1.01×105Pa下,Y与R形成的化合物的熔点为190℃,沸点为180℃。且在熔融状态下不导电,则该化合物属于____ 化合物(“共价”或“离子”);工业上为了获得Y的单质,常采用电解的方法,写出电解的化学方程式_____ 。
(3)X、W、R元素的简单气态氢化物的沸点由高到低的顺序是____ (填化学式)。
(4)Y与W形成的化合物遇水分解,生成一种白色胶状沉淀和一种有毒气体,发生反应的化学方程式为____ 。
(1)Z在元素周期表中的位置为
(2)经测定,在2.5×1.01×105Pa下,Y与R形成的化合物的熔点为190℃,沸点为180℃。且在熔融状态下不导电,则该化合物属于
(3)X、W、R元素的简单气态氢化物的沸点由高到低的顺序是
(4)Y与W形成的化合物遇水分解,生成一种白色胶状沉淀和一种有毒气体,发生反应的化学方程式为
您最近半年使用:0次
名校
解题方法
6 . 某强氧化剂的结构如图所示,其中X、Y、Z三种元素原子序数均小于20,分别处于不同周期;Y、Z同主族且核外电子数之比为2:1。下列叙述正确的是
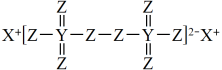
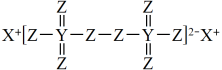
| A.离子半径:X>Y |
| B.简单氢化物热稳定性:Z>Y |
| C.该化合物中Z的化合价为—2 |
| D.该化合物中各元素原子均满足最外层8电子稳定结构 |
您最近半年使用:0次
解题方法
7 . 不同主族的短周期元素X、Y、Z、W其原子序数依次增大,X、Y的简单离子的电子层结构相同,短周期主族元素原子中Y的原子半径最大,Z原子最外层电子数是K层的3倍。下列说法错误的是
| A.熔化YW时离子键被破坏 |
| B.X的简单氢化物可作制冷剂 |
| C.简单离子的半径:Z>W |
| D.Y和Z形成的化合物一定为离子化合物,不含共价键 |
您最近半年使用:0次
8 . 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法不正确的是
| 元素 | X | Y | Z | W | |
| 最高价氧化物的水化物 | 分子式 | 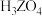 | |||
25℃时, 溶液对应的pH 溶液对应的pH | 1.00 | 13.00 | 1.57 | 0.70 | |
A. 用于汽车防撞气囊,含有两种类型的化学键 用于汽车防撞气囊,含有两种类型的化学键 |
B.简单氢化物分子内的键角: |
| C.足量的锌与W最高价氧化物的水化物的浓溶液充分反应,还原产物有2种 |
D.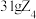 分子中含有 分子中含有 键 键 |
您最近半年使用:0次
名校
解题方法
9 . 已知X、Y、Z、W是原子序数依次增大的短周期主族元素,位于三个不同的周期。由X、Y、Z组成的某有机物常用于合成高分子化合物,其结构如图所示。W原子的最外层电子数比Z多。下列说法正确的是
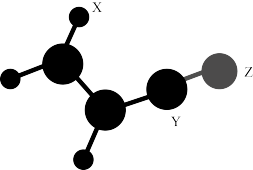

| A.原子半径W>Z>Y>X |
| B.Y、Z、W不可以组成各原子均满足8电子稳定结构的某种微粒 |
| C.Z的简单氢化物熔点高于Y的简单氢化物. |
| D.氧化物对应水化物的酸性:W一定比Z强 |
您最近半年使用:0次
名校
解题方法
10 . W、X、Y、Z为原子序数增大的短周期不同主族元素,W的简单氢化物可用作制冷剂。Y单质既能溶于强酸也能溶于强碱。Z的最外层电子数是W和X的最外层电子数之和。下列叙述不正确的是
| A.简单氢化物的沸点:W>Z |
| B.Z分别与X、Y组成的二元化合物中,化学键均为离子键 |
| C.简单离子的半径大小为:Z>W>X>Y |
| D.工业上常用电解熔融盐的方法制备X |
您最近半年使用:0次



