名校
解题方法
1 . A、B、C、D、E均为18电子分子,且均为前三周期主族元素的氢化物。A有臭鸡蛋气味;B和C均为四原子分子,B的水溶液常用于医用消毒;D为火箭推进器常用燃料,C和D中除氢外的另一种元素位于同一主族;E为烃。下列判断错误的是
| A.A分子中的化学键为σ键,有轴对称性,可以旋转 |
| B.B和E中均含有极性键和非极性键,两者均为非极性分子 |
| C.已知D可以和氢离子通过配位键形成阳离子,则反应前后中心原子杂化方式不变 |
| D.C分子中原子序数较大的元素可形成正四面体结构的单质分子,键角为109°28′ |
您最近半年使用:0次
名校
2 . 化合物X的结构如图所示,a、b、c、d是四种原子序数依次增大的短周期主族元素,基态时c原子2p原子轨道上有1对成对电子。下列说法正确的是
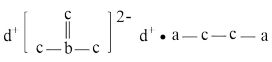
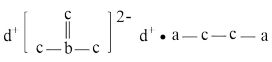
| A.X的水溶液呈碱性,不能使酸性高锰酸钾褪色 |
B.原子半径: |
C.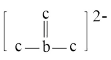 的结构中存在大 的结构中存在大 键,可表示为 键,可表示为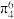 (用 (用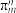 表示,m代表参与形成大 表示,m代表参与形成大 键的原子数,n代表参与形成大 键的原子数,n代表参与形成大 键的电子数) 键的电子数) |
D.电负性: |
您最近半年使用:0次
2023-02-06更新
|
229次组卷
|
5卷引用:湖南师范大学附属中学2022-2023学年高三上学期月考卷(六)化学试题
解题方法
3 . 一种用于合成治疗免疫疾病药的物质,结构如图所示,其中X、Y、Z、Q、W为1~20号元素且原子序数依次增大,Z与Q同主族,Q和W的简单离子具有相同的电子层结构。下列说法错误的是
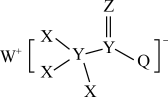

| A.原子半径:W>Q |
| B.Z的氢化物的熔点低于Q的氢化物的熔点 |
C.阴离子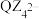 的VSEPR模型与其空间结构一致 的VSEPR模型与其空间结构一致 |
D.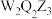 溶液与Q的最高价氧化物对应的水化物反应有黄色浑浊和无色气体 溶液与Q的最高价氧化物对应的水化物反应有黄色浑浊和无色气体 |
您最近半年使用:0次
4 . 已知A、B、C、D、E是原子序数依次增大的短周期主族元素,F是第四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号 完成下列空白:
①元素:A___________ 、D___________ 、F___________
②B、C两种元素第一电离能的大小关系为:___________
(2)元素F的基态价层电子排布式是:___________
(3)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________
(4)F元素位于周期表的___________ 区。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用
①元素:A
②B、C两种元素第一电离能的大小关系为:
(2)元素F的基态价层电子排布式是:
(3)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
电离能( ) ) | I1 | I2 | I3 | I4 | I5 |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近半年使用:0次
5 . 下图是元素周期表的一部分,所列的字母分别代表一种化学元素。试回答下列问题:
(1)基态n原子中,核外电子占据最高能层的符号是_______ ,占据该能层的电子云轮廓图形状为_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ 。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
①o元素价电子的轨道表示式为_______ 。
②比较两元素的 、
、 可知,气态
可知,气态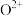 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为_______ (填元素符号)。
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式_______ 。
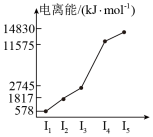
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
| 元素 | o | p | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
②比较两元素的
 、
、 可知,气态
可知,气态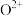 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式

您最近半年使用:0次
名校
6 . 矩周期元素X、Y、Z、W分属三个周期,且原子序数依次增大。其中Y与X、Z均可形成 或
或 的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是
的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是
 或
或 的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是
的二元化合物,X与Z最外层电子数相同,Y与W的一种化合物是一种新型的自来水消毒剂。下列说法中正确的是A.Y与X形成 化合物的电子式为: 化合物的电子式为: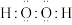 |
B.Y原子的电子排布图: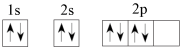 |
C.Z元素在周期表中的位置: 区、第三周期、第IA族 区、第三周期、第IA族 |
D.W原子价层电子排布式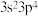 |
您最近半年使用:0次
2022-12-15更新
|
220次组卷
|
2卷引用:湖南省长沙市A佳教育联盟2022-2023学年高二上学期第三次月考化学试题
名校
解题方法
7 . 某物质的结构如图所示,W、X、Y、Z、M为原子序数依次增大的短周期元素,元素Z的原子序数是X原子最外层电子数的2倍。如果不慎将碱沾到皮肤上,应立即用大量的水冲洗,然后涂上W的最高价含氧酸的稀溶液。下列说法一定正确的是


| A.阴离子中所有原子均满足8电子结构 |
| B.上述元素中M元素最高价氧化物水化物的酸性最强 |
| C.上述5种元素中Z的简单气态氢化物稳定性不一定最强 |
| D.微粒半径r(Na+)>r(Y的简单阴离子) |
您最近半年使用:0次
解题方法
8 . 短周期主族元素X、Y、Z、W的原子序数依次增大,其中X是地壳中含量最多的元素,X原子的电子数与Y、Z、W原子的最外层电子数之和相等。Y、Z原子的最外层电子数之和与W的最外层电子数相等,且X、Y可形成两种常见的离子化合物,且晶体中的阴阳离子个数比均为1∶2,下列说法不正确的是
| A.工业上通常采用电解法制备Y和Z的单质 |
B.W和X形成的物质 是酸性氧化物,能与水反应生成W的最高价含氧酸 是酸性氧化物,能与水反应生成W的最高价含氧酸 |
| C.与水反应的剧烈程度:Y>Z |
| D.简单离子半径大小:X>Y>Z |
您最近半年使用:0次
名校
9 . 短周期主族非金属元素W、X、Y、Z的原子序数依次增大,由这四种元素形成的一种盐溶液,遇到FeCl3溶液呈现血红色,该盐溶液与NaOH在加热条件下会生成一种能使湿润的红色石蕊试纸变蓝的气体。下列说法不正确的是
| A.该盐的阳离子中含有配位键 |
| B.三价铁离子与该盐的阴离子形成了配离子而呈现血红色 |
| C.该盐的阳离子VSEPR模型名称与其空间结构名称相同 |
| D.电负性:Y>Z>W>X |
您最近半年使用:0次
名校
10 . 物质W常用作漂白剂和氧化剂,其组成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,实验室中常用CS2洗涤残留在试管壁上的N单质。下列说法正确的是
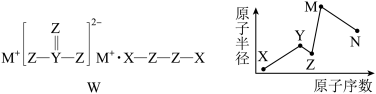
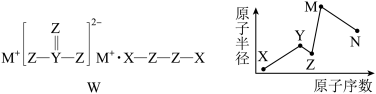
| A.X、Z形成的化合物与M、N形成的化合物不能发生氧化还原反应 |
| B.实验室中用CS2洗涤残留在试管壁上的N单质,利用了N单质的还原性 |
| C.Z的氢化物的沸点一定大于Y的氢化物的沸点 |
| D.化合物W常用作氧化剂,不宜在高温下使用 |
您最近半年使用:0次



