解题方法
1 . A、B、C、D、E、F为短周期元素.A的焰色反应为黄色,B的氢氧化物具有两性,C的原子最外层电子数是次外层电子数的2倍.D的原子最外层电子数是次外层电子数的3倍.E与D同主族,F的单质是黄绿色气体。
(1)B、F的元素符号分别为______ 、____ ;
(2)A、E两种元素按原子半径由大到小的顺序为______ (用元素符号填写);
(3)D元素氢化物的化学式为______ ;
(4)C的氧化物中能产生温室效应的是__________ (填化学式)。
(1)B、F的元素符号分别为
(2)A、E两种元素按原子半径由大到小的顺序为
(3)D元素氢化物的化学式为
(4)C的氧化物中能产生温室效应的是
您最近一年使用:0次
2 . 下表为元素周期表中的一部分,列出10种元素在元素周期表中的位置.用化学符号回答下列各问题.
(1)10种元素中,化学性质最不活泼的是_________ .
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是_________ .
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是_________ .
(4)元素⑦的简单氢化物的化学式为_____ ;若该氢化物和元素⑨的单质反应,则化学方程式为_______ .
(5)⑤和⑨的最高价氧化物对应水化物的化学式分别为_________ 和_________ .
(6)①和⑤最高价氧化物对应水化物相互反应的离子方程式为__________________ .
 族 族周期 |  |  |  | 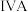 | 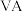 | 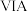 |  | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(1)10种元素中,化学性质最不活泼的是
(2)①、③、⑤三种元素最高价氧化物对应水化物中,碱性最强的是
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是
(4)元素⑦的简单氢化物的化学式为
(5)⑤和⑨的最高价氧化物对应水化物的化学式分别为
(6)①和⑤最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次
3 . 下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
回答下列问题:
(1)上述元素中②元素的名称_______ ;⑤元素在周期表中的位置是________ 。
(2)在③、⑦、⑧的气态氢化物中最稳定的是_____ (用化学式表示);⑦的最高价氧化物对应水化物的化学式是________ 。
(3)写出⑥的单质和④的最高价氧化物对应水化物的化学方程式是________ 。
(4)④、⑤是两种活泼性不同的金属,用事实来说明④比⑤活泼性更强________ 。
(5)由①和⑧组成的化合物极易溶于水,请设计简单的实验加以说明。写出简要的实验操作、现象和结论。__________________________ 。
族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | V A | Ⅵ A | Ⅶ A | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述元素中②元素的名称
(2)在③、⑦、⑧的气态氢化物中最稳定的是
(3)写出⑥的单质和④的最高价氧化物对应水化物的化学方程式是
(4)④、⑤是两种活泼性不同的金属,用事实来说明④比⑤活泼性更强
(5)由①和⑧组成的化合物极易溶于水,请设计简单的实验加以说明。写出简要的实验操作、现象和结论。
您最近一年使用:0次
解题方法
4 . W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次
2019-09-26更新
|
387次组卷
|
2卷引用:浙江省平阳县万全综合高级中学2022-2023学年高二下学期第一次月考化学试题
名校
5 . A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐X;D与A同主族,且与F同周期;F元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、F这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
请回答下列问题:
(1)写出B、C、E元素的名称B_________ 、C___________ 、E____________ ;
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为_______________ ;
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)_________________ ;
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为____________ 。
(5)A、C、D、F四种元素可以形成两种酸式盐 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为_____ 、______ ,这两种酸式盐相互反应的离子方程式为______________________ 。
请回答下列问题:
(1)写出B、C、E元素的名称B
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为
(5)A、C、D、F四种元素可以形成两种酸式盐
 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为
您最近一年使用:0次
2019-06-13更新
|
393次组卷
|
2卷引用:湖南省长沙市第一中学2020-2021学年高二上学期入学考试化学试题
名校
解题方法
6 . 有三种物质AC2(气体)、B2C2、AD4,元素A的最高正价和负价绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,火焰呈黄色,并生成淡黄色固体B2C2;元素D的负一价阴离子电子层结构与氩原子相同,则:
(1)AC2、AD4的化学式分别为______ 、______ 。
(2)AD4分子其中含有的σ键类型为_______ (填“s-s σ键”“s-p σ键”或“p-p σ键”)。
(3)D的负一价阴离子的电子排布式为_________ ,B2C2的电子式为__________ ,属___________ (填“离子化合物”或“共价化合物”)。
(4)写出一种与AC互为等电子体的分子______________
(1)AC2、AD4的化学式分别为
(2)AD4分子其中含有的σ键类型为
(3)D的负一价阴离子的电子排布式为
(4)写出一种与AC互为等电子体的分子
您最近一年使用:0次
2019-04-22更新
|
82次组卷
|
3卷引用:云南省景谷一中2018-2019学年高二下学期第一次月考化学试题
解题方法
7 . A,B为两种短周期元素,A的原子序数大于B,且B原子的最外层电子数为A原子最外层电子数的3倍。A,B形成的化合物是中学化学常见的化合物,该化合物熔融时能导电。试回答下列问题:
(1)A,B的元素符号分别是________ 、________ 。
(2)用电子式表示A,B元素形成化合物的过程___________________________________________________ 。
(3)A,B所形成的化合物的晶体结构与氯化钠晶体结构相似,则每个阳离子周围吸引了________ 个阴离子;晶体中阴、阳离子数之比为________ 。
(4)A,B所形成化合物的晶体的熔点比NaF晶体的熔点________ ,其判断的理由是
________________________________________________________________________ 。
(1)A,B的元素符号分别是
(2)用电子式表示A,B元素形成化合物的过程
(3)A,B所形成的化合物的晶体结构与氯化钠晶体结构相似,则每个阳离子周围吸引了
(4)A,B所形成化合物的晶体的熔点比NaF晶体的熔点
您最近一年使用:0次
2019-02-26更新
|
162次组卷
|
2卷引用:云南省玉溪市江川区第二中学2018-2019学年高二上学期期末考试化学试题
解题方法
8 . 现有原子序数之和为51的5种短周期元素A,B,C,D,E。已知A的单质在常温下为无色气体;B原子的最外层电子数比次外层电子数多3个;C和B属于同一主族;D的最高正价与负价的代数和为4,其最高价氧化物对应的水化物的酸性在同主族元素中最强,E元素最外层电子数与其K层电子数相同。
(1)试写出它们的元素符号。__________________________________________ 。
(2)写出B的氢化物的电子式_____________________________ 。
(3)由A、D两种元素形成的化合物是________ 化合物(填“离子”或“共价”),化合物内存在________ 键(填“离子”或“共价”)。
(4)由D、E两种元素形成的化合物的电子式为________ ,它属于________ 化合物,化合物内存在________ 键。
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是________ (多选)。
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
(1)试写出它们的元素符号。
(2)写出B的氢化物的电子式
(3)由A、D两种元素形成的化合物是
(4)由D、E两种元素形成的化合物的电子式为
(5)下列关于A,B,C,D,E 5种元素形成的物质的有关叙述正确的是
a.A,B,C,D都能通过共价键形成单质,其中B形成的单质性质最稳定,是因为其原子半径最小
b.A,B,D 3种元素为非金属元素,它们共同组成的化合物一定是共价化合物
c.B,E形成的化合物E3B2应为离子化合物
d.5种元素两两组合形成的化合物中既有共价化合物,又有离子化合物
e.5种元素形成简单离子的离子半径大小为C>D>B>E>A
您最近一年使用:0次
解题方法
9 . A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第________ 周期第________ 族。
(2)E元素形成的氧化物对应的水化物的化学式为____________________ 。
(3)元素C、D、E形成的简单离子半径大小关系是______ >______ >_____ (用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:____________________ 。C、D还可形成化合物D2C2,D2C2中含有的化学键是________________________ 。
(1)B在周期表中的位置为第
(2)E元素形成的氧化物对应的水化物的化学式为
(3)元素C、D、E形成的简单离子半径大小关系是
(4)用电子式表示化合物D2C的形成过程:
您最近一年使用:0次
解题方法
10 . 下表中①~⑦表示元素周期表的部分元素。
(1)②元素最外层电子数比次外层电子数多______ 个,该元素的符号是_______ ;⑦元素的氢化物的电子式为____________________ 。
(2)由①③④三种元素组成的物质是______________ ,此物质的水溶液显_____ 性。
(3)⑥元素的原子半径大于③的理由是____________________________________ 。
(4)④元素的最高价氧化物对应的水化物的碱性强于⑤元素,用一个化学方程式来证明。________________________________________
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 1 | |||||||
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)②元素最外层电子数比次外层电子数多
(2)由①③④三种元素组成的物质是
(3)⑥元素的原子半径大于③的理由是
(4)④元素的最高价氧化物对应的水化物的碱性强于⑤元素,用一个化学方程式来证明。
您最近一年使用:0次



