1 . 回答下列问题
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦ ;能导电的是
;能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)在离子 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是___________ 。
(3)用___________ 方法将植物油和水的混合体系分离;用___________ 方法分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合液体(四氯化碳和甲苯互溶)。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打( ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:___________ ;此时最好用含氢氧化铝的胃药(如胃舒平)离子方程式:___________ 。
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦
 ;能导电的是
;能导电的是(2)在离子
 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是(3)用
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(
 ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:
您最近一年使用:0次
解题方法
2 . 下列理论或实验能说明原子核外电子是分层排布的是
| A.道尔顿的原子论 | B.汤姆孙的阴极射线实验 |
| C.玻尔的氢原子光谱实验 | D.卢瑟福α粒子的散射实验 |
您最近一年使用:0次
真题
解题方法
3 . 利用18O示踪技术研究H2O2与Cl2的反应历程,结果如下:
①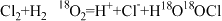
②
下列叙述正确的是
①
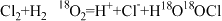
②

下列叙述正确的是
| A.反应①是置换反应 |
| B.18O的核电荷数是18 |
| C.18O与16O互为同素异形体 |
D.反应历程中 中的O-O键未发生断裂 中的O-O键未发生断裂 |
您最近一年使用:0次
4 . 推理是学习化学的一种方法,以下推理正确的是
| A.溶液一定是均一稳定的,但均一稳定的物质不一定是溶液 |
| B.利用红磷燃烧可测定空气中氧气的含量,铁丝的燃烧,也可以测定空气中氧气的含量 |
| C.二氧化锰可以加快过氧化氢分解速率,所以二氧化锰可以做任何化学反应的催化剂 |
| D.原子核是由质子和中子构成的,所以任何原子的原子核内部都含有质子和中子 |
您最近一年使用:0次
解题方法
5 . 氨硼烷 是一种新型储氢材料,分子中与
是一种新型储氢材料,分子中与 原子相连的
原子相连的 原子呈正电性,与
原子呈正电性,与 原子相连的
原子相连的 原子呈负催化剂电性。氨硼烷与水发生如下反应:
原子呈负催化剂电性。氨硼烷与水发生如下反应: 。下列说法正确的是
。下列说法正确的是
 是一种新型储氢材料,分子中与
是一种新型储氢材料,分子中与 原子相连的
原子相连的 原子呈正电性,与
原子呈正电性,与 原子相连的
原子相连的 原子呈负催化剂电性。氨硼烷与水发生如下反应:
原子呈负催化剂电性。氨硼烷与水发生如下反应: 。下列说法正确的是
。下列说法正确的是A.中子数为 的 的 原子: 原子: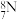 |
B.基态原子第一电离能由大到小: |
C.反应前后 原子均采用 原子均采用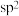 杂化 杂化 |
| D.氨硼烷中两种氢原子之间存在相互吸引作用 |
您最近一年使用:0次
解题方法
6 . 许多元素有多种核素,而且各种核素在自然界中所占的比例相对固定,其中氢元素有 、
、 、
、 三种核素,钛元素有
三种核素,钛元素有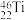 、
、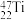 、
、 、
、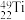 、
、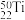 五种核素,有关核素的说法错误的是
五种核素,有关核素的说法错误的是
 、
、 、
、 三种核素,钛元素有
三种核素,钛元素有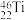 、
、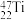 、
、 、
、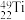 、
、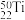 五种核素,有关核素的说法错误的是
五种核素,有关核素的说法错误的是A. 、 、 、 、 三种核素与 三种核素与 最多可以形成6种不同的水分子 最多可以形成6种不同的水分子 |
B.放射性的氡(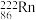 )内中子数与质子数之差为136 )内中子数与质子数之差为136 |
C.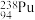 与 与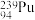 具有相同的最外层电子数 具有相同的最外层电子数 |
| D.钛元素的相对原子质量介于46~50之间 |
您最近一年使用:0次
名校
7 . 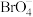 制备过程描述如下:
制备过程描述如下: ,以下说法正确的是
,以下说法正确的是
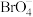 制备过程描述如下:
制备过程描述如下: ,以下说法正确的是
,以下说法正确的是| A.该过程发生了化学变化 | B.Br元素的质量数为83 |
C.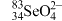 中含有68个电子 中含有68个电子 | D. 与 与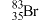 互为同位素 互为同位素 |
您最近一年使用:0次
2024-02-29更新
|
97次组卷
|
2卷引用:上海市七宝中学2023-2024学年高一上学期化学12月练习卷
名校
8 . 2023年8月,日本排放的核废水中含有氚(3H)、碳14C、钚(94Pu)等多种放射性元素,下列说法正确的是
| A.3H、3He互为同位素 |
| B.14CO、14CO2互为同素异形体 |
| C.考古时可利用14C测定一些文物的年代 |
D.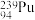 与 与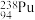 的原子核外电子排布不同 的原子核外电子排布不同 |
您最近一年使用:0次
2024-02-04更新
|
155次组卷
|
2卷引用:四川省达州市2023-2024学年高一上学期期末监测化学试题
解题方法
9 . 科研发现,高压电极之间在放电间隙处会产生微放电, 被分解为自由态的
被分解为自由态的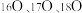 ,部分自由态的
,部分自由态的 与末分解的
与末分解的 重新结合生成
重新结合生成 。下列说法错误的是
。下列说法错误的是
 被分解为自由态的
被分解为自由态的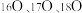 ,部分自由态的
,部分自由态的 与末分解的
与末分解的 重新结合生成
重新结合生成 。下列说法错误的是
。下列说法错误的是A.核素 的中子数为9 的中子数为9 | B.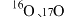 和 和 互为同位素 互为同位素 |
C. 和 和 是氧元素的同素异形体 是氧元素的同素异形体 | D.上述生成 的过程属于物理变化 的过程属于物理变化 |
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.根据所学知识,完成下列问题
(1)元素周期表的主要发现者是谁?_______
(2)关于俄罗斯科学家找到的第119号元素,下列说法正确的是_______
(3)格致中学前身格致书院的创始人之一徐寿把化学元素译成汉字,作为这个元素的汉字名称。Ts是第117号元素的缩写,汉字名称为“石田”,其中对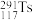 中数字的叙述正确的是_______
中数字的叙述正确的是_______
Ⅱ.下表是元素周期表的一部分,表中的每个编号表示一种元素。根据下表回答题:
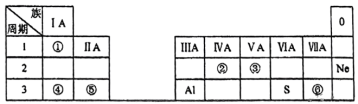
(4)元素⑥在元素周期表中的位置是___________ ,其最高价氧化物的水化物酸性与 的酸性相比,
的酸性相比,___________ (填写化学式)更强。
(5)元素②的原子结构示意图是___________ 。
(6)元素③最简单氢化物的电子式是___________ 。
(7)比较④和⑤两种元素的金属性:④___________ ⑤(选填“<”或“>”),以下能够用于判断④和⑤金属性强弱关系的依据是___________ 。
A.相同条件下,比较两者与水反应的难易程度 B.比较两者的电子层数
C.比较两者的气态氢化物稳定性 D.比较两者最高价氧化物水化物碱性
(1)元素周期表的主要发现者是谁?_______
| A.道尔顿 | B.门捷列夫 | C.阿伏伽德罗 | D.凯库勒 |
| A.该元素原子的质量数为119 | B.119号元素的原子一定含119个中子 |
| C.该元素的原子量可能为119 | D.119号元素应在周期表第ⅠA族 |
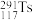 中数字的叙述正确的是_______
中数字的叙述正确的是_______| A.291是Ts元素的相对原子质量 | B.291是Ts元素的质量数 |
C.117是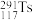 的质子数 的质子数 | D.117是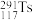 的中子数 的中子数 |
Ⅱ.下表是元素周期表的一部分,表中的每个编号表示一种元素。根据下表回答题:

(4)元素⑥在元素周期表中的位置是
 的酸性相比,
的酸性相比,(5)元素②的原子结构示意图是
(6)元素③最简单氢化物的电子式是
(7)比较④和⑤两种元素的金属性:④
A.相同条件下,比较两者与水反应的难易程度 B.比较两者的电子层数
C.比较两者的气态氢化物稳定性 D.比较两者最高价氧化物水化物碱性
您最近一年使用:0次



