16. 工业上以硫黄为原料制备硫酸的原理示意图如下,其过程包括Ⅰ、Ⅱ、Ⅲ三个阶段。

Ⅰ.硫液化后与空气中的氧反应生成SO
2。
(1)

的晶体类型是
______。
(2)第一步时,硫粉液化并与氧气共热生成二氧化硫。若反应温度超过硫粉沸点,部分硫粉会转化为硫蒸气,与生成的二氧化硫一同参加第二步反应,关于这种情况说法正确的是
______。(填序号)
a.硫粉消耗会增大 b.二氧化硫生成率降低 c.生成较多SO
2(3)若每生成
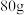
气体三氧化硫,放出
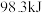
能量,写出生成三氧化硫的反应的热化学方程式:
______,若反应温度升高,则二氧化硫转化率
______(填“升高”或“降低”)。
(4)从能量角度分析,钒催化剂在反应中的作用为
______。
Ⅱ.一定条件下,钒催化剂的活性温度范围是450~600℃。为了兼顾转化率和反应速率,可采用四段转化工艺:预热后的SO
2和O
2通过第一段的钒催化剂层进行催化氧化,气体温度会迅速接近600℃,此时立即将气体通过热交换器,将热量传递给需要预热的SO
2和O
2,完成第一段转化。降温后的气体依次进行后三段转化,温度逐段降低,总转化率逐段提高,接近平衡转化率。最终反应在450℃左右时,SO
2转化率达到97%。
(5)气体经过每段的钒催化剂层,温度都会升高,其原因是
______,升高温度后的气体都需要降温,其目的是
______(6)采用四段转化工艺可以实现
______(填序号)。
a.控制适宜的温度,尽量加快反应速率,尽可能提高SO
2转化率
b.使反应达到平衡状态
c.节约能源
Ⅲ.工业上用浓硫酸吸收SO
3.若用水吸收SO
3会产生酸雾,导致吸收效率降低。
(7)SO
3的吸收率与所用硫酸的浓度、温度的关系如图所示。

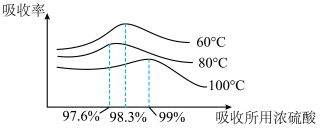
据图分析,最适合的吸收条件;硫酸的浓度
______,温度
______。
(8)一批32吨含硫元素

的硫粉,参加反应,在第一步反应中硫元素损失了

,二氧化硫在第二步反应中

转化为了三氧化硫,三氧化硫在第三步反应中被吸收时,视作全部吸收,那么这批硫粉总计可以生产

的浓硫酸
______吨。