名校
1 . 完成表格
(1)①_______ ②_______ ③_______ ④_______
(2)①_______ ②_______
(3)①_______ ②_______
(4)①_______ ② _______
(5)①_______ ②_______ ③_______
| 小题序号 | 化学符号 | 质子数 | 中子数 | 电子数 | 质量数 |
| (1) |  C C | ①_______ | ②_______ | ③_______ | ④_______ |
| (2) | ①_______ | 8 | 10 | 10 | ②_______ |
| (3) | ①_______ | 12 | 12 | 10 | ②_______ |
| (4) | H3O+ | ①_______ | / | ②_______ | / |
| (5) | TD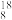 O O | ①_______ | ②_______ | ③_______ | / |
(1)①
(2)①
(3)①
(4)①
(5)①
您最近一年使用:0次
名校
解题方法
2 . 2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水。该核废水中含有以目前技术手段无法去除的放射性物质“氚”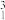 H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)
H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)
(1)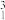 H与
H与 H互为
H互为___ 。
(2)数字3表示___ 。
(3)氢元素的相对原子质量计算表达式___ 。(氕、氘、氚原子的质量用m1,m2,m3表示,C—12原子质量用m0表示)。
(4)碳也有一种放射性核素14C,举出一种该核素的应用___ 。
(5)该两种核素形成的化合物14C3H4中化学键为__ ;空间构型__ ;用电子式表示该化合物的形成过程___ 。
(6)6.5g该两种核素形成的化合物14C3H4,在标况下的体积为___ L;其中所含的质子为___ mol,中子为___ 个。
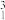 H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)
H。(天然氢元素中:氕,丰度为99.98%;氘,丰度0.016%;氚,丰度0.004%。)(1)
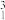 H与
H与 H互为
H互为(2)数字3表示
(3)氢元素的相对原子质量计算表达式
(4)碳也有一种放射性核素14C,举出一种该核素的应用
(5)该两种核素形成的化合物14C3H4中化学键为
(6)6.5g该两种核素形成的化合物14C3H4,在标况下的体积为
您最近一年使用:0次
名校
3 . 按要求填空。
(1)33.3g某金属氯化物 中含有
中含有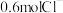 ,则M的相对原子质量为
,则M的相对原子质量为_______ 。
(2)标准状况下,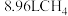 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为_______ L, 的质量为
的质量为_______ g。
(3) 个
个 约含
约含_______ 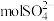 ,其质量为
,其质量为_______ g。
(4)中子数为18的硫原子,其微粒符号可表示为_______ 。
(5)质量数为37、中子数为20的原子,其结构示意图可表示为_______ 。
(6)已知Mm+的电子数为a,M的质量数为A,则 的M的中子数为
的M的中子数为_______ 。
(1)33.3g某金属氯化物
 中含有
中含有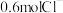 ,则M的相对原子质量为
,则M的相对原子质量为(2)标准状况下,
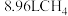 和
和 的混合气体,其质量为7.6g,则混合气体中
的混合气体,其质量为7.6g,则混合气体中 的体积为
的体积为 的质量为
的质量为(3)
 个
个 约含
约含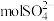 ,其质量为
,其质量为(4)中子数为18的硫原子,其微粒符号可表示为
(5)质量数为37、中子数为20的原子,其结构示意图可表示为
(6)已知Mm+的电子数为a,M的质量数为A,则
 的M的中子数为
的M的中子数为
您最近一年使用:0次
2023-08-08更新
|
152次组卷
|
2卷引用:福建省福州市八县市协作校2022-2023学年高一上学期期中联考化学试题
名校
解题方法
4 . 回答下列问题:
(1)填表,完成下列表格
(2)某微粒的结构示意图可表示为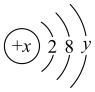 。
。
①当x=10+y时,该粒子为___________ (填“原子”“正离子”或“负离子”),当x<10+y时,该粒子为___________ 。
②当y=8时,若该微粒带有一个单位负电荷,则x=___________ ,该微粒的离子符号为___________ 。
③当y=5时,若该微粒为中性原子R,其质量数为31,则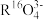 中含有的中子数为
中含有的中子数为___________ 。
(1)填表,完成下列表格
| 微粒名称 | 微粒结构示意图 | 电子式 |
| 硫离子 | ||
| 氩原子 | ||
| 镁离子 |
(2)某微粒的结构示意图可表示为
 。
。①当x=10+y时,该粒子为
②当y=8时,若该微粒带有一个单位负电荷,则x=
③当y=5时,若该微粒为中性原子R,其质量数为31,则
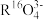 中含有的中子数为
中含有的中子数为
您最近一年使用:0次
5 . 回答下列问题。
(1)仔细观察下图的微观反应过程,写出该化学反应方程式___________ 。
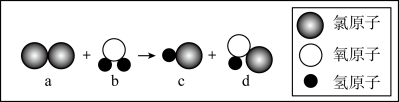
(2)画出氧原子的结构示意图___________ 。
(3)电解水时,为增强水的导电性,通常向纯水中加入适量的NaOH(NaOH不参加反应)。
①某电解水实验开始时,向180g纯水中溶解了4g NaOH.此时溶液中 和水分子的个数比是
和水分子的个数比是___________ 。
②当实验进行到一段时间,两个电极共收集到的气体折合成标准状况约是6.72L(不考虑气体溶解)。计算此时被电解的水的物质的量是___________ 。
③实际收集气体的外界条件并非标况。假如该条件下气体摩尔体积是C L/mol,阿伏伽德罗常数的值是 ,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是
,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是___________ 。
(1)仔细观察下图的微观反应过程,写出该化学反应方程式

(2)画出氧原子的结构示意图
(3)电解水时,为增强水的导电性,通常向纯水中加入适量的NaOH(NaOH不参加反应)。
①某电解水实验开始时,向180g纯水中溶解了4g NaOH.此时溶液中
 和水分子的个数比是
和水分子的个数比是②当实验进行到一段时间,两个电极共收集到的气体折合成标准状况约是6.72L(不考虑气体溶解)。计算此时被电解的水的物质的量是
③实际收集气体的外界条件并非标况。假如该条件下气体摩尔体积是C L/mol,阿伏伽德罗常数的值是
 ,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是
,当收集到氢气的体积是V L时,则同时收集到的氧气分子的个数是
您最近一年使用:0次
名校
解题方法
6 . 某种微粒的结构示意图为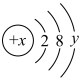 ,试回答下列问题:
,试回答下列问题:
(1)结构示意图中的“x”表示_______ ,结构示意图中的“y”表示_______ ,y的数值和微粒的电子层数共同决定了该微粒的_______ 。
(2)若x-y=10,则由该结构示意图推知该微粒是_______ (选填“原子”或“离子”)。
(3)若y=8,且该微粒带有2个单位负电荷,则该微粒符号的化学式为_______ ,该微粒的电子式为_______ 。
 ,试回答下列问题:
,试回答下列问题:(1)结构示意图中的“x”表示
(2)若x-y=10,则由该结构示意图推知该微粒是
(3)若y=8,且该微粒带有2个单位负电荷,则该微粒符号的化学式为
您最近一年使用:0次
名校
解题方法
7 . 在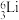 、
、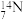 、
、 、
、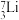 、
、 、
、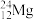 中
中
(1)互为同位素的是_______ 和_______ 。
(2)质量数相等,但不能互称同位素的是_______ 和_______ 。
(3)中子数相等,但质子数不相等的是_______ 和_______ 。
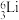 、
、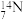 、
、 、
、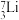 、
、 、
、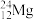 中
中(1)互为同位素的是
(2)质量数相等,但不能互称同位素的是
(3)中子数相等,但质子数不相等的是
您最近一年使用:0次
名校
8 . (1)微粒AXn-核外有18个电子,则它的核电荷数为________ ,核内中子数为_______ 。
(2)由1H216O与2H217O所代表的物质中,共有__________ 种元素,_________ 种原子,16O、17O的关系为________ 。
(3)已知:碳元素有12C、13C、14C;氧元素有16O、18O,则它们能够形成______ 种CO2分子。
(2)由1H216O与2H217O所代表的物质中,共有
(3)已知:碳元素有12C、13C、14C;氧元素有16O、18O,则它们能够形成
您最近一年使用:0次
名校
解题方法
9 . 地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)___________ ;
(2)由极性键构成的非极性分子有___________ ;
(3)与 可直接形成配位键的分子有
可直接形成配位键的分子有___________ ;
(4)分子中不含孤电子对的分子有___________ ,它的立体构型为___________ ;
(5)极易溶于水、且水溶液呈碱性的物质的分子是___________ ,它极易溶于水的原因是___________ 。
| 目前空气的成分 |  、 、 、 、 、水蒸气及稀有气体(如He、Ne等) 、水蒸气及稀有气体(如He、Ne等) |
| 原始大气的主要成分 |  、 、 、CO、 、CO、 等 等 |
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)
(2)由极性键构成的非极性分子有
(3)与
 可直接形成配位键的分子有
可直接形成配位键的分子有(4)分子中不含孤电子对的分子有
(5)极易溶于水、且水溶液呈碱性的物质的分子是
您最近一年使用:0次
2023-05-08更新
|
59次组卷
|
2卷引用:四川省巴中市恩阳区2022-2023学年高二下学期4月期中考试化学试题
解题方法
10 . 英国物理学家E·卢瑟福领导的科研小组在1911年通过α粒子散射实验提出了新的原子结构模型,标志着人类对原子结构的认识进入了新阶段。
(1)卢瑟福团队用到α粒子( He2+)来轰击金箔,该化学符号中4代表的含义是
He2+)来轰击金箔,该化学符号中4代表的含义是___ ;在1-18号元素中,最外层电子数与氦原子相等的元素是___ 。
(2)氦元素在自然界中仅有3He和4He两种原子,它们具有相同的___ 。
A.质子数 B.中子数 C.物理性质 D.化学性质
表中是来文献当中关于氮元素的相关记载,其中的“99.999863%”表示的是__ ,“4.002602”表示的是___ 。
(3)关于α粒子散射实验现象的记载如下:____①____的α粒子都且按穿过金箔,____②___的α粒子发生偏转,____③____的α粒子甚至被直接反弹回去。①②③三处空格分别为___ 。
A.绝大多数,极少数,个别 B.别,极少数,绝大多数
C.几乎半数,几乎半数,个别 D.个别,几乎半数,几乎半数
通过该试验,卢瑟福得出了原子结构的___ 模型。
(1)卢瑟福团队用到α粒子(
 He2+)来轰击金箔,该化学符号中4代表的含义是
He2+)来轰击金箔,该化学符号中4代表的含义是(2)氦元素在自然界中仅有3He和4He两种原子,它们具有相同的
A.质子数 B.中子数 C.物理性质 D.化学性质
表中是来文献当中关于氮元素的相关记载,其中的“99.999863%”表示的是
| 3He | 3.016010 | 0.000137% |
| 4He | 4.002603 | 99.999863% |
| 平均 | 4.002602 | |
(3)关于α粒子散射实验现象的记载如下:____①____的α粒子都且按穿过金箔,____②___的α粒子发生偏转,____③____的α粒子甚至被直接反弹回去。①②③三处空格分别为
A.绝大多数,极少数,个别 B.别,极少数,绝大多数
C.几乎半数,几乎半数,个别 D.个别,几乎半数,几乎半数
通过该试验,卢瑟福得出了原子结构的
您最近一年使用:0次



