1 . 硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为_______ ,Si原子的电子式为_______ 。Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(2)如图中,“28.09”的含义是指_______ 。
(3)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。0.1mol的硅酸根离子( )中含有质子
)中含有质子_______ mol,电子_______ 个。
(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”)。
iii.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为(2)如图中,“28.09”的含义是指
| 14 Si 硅 28.09 |
 )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 )中含有质子
)中含有质子(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为
ii.流程①焦炭体现了
iii.流程④的化学反应为置换反应,写出其化学方程式:
您最近一年使用:0次
名校
解题方法
2 . 研究物质的微观结构和元素组成,并用恰当的化学用语进行表达,能帮助我们揭示物质变化的本质,发现物质变化的规律。
(1)下图是部分元素原子或离子的结构示意图.请你仔细观察、分析,用序号填空:
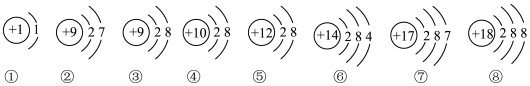
①上述粒子中,属于稀有气体元素的原子是_____________ ;
②在化学反应中容易得到电子的是_____________ ;
③属于正离子的是_____________ ;
④表示 的是
的是_____________ ;
⑤属于同一种元素的是_____________ ;
⑥属于非金属元素的是_____________ ;
⑦电子层数相同、最外层电子数也相同的粒子有_____________ .
(2)卤族元素F和 具有相似的化学性质,其原因是它们的原子具有相同的
具有相似的化学性质,其原因是它们的原子具有相同的
(3)写出铝离子的结构示意图①_____________ ,其核外能量最高的电子层符号为②___________ 。
(4)两种微粒的电子数相同,质子数不同,则它们可能是
①两种不同的原子;②两种不同的离子;③同一种元素的原子和离子;④不同元素的原子和离子
(5)在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与 层相同,当它作为原子的次外层时,其电子数比
层相同,当它作为原子的次外层时,其电子数比 层最少能多10个,则此电子层是
层最少能多10个,则此电子层是
(6)一瓶气体经分析只含一种元素,则该气体
(7)下列物质变化过程不会破坏化学键的是
(8)下列关于化学键的说法正确的是
(9) 的电子式是
的电子式是_____________ 。
(10)请用电子式表示 的形成过程
的形成过程_____________ 。
(1)下图是部分元素原子或离子的结构示意图.请你仔细观察、分析,用序号填空:

①上述粒子中,属于稀有气体元素的原子是
②在化学反应中容易得到电子的是
③属于正离子的是
④表示
 的是
的是⑤属于同一种元素的是
⑥属于非金属元素的是
⑦电子层数相同、最外层电子数也相同的粒子有
(2)卤族元素F和
 具有相似的化学性质,其原因是它们的原子具有相同的
具有相似的化学性质,其原因是它们的原子具有相同的 | A.电子层数 | B.核外电子数 | C.最外层电子数 | D.原子半径 |
(3)写出铝离子的结构示意图①
(4)两种微粒的电子数相同,质子数不同,则它们可能是
①两种不同的原子;②两种不同的离子;③同一种元素的原子和离子;④不同元素的原子和离子
| A.①和④ | B.②和③ | C.①和③ | D.②和④ |
(5)在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与
 层相同,当它作为原子的次外层时,其电子数比
层相同,当它作为原子的次外层时,其电子数比 层最少能多10个,则此电子层是
层最少能多10个,则此电子层是 | A.K层 | B.M层 | C.L层 | D.N层 |
(6)一瓶气体经分析只含一种元素,则该气体
| A.一定是单质 | B.可能是化合物 |
| C.可能是几种单质的混合物 | D.可能是化合物与单质的混合物 |
(7)下列物质变化过程不会破坏化学键的是
| A.水气化为水蒸气 | B.水蒸气在高温下分解为氢气和氧气 |
| C.氯化钠溶于水 | D.氯化钠熔化 |
(8)下列关于化学键的说法正确的是
| A.破坏化学键会放出能量 | B.所有物质中都存在化学键 |
| C.金属元素和非金属元素间一定形成离子键 | D.离子化合物中不一定含有金属元素 |
(9)
 的电子式是
的电子式是(10)请用电子式表示
 的形成过程
的形成过程
您最近一年使用:0次
解题方法
3 . 下面是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:
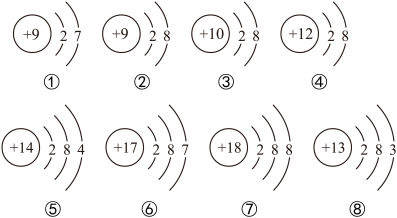
(1)上述微粒中属于同种元素的是_______ (填序号,下同),属于阳离子的是_______ ,属于原子的是_______ 。
(2)电子层数相同,最外层电子数也相同的微粒有_______ 。
(3)属于稀有气体元素的有_______ 。
(4)通过上图还可总结出原子和离子的一些区别,请写出其中两个:_______ 、_______

(1)上述微粒中属于同种元素的是
(2)电子层数相同,最外层电子数也相同的微粒有
(3)属于稀有气体元素的有
(4)通过上图还可总结出原子和离子的一些区别,请写出其中两个:
您最近一年使用:0次
名校
4 . 某微粒A的结构示意图如下:
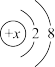
(1)若X=8,则此阴离子与图中带一个正电荷的阳离子形成一种常见化合物的化学式是_______ 。
(2)1mol微粒A含有10mol电子,下列微粒各1mol,也含有10mol电子的有:_______ (填序号)
①CH4②H2O2③HF④Al3+⑤Cl-⑥
(3)若A的阳离子为An+且质量数为a,则其质子数为_______ ,中子数为_______ (用含有a,n的代数式表达)
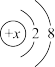
(1)若X=8,则此阴离子与图中带一个正电荷的阳离子形成一种常见化合物的化学式是
(2)1mol微粒A含有10mol电子,下列微粒各1mol,也含有10mol电子的有:
①CH4②H2O2③HF④Al3+⑤Cl-⑥

(3)若A的阳离子为An+且质量数为a,则其质子数为
您最近一年使用:0次
18-19高二·浙江·期中
解题方法
5 . 请完成下列问题:
(1)画出氯离子结构示意图______________ ;
(2)写出小苏打的化学式________________ ;
(3)写出工业炼铁的化学方程式_____________________ ;
(4)写出红热的木炭与浓硫酸反应的化学方程式_________________________________ 。
(1)画出氯离子结构示意图
(2)写出小苏打的化学式
(3)写出工业炼铁的化学方程式
(4)写出红热的木炭与浓硫酸反应的化学方程式
您最近一年使用:0次
名校
6 . 钋(Po)是一种低熔点金属,极其稀有,毒性和放射性极强。回答下列问题:
(1) Po具有放射性,经
Po具有放射性,经 衰变成稳定的铅,在衰变过程中释放一个
衰变成稳定的铅,在衰变过程中释放一个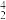 He2+,Pb的原子核中质子数为
He2+,Pb的原子核中质子数为____ ,中子数为____ ,Po元素能形成较稳定的+4价离子,wg Po4+含有的电子的物质的量为
Po4+含有的电子的物质的量为____ ;
(2)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间,已知 Po的半衰期为138天,质量为64克的
Po的半衰期为138天,质量为64克的 Po,经276天后,得到铅的质量为
Po,经276天后,得到铅的质量为____ 。
(1)
 Po具有放射性,经
Po具有放射性,经 衰变成稳定的铅,在衰变过程中释放一个
衰变成稳定的铅,在衰变过程中释放一个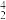 He2+,Pb的原子核中质子数为
He2+,Pb的原子核中质子数为 Po4+含有的电子的物质的量为
Po4+含有的电子的物质的量为(2)半衰期是指由大量原子组成的放射性样品中,放射性元素原子核有50%发生衰变所需的时间,已知
 Po的半衰期为138天,质量为64克的
Po的半衰期为138天,质量为64克的 Po,经276天后,得到铅的质量为
Po,经276天后,得到铅的质量为
您最近一年使用:0次
2019-10-30更新
|
233次组卷
|
2卷引用:上海交通大学附属中学2016-2017学年高一上学期期中考试化学试题2
名校
解题方法
7 . 有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到淡黄色固态化合物,D的M层电子数为K层电子数的3倍.试根据以上叙述回答:
(1)写出元素名称:A_____ D_____ ;
(2)画出D的原子结构示意图____________ ;
(3)用电子式表示化合物C2D的形成过程___________________ .
(1)写出元素名称:A
(2)画出D的原子结构示意图
(3)用电子式表示化合物C2D的形成过程
您最近一年使用:0次
2016-12-09更新
|
311次组卷
|
5卷引用:2015-2016学年宁夏银川九中高一下学期期中考试化学试卷
解题方法
8 . (1)某元素M,其离子M2+,M2+原子核核内有20个中子,核外有18个电子,则M的质子数是__________ ,质量数是_________
(2)根据下列叙述,写出微粒符号和结构示意图。
a.原子核外有2个电子层,核外有10个电子的原子________ 、______________ ;
b.质量数为24,质子数等于中子数的原子_________ 、__________________ ;
c.最外层电子数是次外层电子数的4倍的二价阴离子_________ 、_________________ 。
(3)结构示意图为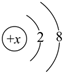 的阳离子,其电子式符号可能为
的阳离子,其电子式符号可能为________ 、________ 、________ 。
(2)根据下列叙述,写出微粒符号和结构示意图。
a.原子核外有2个电子层,核外有10个电子的原子
b.质量数为24,质子数等于中子数的原子
c.最外层电子数是次外层电子数的4倍的二价阴离子
(3)结构示意图为
 的阳离子,其电子式符号可能为
的阳离子,其电子式符号可能为
您最近一年使用:0次
名校
解题方法
9 . 人类对物质微观结构的探索从未停歇,随着科学技术的发展,新的发现将继续揭开开原子更深层次结构的奥秘.
(1)原子结构模型的演变顺序正确的是
①道尔顿模型 ②有核模型 ③葡萄干面包模型 ④电子云模型 ⑤玻尔模型
(2)第一位通过实验证明原子可以再分的科学家是
(3)卢瑟福团队用 粒子
粒子 来轰击金箔,该化学符号中4代表的含义是①
来轰击金箔,该化学符号中4代表的含义是①_____________ ;在1~18号元素中,最外层电子数与氦原子相等的元素是②_____________ (填元素符号)。
(4)氦元素在自然界中仅有 和
和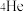 两种原子,它们具有相同的
两种原子,它们具有相同的
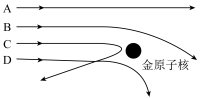
(5)当用 粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
(6)关于 粒子散射实验现象的记载如下:①________的
粒子散射实验现象的记载如下:①________的 粒子都直接穿过金箔,②______的
粒子都直接穿过金箔,②______的 粒子发生偏转,③ 的
粒子发生偏转,③ 的 粒子甚至被直接反弹回去.①②③三处空格分别为
粒子甚至被直接反弹回去.①②③三处空格分别为
(7)通过该试验,卢瑟福得出了原子结构的_____________ 模型。
(8)2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面作出突出贡献的科学家.点击化学的核心理念是,通过小单元的简便拼接,快速可靠地完成各种各样分子的化学合成.在点击化学中,反应快速发生,而且不会产生副产物.下列有关点击化学说法错误的是
(1)原子结构模型的演变顺序正确的是
①道尔顿模型 ②有核模型 ③葡萄干面包模型 ④电子云模型 ⑤玻尔模型
| A.①③②⑤④ | B.①②③④⑤ | C.①⑤③②④ | D.①③⑤④② |
(2)第一位通过实验证明原子可以再分的科学家是
| A.德谟克利特 | B.道尔顿 | C.汤姆孙 | D.卢瑟福 |
(3)卢瑟福团队用
 粒子
粒子 来轰击金箔,该化学符号中4代表的含义是①
来轰击金箔,该化学符号中4代表的含义是①(4)氦元素在自然界中仅有
 和
和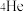 两种原子,它们具有相同的
两种原子,它们具有相同的 | A.质子数 | B.中子数 | C.物理性质 | D.化学性质 |
(5)当用
 粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是
粒子轰击金箔时,如图所示的运动轨迹中不可能存在的是 
| A.A | B.B | C.C | D.D |
(6)关于
 粒子散射实验现象的记载如下:①________的
粒子散射实验现象的记载如下:①________的 粒子都直接穿过金箔,②______的
粒子都直接穿过金箔,②______的 粒子发生偏转,③ 的
粒子发生偏转,③ 的 粒子甚至被直接反弹回去.①②③三处空格分别为
粒子甚至被直接反弹回去.①②③三处空格分别为 | A.绝大多数,极少数,个别 | B.个别,极少数,绝大多数 |
| C.几乎半数,几乎半数,个别 | D.个别,几乎半数,几乎半数 |
(7)通过该试验,卢瑟福得出了原子结构的
(8)2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面作出突出贡献的科学家.点击化学的核心理念是,通过小单元的简便拼接,快速可靠地完成各种各样分子的化学合成.在点击化学中,反应快速发生,而且不会产生副产物.下列有关点击化学说法错误的是
| A.点击化学的反应中会出现新的分子 | B.点击化学的反应中会出现新的原子 |
| C.点击化学能提高反应的准确性 | D.点击化学在生物医疗领域有广泛的应用前景 |
您最近一年使用:0次
18-19高一下·内蒙古·期中
名校
10 . 已知1-20号元素中A、B、C、D、E、F、G元素原子质子数依次增大,A的某种同位素可用于考古测定文物年代;C最外层电子数是次外层的3倍;D的阳离子是同周期元素形成的阳离子中半径最大的,E的阳离子为同周期中最小的;F最高正价与最低负价代数和为6;G的原子核外K、M层电子数之和等于L、N层电子数之和,试推断:
(1)元素的名称:B_______ D______ G在周期表中的位置_____
(2)写出含有10个中子的C元素的原子符号________
(3)B、E、F、G形成的简单离子的半径由大到小排序__________ (用元素符号表示)
(4)在A、B元素各自形成的氢化物中,稳定性较差的氢化物的化学式为____ ,原因为是_____ ;其氢化物中沸点较高的化学式为________ ,原因是______ 。
(5)C可与氢元素形成四核18电子的物质,其电子式为______ ,含有的化学键类型_____ 。
(6)E的最高价氧化物对应的水化物可与G的最高价氧化物对应的水化物发生反应的离子方程式为____ 。
(7)D与周期表中非金属性最强的元素可形成化合物X,用电子式表示X的形成过程_______ 。
(1)元素的名称:B
(2)写出含有10个中子的C元素的原子符号
(3)B、E、F、G形成的简单离子的半径由大到小排序
(4)在A、B元素各自形成的氢化物中,稳定性较差的氢化物的化学式为
(5)C可与氢元素形成四核18电子的物质,其电子式为
(6)E的最高价氧化物对应的水化物可与G的最高价氧化物对应的水化物发生反应的离子方程式为
(7)D与周期表中非金属性最强的元素可形成化合物X,用电子式表示X的形成过程
您最近一年使用:0次



