解题方法
1 . (1)画出下列元素的原子结构示意图。
①核电荷数为13的元素:_______ 。
②最外层电子数等于次外层电子数的元素原子:______ 。
(2)现有粒子:1H、35Cl、2H、14N、2H37Cl,其中:
①有_________ 种元素;
②__________ 之间互称同位素。
①核电荷数为13的元素:
②最外层电子数等于次外层电子数的元素原子:
(2)现有粒子:1H、35Cl、2H、14N、2H37Cl,其中:
①有
②
您最近一年使用:0次
2012·上海浦东新·三模
2 . 硼矿是无机盐工业的重要原料,硼镁石用硫酸分解的反应式为2MgO·B2O3·H2O+2H2SO4→2H3BO3+2MgSO4。
(1)上述反应中,核外电子排布式相同的离子有__ ;原子核外具有五种不同能量电子的元素名称是__ 。
(2)硼元素在元素周期表中的位置是__ ;已知BF3分子的空间构型为平面正三角形,则BF3属于__ 分子(填“极性”或“非极性”)。
(3)Mg元素的原子结构示意图为__ 。Mg(OH)2碱性比Ca(OH)2__ (填“强”或“弱”)。
(4)硼酸[H3BO3或B(OH)3]是一元弱酸,它的水溶液之所以呈弱酸性并非本身电离出H+,而是硼酸与水作用时,与水电离产生的OH-结合,导致溶液中c(H+)>c(OH-)。用离子方程式表示硼酸呈酸性的原因__ 。
(1)上述反应中,核外电子排布式相同的离子有
(2)硼元素在元素周期表中的位置是
(3)Mg元素的原子结构示意图为
(4)硼酸[H3BO3或B(OH)3]是一元弱酸,它的水溶液之所以呈弱酸性并非本身电离出H+,而是硼酸与水作用时,与水电离产生的OH-结合,导致溶液中c(H+)>c(OH-)。用离子方程式表示硼酸呈酸性的原因
您最近一年使用:0次
解题方法
3 . (1)写出符合下列条件的原子的元素符号并画出其原子结构示意图。
①核外有2个电子层、10个电子的原子__________________ ;
②质量数为23、中子数为12的原子__________________ ;
③电子总数是最外层电子数3倍的原子__________________ 。
(2)用下列原子或离子的结构示意图的编号(A、B、C、D)填空:
A.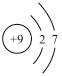 B.
B.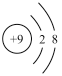 C.
C.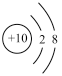 D.
D.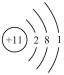
①电子层排布相同的是__________________ ;
②属于同一种元素的是__________________ ;
③属于金属元素的是__________________ ;
④属于稀有气体元素的是__________________ 。
①核外有2个电子层、10个电子的原子
②质量数为23、中子数为12的原子
③电子总数是最外层电子数3倍的原子
(2)用下列原子或离子的结构示意图的编号(A、B、C、D)填空:
A.
 B.
B. C.
C. D.
D.
①电子层排布相同的是
②属于同一种元素的是
③属于金属元素的是
④属于稀有气体元素的是
您最近一年使用:0次
19-20高二·浙江·阶段练习
解题方法
4 . (1)地壳由90多种化学元素组成,其含量最高的几种元素依次为①氧②硅③铝④铁,写出氧原子的结构示意图_______________ ;写出一种与氖具有相同核外电子 排布的离子___________ 。
(2)下列物质中① ②熔融碳酸钠③
②熔融碳酸钠③ 固体④蔗糖⑤
固体④蔗糖⑤ 溶液⑥铁能导电的是
溶液⑥铁能导电的是________ 属于非电解质的是________ ;(以上填写物质编号);写出②的电离方程式__________________ 。
(2)下列物质中①
 ②熔融碳酸钠③
②熔融碳酸钠③ 固体④蔗糖⑤
固体④蔗糖⑤ 溶液⑥铁能导电的是
溶液⑥铁能导电的是
您最近一年使用:0次
5 . 化学用语表示:
(1)根据下列几种粒子的结构示意图,回答问题:
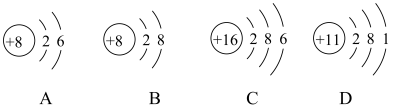
①写出B微粒的符号_________ ;
②若A微粒的中子数为10,写出表示A微粒的组成符号________ ;
③写出A、C、D三种元素形成的某种化合物在水溶液中的电离方程式:_________ ;
(2)写出下列反应的化学方程式:
①氯化铵与氢氧化钠共热____________ ;
②工业上制备氯气____________ 。
(1)根据下列几种粒子的结构示意图,回答问题:

①写出B微粒的符号
②若A微粒的中子数为10,写出表示A微粒的组成符号
③写出A、C、D三种元素形成的某种化合物在水溶液中的电离方程式:
(2)写出下列反应的化学方程式:
①氯化铵与氢氧化钠共热
②工业上制备氯气
您最近一年使用:0次
解题方法
6 . 我国自主研制的C919大型客机的机身大量采用第三代铝锂合金减重并提高刚度。某铝锂合金成分(质量百分比)如下(Bal指剩余的百分含量):

为了使合金具有高耐腐性能,通常先用酸腐蚀除去铝锂合金表面的氧化层,再进行氧化处理,并进行适当封闭,以提高合金表面耐腐蚀性能。仔细阅读上述信息,回答下列问题:
(1)铝锂合金可用于制造飞机,铝锂合金材料的主要特点是______________________________ 。
(2)铝元素原子核外有_____ 种不同运动状态的电子,最外层电子排布式为___________ 。
(3)碱腐蚀工艺采用40~60g/L的NaOH溶液,在40~55℃下处理0.5~2min时间。写出碱腐蚀主要反应的化学方程式_____________________________ (写一个即可)。
(4) 镁与铝也是构成轻合金的两种常见金属,请从原子结构角度分析比较它们金属性的强弱_____________
(5) 向镁铝合金滴入盐酸至恰好全部溶解,再逐渐滴入氢氧化钠溶液至过量,在滴氢氧化钠过程中观察到的现象有:______________________________________ ;写出其现象中的一个离子方程式_________________ 。

| 成分 | Si | Fe | Cu | Mn | Mg | Zn | Ti | Li | Al |
| 含量 | 0.08 | 0.1 | 2.9~3.5 | 0.5 | 0.25~0.8 | 0.25 | 0.1 | 0.8~1.1 | Bal |
(1)铝锂合金可用于制造飞机,铝锂合金材料的主要特点是
(2)铝元素原子核外有
(3)碱腐蚀工艺采用40~60g/L的NaOH溶液,在40~55℃下处理0.5~2min时间。写出碱腐蚀主要反应的化学方程式
(4) 镁与铝也是构成轻合金的两种常见金属,请从原子结构角度分析比较它们金属性的强弱
(5) 向镁铝合金滴入盐酸至恰好全部溶解,再逐渐滴入氢氧化钠溶液至过量,在滴氢氧化钠过程中观察到的现象有:
您最近一年使用:0次
7 . 观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
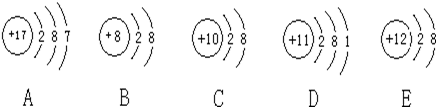
(1)属于离子结构示意图的是______ 、______ (填编号)。
(2)性质最稳定的原子是(填写编号,在本小题中下同)______ ,最容易失去电子的原子是______ ,最容易得到电子的原子是______ 。
(3)A、D两种元素形成的化合物在水溶液中的电离方程式______ 。
(4)在核电荷数1-18的元素内,列举两个与B核外电子层排布相同的离子,写出离子的符号______ 、______ 。

(1)属于离子结构示意图的是
(2)性质最稳定的原子是(填写编号,在本小题中下同)
(3)A、D两种元素形成的化合物在水溶液中的电离方程式
(4)在核电荷数1-18的元素内,列举两个与B核外电子层排布相同的离子,写出离子的符号
您最近一年使用:0次
2019-01-27更新
|
542次组卷
|
7卷引用:2011-2012学年江苏省江阴市一中高一上学期期中考试化学试卷
(已下线)2011-2012学年江苏省江阴市一中高一上学期期中考试化学试卷陕西省黄陵中学2018-2019学年高一(普通班)上学期期末考试化学试题(已下线)2019年4月1日《每日一题》 必修2 原子的组成与结构第1章原子结构与元素周期律第1节易错疑难集训(一)鲁科版(2019)必修第二册第一章第1节 易错疑难集训(已下线)2.3.2 原子核外电子排布练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)2.3.2 原子核外电子排布-2021-2022学年高一化学10分钟课前预习练(苏教版2019必修第一册)
名校
8 . 下表是元素周期表的一部分。
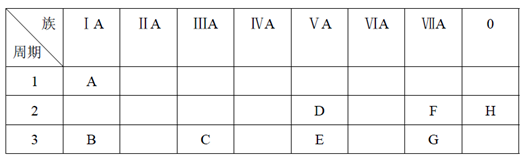
根据A~G元素在周期表中的位置,用化学式填写空白。
(1)氧化性最强的单质是______ ,还原性最强的单质是______ ,化学性质最不活泼的单质是______ 。(填相应的化学式)
(2)最稳定的氢化物是______ 。(填相应的化学式)
(3)一个E原子的核外电子总共有______ 种运动状态。
(4)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是_______ 。(填相应的化学式)

根据A~G元素在周期表中的位置,用化学式填写空白。
(1)氧化性最强的单质是
(2)最稳定的氢化物是
(3)一个E原子的核外电子总共有
(4)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是
您最近一年使用:0次
2018-05-28更新
|
555次组卷
|
2卷引用:【全国百强校】四川省南充高级中学2017-2018学年高二下学期期中化学试题
9 . A、B、C、D、E代表5种元素。请填空:
(1)A 元素基态原子的最外层有2 个未成对电子,次外层有2 个电子,其元素符号为______ ;
(2) B 元素的负一价离子和C元素的正一价离子的电子层结构都与氖相同,B 的元素符号为______ , C的元素符号为______ 。
(3) D 元素的正二价离子的3d能级为半充满,D的元素符号为_____ ,其基态原子的电子排布式为______ ,它位于第________ 周期第______ 族;
(4) E 元素基态原子的M 层能量最高的能级半充满,N 层没有成对电子,只有一个未成对电子,E 的元素符号为_____________ , 其基态原子的电子排布式为_______________ 。
(1)A 元素基态原子的最外层有2 个未成对电子,次外层有2 个电子,其元素符号为
(2) B 元素的负一价离子和C元素的正一价离子的电子层结构都与氖相同,B 的元素符号为
(3) D 元素的正二价离子的3d能级为半充满,D的元素符号为
(4) E 元素基态原子的M 层能量最高的能级半充满,N 层没有成对电子,只有一个未成对电子,E 的元素符号为
您最近一年使用:0次
10 . 根据下列几种粒子的结构示意图,回答问题:
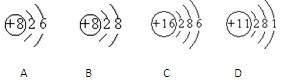
(1)属于阴离子的是______ (填粒子代号,下同)
(2)属于金属元素的是_______________________
(3)具有相似化学性质的是____________________
(4)D2C2含有的化学键类型有___________________ (选填“离子键”“极性键”“非极性键”)
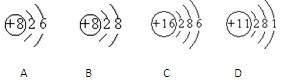
(1)属于阴离子的是
(2)属于金属元素的是
(3)具有相似化学性质的是
(4)D2C2含有的化学键类型有
您最近一年使用:0次



