名校
解题方法
1 . 安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为___________ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为___________ ,能量最高的电子为___________ 层上的电子。反应中涉及的主族元素的简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有___________ 个氮原子(保留三个有效数字);已知获得上述N2需要NaN3130g,反应生成N2的产率是___________ %(产率= ×100%)
×100%)
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有
 ×100%)
×100%)
您最近一年使用:0次
2 . 写出下列概念的含义:
(1)反应的热效应:_______________________________ 。
(2)泡利不相容原理:______________________________ 。
(1)反应的热效应:
(2)泡利不相容原理:
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)原子核外电子是分层排布的,当N层为最外层时,最多可容纳电子数是______ ;
(2)某元素原子,L层上的电子数是M层电子数的两倍,中子数为15,可表示相关信息的原子符号为______ ;
(3)原子核外电子排布可以用原子结构示意图简明的表示,如:
a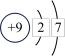 b
b c
c d
d
微粒d在化学反应中容易______ (选填“得到”或“失去”)电子,达到______ 结构;这些微粒中的稀有气体元素原子的电子式是______ ; 和
和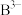 两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则
两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则 的结构示意图为
的结构示意图为______ ,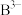 的电子式为
的电子式为______ 。
(1)原子核外电子是分层排布的,当N层为最外层时,最多可容纳电子数是
(2)某元素原子,L层上的电子数是M层电子数的两倍,中子数为15,可表示相关信息的原子符号为
(3)原子核外电子排布可以用原子结构示意图简明的表示,如:
a
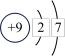 b
b c
c d
d
微粒d在化学反应中容易
 和
和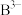 两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则
两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则 的结构示意图为
的结构示意图为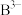 的电子式为
的电子式为
您最近一年使用:0次
4 . 最外层电子数目的变化
除第1周期外,每隔一定数目的元素,元素原子的最外层电子数重复出现从_____ 逐渐增加到_____ 的周期性变化。
除第1周期外,每隔一定数目的元素,元素原子的最外层电子数重复出现从
您最近一年使用:0次
5 . 电子在原子核外的区域内作高速运动,根据电子的能量高低划分为电子层,在各电子层上电子的排布也遵循着一定的规律。一些粒子的结构都可用下面的示意图来表示,且0<y≤8。
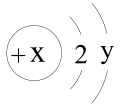
(1)若x=12时对应的元素为A,则y =_______ ;
(2)若某粒子带一个单位正电荷,则该粒子的化学符号为_______ ;
(3)若x=10,与其电子数相同的的微粒有(各举1个例子,可以是多核微粒):正离子_______ ,负离子_______ ,分子_______ 。
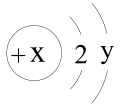
(1)若x=12时对应的元素为A,则y =
(2)若某粒子带一个单位正电荷,则该粒子的化学符号为
(3)若x=10,与其电子数相同的的微粒有(各举1个例子,可以是多核微粒):正离子
您最近一年使用:0次
6 . 有甲、乙、丙三种元素,甲元素的第3层的电子数是其第1层的电子数的1/2,乙元素原子核内无中子,丙元素原子核内有8个质子。
(1)写出甲元素的元素符号_______ 。
(2)画出丙元素的原子结构示意图_______ 。
(3)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式_______ 。
(1)写出甲元素的元素符号
(2)画出丙元素的原子结构示意图
(3)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
您最近一年使用:0次
7 . 据报道,某些花岗岩会释放氡 ,对人体造成伤害。
,对人体造成伤害。
(1)氡原子的核外电子数是___________ ,中子数是___________ 。
(2)请将Rn的原子结构示意图补全___________ 。
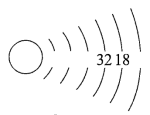
(3)请根据Rn的原子结构预测氡气的化学性质___________
(4)研究发现,镭能蜕变为 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为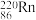 ,故将
,故将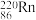 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为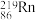 ,
,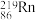 故将称为锕射气。
故将称为锕射气。 、
、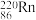 、
、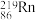
___________ 。
A.属于同种元素B.互为同位素C.属于同种核素D.属于同种原子
判断依据:___________ 决定元素种类,___________ 决定核素种类。
 ,对人体造成伤害。
,对人体造成伤害。(1)氡原子的核外电子数是
(2)请将Rn的原子结构示意图补全

(3)请根据Rn的原子结构预测氡气的化学性质___________
| A.非常活泼,容易与氧气等非金属单质反应 |
| B.比较活泼,能与钠等金属反应 |
| C.不太活泼,与氮气性质相似 |
| D.很难与其他物质发生反应 |
 ,故将
,故将 称为镭射气;钍能蜕变为
称为镭射气;钍能蜕变为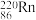 ,故将
,故将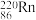 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为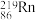 ,
,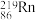 故将称为锕射气。
故将称为锕射气。 、
、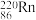 、
、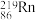
A.属于同种元素B.互为同位素C.属于同种核素D.属于同种原子
判断依据:
您最近一年使用:0次
8 . 科学家们用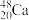 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了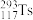 原子。已知
原子。已知
(1)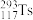 的原子结构示意图是
的原子结构示意图是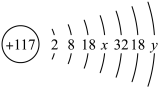 ,其中的x=
,其中的x=_______ ,y=_______ 。
(2)Ts位于元素周期表的第_______ 周期,第_______ 族,与它属于同族的一种元素是_______ 。(填元素符号)
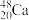 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了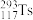 原子。已知
原子。已知(1)
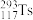 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x=(2)Ts位于元素周期表的第
您最近一年使用:0次
解题方法
9 . 按要求填空:
(1)基态Si原子中,电子占据的能量最高的电子层符号为_______ ,该电子层具有的原子轨道数为_______ ,具有的电子数为_______
(2)基态N原子中,核外电子占据_______ 个电子层,_______ 个原子轨道,共有_______ 种运动状态;电子占据的能量最高的原子轨道的形状为_______ 。
(1)基态Si原子中,电子占据的能量最高的电子层符号为
(2)基态N原子中,核外电子占据
您最近一年使用:0次
2022-08-22更新
|
240次组卷
|
2卷引用:专题2 原子结构与元素性质 第一单元 原子核外电子的运动 第1课时 人类对原子结构的认识 原子核外电子的运动特征
名校
10 . A、B两元素。A元素的M层电子数与K层电子数相等;B元素原子的M层电子数等于其L层电子数的一半。则A为_______ ,B为_______ 。
您最近一年使用:0次



