1 . 已知短周期主族元素Q、T、U、V、W、X、Y、Z原子序数依次增大。已知:T与U、V同周期,W与X、Y、Z同周期,U和Y同族;元素Q的某种核素没有中子;元素T的最高正价与最低负价的代数和为0;Q与U形成的气态化合物相对分子质量为17;工业上通过分离液态空气获得V的单质,且该单质的某种同素异形体是保护地球地表环境的重要屏障;W、X、Z的最高价氧化物对应的水化物两两之间都能反应,且W、X、Z原子最外层电子数之和等于W的原子序数。
(1)Z元素原子的 L层电子数为______ ,元素 Y的原子结构示意图___________ ,T的一种核素在考古时常用来鉴定一些文物的年代,用的核素是___________ (填核素符号)。
(2)元素Q与V可以形成18电子化合物的其电子式为_________ ,元素W与Q形成的化合物的类型_____________ (填‘离子化合物’或‘共价化合物’)。
(3)V的氢化物比同主族其他元素的氢化物的熔沸点明显偏高,原因是___________ 。
(4)写出X、W 两种元素最高价氧化物对应的水化物相互反应的离子方程式:____________ 。
(1)Z元素原子的 L层电子数为
(2)元素Q与V可以形成18电子化合物的其电子式为
(3)V的氢化物比同主族其他元素的氢化物的熔沸点明显偏高,原因是
(4)写出X、W 两种元素最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
2019-05-05更新
|
337次组卷
|
3卷引用:四川省宜宾市叙州区第二中学校2019-2020学年高一下学期期中考试化学试题
名校
2 . (1)H、D、T三种原子,在标准状况下,它们的单质的密度之比是_______ ,它们与氧的同位素16O、18O相互结合为水,可得水分子的种数为_______ ;[14NH3T]+ 中,电子数、质子数、中子数之比为______
(2)含6.02×1023个中子的73Li的质量是_________ g;核内中子数为N的R2+,质量数为A,则n g它的同价态氧化物中所含电子的物质的量为_______________ 。
(3)①Ne ②HCl ③P4 ④N2H4 ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I ⑨AlCl3,请用上述物质的序号填空:
只存在极性共价键的是____________ ,只存在非极性共价键的是_______________ 。既存在离子键又存在非极性共价键的是_______________________ 。
(4)在下列变化中,①碘的升华 ②烧碱熔化 ③MgCl2溶于水 ④HCl溶于水 ⑤Na2O2溶于水,未发生化学键破坏的是_____________ ,仅发生离子键破坏的是_____________ (填写序号)
(2)含6.02×1023个中子的73Li的质量是
(3)①Ne ②HCl ③P4 ④N2H4 ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I ⑨AlCl3,请用上述物质的序号填空:
只存在极性共价键的是
(4)在下列变化中,①碘的升华 ②烧碱熔化 ③MgCl2溶于水 ④HCl溶于水 ⑤Na2O2溶于水,未发生化学键破坏的是
您最近一年使用:0次
真题
名校
3 . 某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为______ 。
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为______ (已知该反应为置换反应).
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为______ ,K的原子结构示意图为_____ 。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为__________ 。
(5)100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况)。
①用碱石灰除去的物质为_____ ;
②该产气药剂中NaN3的质量分数为______ 。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
(5)100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况)。
①用碱石灰除去的物质为
②该产气药剂中NaN3的质量分数为
您最近一年使用:0次
2019-01-30更新
|
2707次组卷
|
16卷引用:【全国百强校】四川省阆中中学新区2018-2019学年高二上学期第一次月考化学试题
【全国百强校】四川省阆中中学新区2018-2019学年高二上学期第一次月考化学试题2015年全国普通高等学校招生统一考试化学(重庆卷)2015-2016学年宁夏六盘山中学高二下第一次月考化学卷2015-2016学年宁夏六盘山高中高一下期中化学试卷2015-2016学年辽宁省大连市瓦房店高中高二下期末化学试卷2017届重庆市育才中学高三上12月考前测试化学卷2017届宁夏固原市第一中学高三下学期第一次月考理综化学试卷22017届宁夏固原市第一中学高三下学期第一次月考理综化学试卷陕西省黄陵中学2018届高三(重点班)上学期期中考试化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.4 氧化还原反应【全国校级联考】新疆维吾尔自治区昌吉市教育共同体2019届高三上学期9月月考化学试题百所名校联考-必修一模块综合检测鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 微项目 研究车用燃料及安全气囊吉林省松原市油田第十一中学2021届高三第一次阶段考试化学试题(已下线)第8单元 原子结构 元素周期律(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷2017届宁夏固原市第一中学高三下学期第一次月考理综化学试卷1
名校
4 . 有下列物质:①金属铜 ②NaOH ③I2 ④MgCl2 ⑤Na2O2 ⑥氩气 回答下列问题:
(1)不存在化学键的是_________________________
(2)只存在非极性键的是__________________________
(3)只存在离子键的是__________________________
(4)既存在离子键又存在极性键的是__________________________
(5)既存在离子键又存在非极性键的是____________________________
(1)不存在化学键的是
(2)只存在非极性键的是
(3)只存在离子键的是
(4)既存在离子键又存在极性键的是
(5)既存在离子键又存在非极性键的是
您最近一年使用:0次
2018-05-02更新
|
1128次组卷
|
7卷引用:四川省眉山市仁寿第二中学、华兴中学2019-2020学年高一下学期5月联考(期中)化学试题
5 . Ⅰ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解。用序号填空:
(1)未破坏化学键的是_____________ ,(2)仅离子键被破坏的是_____________ ,
(3)仅共价键被破坏的是_____________ ;
Ⅱ.有下列各组物质:①石墨和足球烯C60;②126C和136C;③CH3—CH2—CH2—CH3和CH3—CH(CH3)CH3;④漂白粉和漂白液主要成分;⑤正丁烷和异庚烷;⑥乙烯和聚乙烯;⑦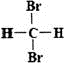 和
和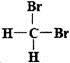 ;⑧丙烷和环丙烷。用序号填空:
;⑧丙烷和环丙烷。用序号填空:
(1)__________ 组两者互为同位素,(2)__________ 组两者互为同素异形体,
(3)__________ 组两者属于同系物,(4)__________ 组两者互为同分异构体,
(5)__________ 组两者是同一物质;
Ⅲ.化合物A的结构简式为: ,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名
,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名_____________________ ,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________ ;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简式为__________________ 。
(1)未破坏化学键的是
(3)仅共价键被破坏的是
Ⅱ.有下列各组物质:①石墨和足球烯C60;②126C和136C;③CH3—CH2—CH2—CH3和CH3—CH(CH3)CH3;④漂白粉和漂白液主要成分;⑤正丁烷和异庚烷;⑥乙烯和聚乙烯;⑦
 和
和 ;⑧丙烷和环丙烷。用序号填空:
;⑧丙烷和环丙烷。用序号填空:(1)
(3)
(5)
Ⅲ.化合物A的结构简式为:
 ,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名
,它是汽油燃烧品质抗震性能的参照物,用系统命名法对它命名
您最近一年使用:0次
名校
6 . I.根据元素周期表1〜18号元素的性质和递变规律,请用元素回答下列问题。
①原子半径最小的元素是_______ (稀有气体除外);②电负性最大的元素是_______ ;
③第一电离能最大的元素是________ ;④金属性最强的元素是_________ 。
II.①He ②SiC ③Na2O ④Na2O2 ⑤NaOH ⑥金刚石 ⑦白磷(P4)七种晶体中,不存在化学键的是_______ (填序号,下同);作用力只有共价键的单质是______ ;只存在离子键的离子化合物是______ ;含有非极性共价键的离子化合物是_______ 。
①原子半径最小的元素是
③第一电离能最大的元素是
II.①He ②SiC ③Na2O ④Na2O2 ⑤NaOH ⑥金刚石 ⑦白磷(P4)七种晶体中,不存在化学键的是
您最近一年使用:0次
13-14高三上·河南南阳·期中
7 . A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题:
(1)元素D在周期表中的位置_______________________ 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)___________ .
(3)由A、B、C三种元素以原子个数比4 :2 :3形成化合物X,X中所含化学键类型有________________ .
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:____________ ;若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:________________ 。
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方________________ 。
请回答下列问题:
(1)元素D在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4 :2 :3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
(5)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方
您最近一年使用:0次
8 . (1)写出电子式:KOH________________________ ;CO2_______________________
(2)用电子式表示下列化合物的形成过程:CaF2:___________________________________
H2S:____________________________________________________________________
(2)用电子式表示下列化合物的形成过程:CaF2:
H2S:
您最近一年使用:0次
2016-12-08更新
|
1469次组卷
|
8卷引用:四川省峨眉山市第一中学2018-2019学年高一下学期月考化学试题
四川省峨眉山市第一中学2018-2019学年高一下学期月考化学试题(已下线)2012届河北省南宫中学高三9月份月考化学试卷(已下线)2011-2012学年甘肃省武威第五中学高一3月月考化学试卷2014-2015学年内蒙古霍林郭勒市第三中学高一下期中考试化学试卷内蒙古巴彦淖尔第一中学2015-2016学年高一下4月考化学卷人教版高一化学必修2第一章物质结构与元素周期律单元检测试题浙江省苍南县金乡卫城中学2020-2021学年高一上学期第二次月考化学试题广西钦州市第四中学2020-2021学年高一下学期4月月考化学试题2



