名校
1 . 下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中、金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(2)由④、⑤、⑥三种元素形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)由元素②形成的单质的电子式为___________ ;元素⑤和⑧可形成化合物乙,请用电子式表示化合物乙的形成过程___________ 。
(4)元素③的最简单氢化物的化学式是___________ ,该氢化物在常温下与元素⑨发生反应的化学方程式是___________ ,所得溶液的pH___________ 7。
(5)元素⑥的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________ 。
| 族周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | |||||||
(1)上述元素中、金属性最强的是
(2)由④、⑤、⑥三种元素形成的简单离子半径由大到小的顺序是
(3)由元素②形成的单质的电子式为
(4)元素③的最简单氢化物的化学式是
(5)元素⑥的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
您最近一年使用:0次
名校
2 . 研究物质的结构,用来探寻物质的性质,是我们学习化学的重要方法。回答下列问题:
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为___________ 。
(2)氰酸铵( )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式___________ 。
(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因___________ 。

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是___________ 。(已知电负性:H-2.1 Be-1.5 B -2.0 N-3.0 O-3.5 Al-1.5 Si-1.8)
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石( )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。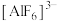 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是___________ 个。
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为
(2)氰酸铵(
 )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石(
 )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。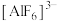 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
您最近一年使用:0次
解题方法
3 . 回答下列问题:
(1)用电子式表示下列化合物的形成过程:
HClO :_______ ,MgCl2:_______ 。
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是_______ ;只含有非极性键的是_______ ;既含有极性键的是又含有非极性键的是_______ ;只含离子键的是_______ ;⑥含有什么键_______ ;属于离子化合物的是_______ ;属于共价化合物的是_______ 。
(1)用电子式表示下列化合物的形成过程:
HClO :
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是
您最近一年使用:0次
名校
解题方法
4 . 在下列物质中:①CO2 ②KOH ③He ④BaSO4 ⑤NaCl。
(1)其中只含离子键的是(填序号,下同)_______ ,既含离子键又含共价键的是_______ ,不含化学键的是_______ 。
(2)下列物质在所述变化中:①烧碱熔化 ②HCl气体溶于水 ③NH4Cl受热分解 ④干冰升华。其中化学键未被破坏的是(填序号,下同)_______ ,仅发生共价键破坏的是_______ ,既发生离子键破坏,又发生共价键破坏的是_______ 。
(1)其中只含离子键的是(填序号,下同)
(2)下列物质在所述变化中:①烧碱熔化 ②HCl气体溶于水 ③NH4Cl受热分解 ④干冰升华。其中化学键未被破坏的是(填序号,下同)
您最近一年使用:0次
5 . I.化学研究的对象是物质,下列物质:①HCl②NaOH③Cl2④H2O2⑤NH4Cl⑥P4⑦NH3•H2O⑧Na2O2⑨HClO⑩MgCl2。
(1)物质②、④的电子式分别为_______ ,⑨的结构式为_______ 。
(2)只存在离子键的是_______ (填序号,下同)。
(3)含有非极性键的共价化合物的是_______ ,既存在离子键又存在共价键的是_______ 。
II.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:
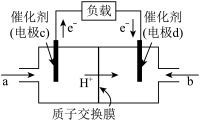
(4)电极d是_______ (填“正极”或“负极”),电极c的电极反应式_______ 。
(5)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。
(1)物质②、④的电子式分别为
(2)只存在离子键的是
(3)含有非极性键的共价化合物的是
II.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:

(4)电极d是
(5)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
名校
6 . 下面是我们熟悉的物质:①O2 ②NaBr ③H2SO4 ④Na2CO3 ⑤NH4Cl ⑥NaHSO4 ⑦Ne ⑧Na2O2 ⑨NaOH ⑩CO2。
(1)这些物质中,只含有共价键的是_______ ;只含有离子键的是_______ ;不存在化学键的是_______ (填物质序号)。
(2)属于共价化合物的是_______ (填物质序号)。
(3)CO2固体气化破坏了_______ 。
(1)这些物质中,只含有共价键的是
(2)属于共价化合物的是
(3)CO2固体气化破坏了
您最近一年使用:0次
名校
7 . Ⅰ.化学研究的对象是物质,下列物质:①HCl②NaOH③Cl2④H2O2⑤NH4Cl⑥P4⑦NH3·H2O⑧Na2O2⑨HClO⑩MgCl2中
(1)只存在离子键的是____ (填序号)。
(2)含有非极性键的共价化合物的是____ (填序号)。
(3)既存在离子键又存在共价键的是____ (填序号)。
(4)②熔化过程破坏____ (选填“离子键”、“极性键”、“非极性键”或“范德华力”)。
(5)③溶于水破坏____ (选填“离子键”、“极性键”、“非极性键”或“范德华力”)。
Ⅱ.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:

(6)电极d是____ (填“正极”或“负极”),电极c的电极反应式____ 。
(7)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为____ L。
(1)只存在离子键的是
(2)含有非极性键的共价化合物的是
(3)既存在离子键又存在共价键的是
(4)②熔化过程破坏
(5)③溶于水破坏
Ⅱ.现代生产、生活和国防中大量使用电池,各种电池应运而生。用CH4和O2组合形成的质子交换膜燃料电池的结构如图所示:

(6)电极d是
(7)若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
8 . (一)下面是我们熟悉的物质:①O2 ②NaBr ③H2SO4 ④Na2CO3 ⑤NH4Cl ⑥NaHSO4 ⑦Ne ⑧Na2O2 ⑨NaOH ⑩CO2。
(1)这些物质中,只含有共价键的是____ ;只含有离子键的是____ ;不存在化学键的是____ (填物质序号)。
(2)属于共价化合物的是____ (填物质序号)。
(3)将Na2O2溶于水,破坏了Na2O2中的____ ,Na2O2的电子式为____ ;NaHSO4熔融状态下电离,破坏了____ 键,写出电离方程式____ 。
(4)CO2固体气化破坏了____ 。
(二)由H、N、O、Al组成的微粒中:微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(5)用化学式表示下列3种微粒:A____ ;C____ ;D____ 。
(6)写出过量的B通入E的溶液中反应的离子方程式____ 。
(7)用电子式表示B的形成过程____ 。
(1)这些物质中,只含有共价键的是
(2)属于共价化合物的是
(3)将Na2O2溶于水,破坏了Na2O2中的
(4)CO2固体气化破坏了
(二)由H、N、O、Al组成的微粒中:微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(5)用化学式表示下列3种微粒:A
(6)写出过量的B通入E的溶液中反应的离子方程式
(7)用电子式表示B的形成过程
您最近一年使用:0次
2022-04-03更新
|
379次组卷
|
2卷引用:四川省成都外国语学校2021-2022学年高一下学期3月月考化学试题
名校
解题方法
9 . 下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语 回答下列问题;
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号_______ 。
(2)④、⑦、⑩的离子半径由大到小的顺序为_______ (用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式____ ,该物质含有的化学键类型有_____ 。
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为____ ,元素⑤和⑩的氢化物中,酸性更强的是_____ 。
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程____ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号
(2)④、⑦、⑩的离子半径由大到小的顺序为
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程
您最近一年使用:0次
2021-05-24更新
|
190次组卷
|
4卷引用:四川省遂宁市第二中学2020-2021学年高一下学期半期考试化学试题
四川省遂宁市第二中学2020-2021学年高一下学期半期考试化学试题(已下线)专题03 化学键【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)江西省南昌市进贤县第一中学2020-2021学年高一下学期期末考试化学试题河南省部分名校2020-2021学年高一下学期期末联考化学试题
名校
解题方法
10 . 有下列物质:①Cl2②Na2O2③NaOH④HCl⑤H2O2⑥MgF2
(1)只由离子键构成的物质是___ 。(填序号,下同)
(2)只由极性键构成的物质是___ 。
(3)只由非极性键构成的物质是___ 。
(4)由极性键和非极性键构成的物质是___ 。
(5)由离子键和极性键构成的物质是___ 。
(6)由离子键和非极性键构成的物质是___ 。
(1)只由离子键构成的物质是
(2)只由极性键构成的物质是
(3)只由非极性键构成的物质是
(4)由极性键和非极性键构成的物质是
(5)由离子键和极性键构成的物质是
(6)由离子键和非极性键构成的物质是
您最近一年使用:0次



