1 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素②的原子结构示意图是_______
(2)元素⑧在周期表中所处位置_______ ,从元素原子得失电子的角度看,元素⑤具有_______ (填“氧化性”或“还原性”)。
(3)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是_______ 。(填离子符号)
(4)第三周期元素除⑩外原子半径最大的是_______ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),具有两性的是_______ ,这两种物质反应的离子方程式为_______ 。
(5)⑤和⑨它们可以形成_______ (填“离子”或“共价”)化合物。
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)元素②的原子结构示意图是
(2)元素⑧在周期表中所处位置
(3)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是
(4)第三周期元素除⑩外原子半径最大的是
(5)⑤和⑨它们可以形成
您最近一年使用:0次
名校
解题方法
2 . 下表是元素周期表的一部分,针对表中的①~⑩中元素,请用化学用语填空回答以下问题:

(1)化学性质最不活泼的元素原子的原子结构示意图为________ 。
(2)元素①、②的简单氢化物的稳定性更强的是______________ (用化学式表示,下同)。
(3)元素的最高价氧化物对应的水化物中酸性最强的是______ ,碱性最强的是____ ,呈两性的氢氧化物是_________ ,元素③的最高价氧化物对应水化物中含有的化学键类型为________ 。
(4)在③~⑦元素中,简单离子半径最小的是_________ 。
(5)元素③的过氧化物的电子式为_________ 。
(6)在⑦与⑩的单质中,氧化性较强的是_____ ,用化学反应方程式证明:______ 。

(1)化学性质最不活泼的元素原子的原子结构示意图为
(2)元素①、②的简单氢化物的稳定性更强的是
(3)元素的最高价氧化物对应的水化物中酸性最强的是
(4)在③~⑦元素中,简单离子半径最小的是
(5)元素③的过氧化物的电子式为
(6)在⑦与⑩的单质中,氧化性较强的是
您最近一年使用:0次
名校
3 . 元素周期表的表达形式有多种,但都能表示出元素的周期性变化规律,请回答下列问题:
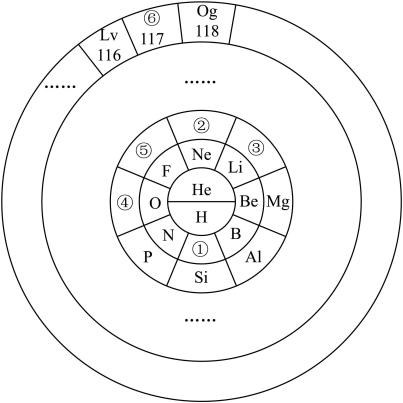
(1)①与④元素形成的化合物属于___________ 晶体。
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:__________ 。
(3)②号元素为___________ (填元素符号)。请写出1个与②核外电子数相同的简单离子组成的化合物的化学式:___________ 。其中存在的化学键属于___________ 键,该物质在熔融状态下___________ 导电(填“能”或“不能”)。
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:___________ ,将反应所得混合物溶于水,得到浅绿色的溶液,请写出相关的离子方程式:___________ 。
(5)其中非金属性④___________ ⑤(填“>”或“<”),请用一个化学方程式证明___________ 。
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为___________ ,根据元素的周期性规律,以下推测正确的是________
A.单质在常温下为气体 B.气态氢化物的稳定性较好
C.离子具有强还原性 D.半径大于⑤

(1)①与④元素形成的化合物属于
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:
(3)②号元素为
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:
(5)其中非金属性④
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为
A.单质在常温下为气体 B.气态氢化物的稳定性较好
C.离子具有强还原性 D.半径大于⑤
您最近一年使用:0次
名校
解题方法
4 . 几种主族元素在周期表中的位置如下:
(1)①⑨形成的化合物属于___________ (填“离子化合物”或“共价化合物”),用电子式表示其形成过程___________ 。
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为___________ 。
(3)比较⑦、⑧简单氢化物的还原性:___________ (填化学式);比较①、⑥、⑦三种简单离子的半径大小,其由大到小的顺序___________ (填离子符号)。
(4)下列可以判断①和③金属性强弱的是___________(填字母)。
(5)金属镓 常用作光学玻璃、真空管、半导体的原料。
常用作光学玻璃、真空管、半导体的原料。
预测 的化学性质并填写表格:
的化学性质并填写表格:
以上预测都是依据___________ 。
 | 0 | |||||||
| 1 | ④ |  |  | 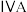 | 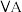 | 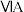 | 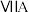 | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑨ | ⑦ | ||||
| 4 | ② |  | ⑧ | |||||
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为
(3)比较⑦、⑧简单氢化物的还原性:
(4)下列可以判断①和③金属性强弱的是___________(填字母)。
A.单质的熔点: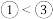 | B.化合价: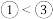 |
| C.单质与水反应的剧烈程度:①>③ | D.最高价氧化物对应水化物的碱性:①>③ |
 常用作光学玻璃、真空管、半导体的原料。
常用作光学玻璃、真空管、半导体的原料。预测
 的化学性质并填写表格:
的化学性质并填写表格:| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
 能与 能与 | 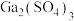 、 、 |
 能与 能与 | 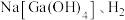 |
您最近一年使用:0次
名校
5 . 有三种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于___________ 。
(2)B的最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(3)元素D的非金属性比元素A的强,用原子结构解释原因___________ 。
(4)已知硒 与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是___________ 。
a. 的最低负化合价为-2价 b.
的最低负化合价为-2价 b. 既有氧化性又有还原性
既有氧化性又有还原性
c. 的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
| 元素 | 相关信息 |
| A | -2价阴离子的电子层结构与 原子相同 原子相同 |
| B | 单质的焰色反应为黄色 |
| D | 单质是黄绿色气体,可用于自来水消毒 |
(1)A在周期表中位于
(2)B的最高价氧化物对应的水化物中含有的化学键类型为
(3)元素D的非金属性比元素A的强,用原子结构解释原因
(4)已知硒
 与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
与A同主族,且位于A下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是a.
 的最低负化合价为-2价 b.
的最低负化合价为-2价 b. 既有氧化性又有还原性
既有氧化性又有还原性c.
 的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
的气态氢化物的稳定性比A的强 d.最高价氧化物对应的水化物为
您最近一年使用:0次
2023·全国·模拟预测
名校
解题方法
6 . 下列实验目的、方案设计和现象、结论都正确的是
| 选项 | 实验目的 | 方案设计和现象 | 结论 |
| A | 判断 的化学键类型 的化学键类型 | 将 固体溶于水,进行导电性实验, 固体溶于水,进行导电性实验, 溶液可导电 溶液可导电 |  中含有离子键 中含有离子键 |
| B | 验证某固体是 还是 还是 | 室温下取少量固体于试管中,插入温度计,加几滴水,温度降低 | 该固体是 |
| C | 探究乙炔的化学性质 | 将饱和食盐水滴入电石中,产生的气体通入溴的四氯化碳溶液中,溶液褪色 | 乙炔具有还原性 |
| D | 比较相同浓度的 溶液和 溶液和 溶液的酸碱性 溶液的酸碱性 | 用洁净干燥的玻璃棒分别蘸取 溶液和 溶液和 溶液,滴在pH试纸上,与标准比色卡比较,测得 溶液,滴在pH试纸上,与标准比色卡比较,测得 溶液对应的pH更小 溶液对应的pH更小 |  溶液的酸性更强 溶液的酸性更强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-11更新
|
889次组卷
|
4卷引用:化学押题卷(三)
(已下线)化学押题卷(三)(已下线)化学-2023年高考押题预测卷02(辽宁卷)(含考试版、全解全析、参考答案、答题卡)辽宁省锦州市渤海大学附属高级中学2023届高三下学期第六次模拟考试化学试题河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题
7 . 我们已经学习了钠、氯、铁、铝等元素的单质及其化合物的相关性质,请回答下列问题:
(1)四种元素的单质中,氧化性和还原性最强的两种单质反应生成某种化合物,用电子式表示该化合物的形成过程:____ 。
(2)把8.3g铁铝合金的粉末放入过量的盐酸中,得到5.6L标况下的H2,则合金中铁的质量分数为:____ (保留三位有效数字)。
(3)配平Na2FeO4与盐酸反应的方程式:____Na2FeO4+____HCl=____NaCl+____FeCl3+____H2O+____Cl2↑____ ,Na2FeO4的电离方程式为____ 。该反应按方程式计量数关系,所得产物中离子键与共价键的个数比为:____ 。
(1)四种元素的单质中,氧化性和还原性最强的两种单质反应生成某种化合物,用电子式表示该化合物的形成过程:
(2)把8.3g铁铝合金的粉末放入过量的盐酸中,得到5.6L标况下的H2,则合金中铁的质量分数为:
(3)配平Na2FeO4与盐酸反应的方程式:____Na2FeO4+____HCl=____NaCl+____FeCl3+____H2O+____Cl2↑
您最近一年使用:0次
解题方法
8 . 元素周期表体现了元素位置、结构和性质的关系,揭示了元素的内在联系。下表列出了①到⑧八种元素在周期表中的位置。
回答下列问题:
(1)元素①形成单质的电子式为_______ 。
(2)元素②的单质与水反应的离子方程式为_______ 。
(3)元素④⑤⑥的简单离子半径最大的是_______ (用离子符号表示)。
(4)用电子式表示元素③和元素⑥组成化合物的形成过程_______ 。
(5)元素④的单质与元素②最高价氧化物的水化物反应可以用于管道疏通,其原理为_______ (用离子方程式表示)。
(6)下列对元素⑦的说法正确的是_______ (填序号)。
a.原子最外层有6个电子
b.元素的非金属性:⑧>⑦
c.能形成 价的氧化物,该氧化物既有氧化性又有还原性
价的氧化物,该氧化物既有氧化性又有还原性
(7)从原子结构的角度解释元素⑥的非金属性强于元素⑤的原因_______ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 4 | ⑦ | ⑧ | ||||||
(1)元素①形成单质的电子式为
(2)元素②的单质与水反应的离子方程式为
(3)元素④⑤⑥的简单离子半径最大的是
(4)用电子式表示元素③和元素⑥组成化合物的形成过程
(5)元素④的单质与元素②最高价氧化物的水化物反应可以用于管道疏通,其原理为
(6)下列对元素⑦的说法正确的是
a.原子最外层有6个电子
b.元素的非金属性:⑧>⑦
c.能形成
 价的氧化物,该氧化物既有氧化性又有还原性
价的氧化物,该氧化物既有氧化性又有还原性(7)从原子结构的角度解释元素⑥的非金属性强于元素⑤的原因
您最近一年使用:0次
名校
9 . 短周期主族元素W、X、Y、Z、Q原子序数依次增大,这几种元素形成的一种化合物的结构如图所示。Z原子的核外最外层电子数与X原子核外电子总数相等,W的原子半径在周期表中最小。下列有关叙述不正确的是


| A.Z与W形成的化合物可能既有氧化性又有还原性 |
| B.简单氢化物的稳定性:X>Z |
| C.原子半径:X>Y>Z |
| D.Y与W两种元素既能形成10电子微粒,也能形成18电子微粒 |
您最近一年使用:0次
解题方法
10 . (1)下列关于硫酸的说法正确的是_______ (填序号)。
①在常温下,浓硫酸和浓硝酸与Fe和Al发生“钝化”,说明常温下浓硫酸和浓硝酸与Fe和Al都不反应
②浓硫酸具有强氧化性,稀硫酸不具有氧化性
③常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生“钝化”
④将浓硫酸滴到湿的蔗糖表面,固体变黑膨胀并有刺激性气味气体生成,说明浓硫酸有脱水性、吸水性和强氧化性
⑤浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
⑥浓硫酸具有吸水性,所以浓硫酸可以干燥H2、CO、NH3、H2S、HI、HBr等气体
(2)写出下列物质的电子式:
N2_______ ;MgCl2 _______ ;Na2O2_______ 。
①在常温下,浓硫酸和浓硝酸与Fe和Al发生“钝化”,说明常温下浓硫酸和浓硝酸与Fe和Al都不反应
②浓硫酸具有强氧化性,稀硫酸不具有氧化性
③常温下将铜片放入浓硫酸中,无明显变化,说明铜在浓硫酸中发生“钝化”
④将浓硫酸滴到湿的蔗糖表面,固体变黑膨胀并有刺激性气味气体生成,说明浓硫酸有脱水性、吸水性和强氧化性
⑤浓硫酸具有强氧化性,SO2具有还原性,所以浓硫酸不能干燥SO2
⑥浓硫酸具有吸水性,所以浓硫酸可以干燥H2、CO、NH3、H2S、HI、HBr等气体
(2)写出下列物质的电子式:
N2
您最近一年使用:0次



