1 . 利用反应CCl4+4Na 4NaCl+C(金刚石)可实现人工合成金刚石。下列说法正确的是
4NaCl+C(金刚石)可实现人工合成金刚石。下列说法正确的是
 4NaCl+C(金刚石)可实现人工合成金刚石。下列说法正确的是
4NaCl+C(金刚石)可实现人工合成金刚石。下列说法正确的是| A.反应过程中有离子键的断裂与形成 |
| B.熔点:C(金刚石)>Na>NaCl>CCl4 |
| C.NaCl晶体中,每个Cl–的周围距离其最近的Cl–有6个 |
D.金刚石晶胞中,若键长为apm,则晶胞参数为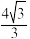 apm apm |
您最近一年使用:0次
名校
2 . 电负性用来描述不同元素的原子对键合电子吸引力的大小,是元素的一种基本性质。下表为一些元素的电负性(已知两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键):
下列说法不正确的是
| 元素 | Li | Be | B | C | N | F | Na | Mg | Al | Si | Cl | Ca |
| 电负性 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 4.0 | 0.9 | a | 1.5 | 1.8 | 3.0 | 1.0 |
| A.根据电负性变化规律,确定a的最小范围为1.0<a<1.5 |
| B.NF3中N-F键的极性比NCl3中N-Cl键的极性强 |
| C.AlCl3是一种可溶性盐,属于离子化合物 |
| D.可以通过测定化合物在熔融状态下是否导电鉴别Li3N与SiC |
您最近一年使用:0次
2024-02-22更新
|
201次组卷
|
4卷引用:安徽省皖中联盟考试2023-2024学年高二上学期1月期末化学试题
名校
解题方法
3 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。下表为元素周期表的一部分,列出了元素a~j在表中的位置。

回答下列问题:
(1)以上元素中金属性最强的是___________ (填元素符号)。
(2)f的最高价氧化物属于酸性氧化物,写出它与氢氧化钠溶液反应的化学方程式_________ 。
(3)b、d、i形成的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)d与h形成的化合物中化学键类型为___________ ,用电子式表示该化合物的形成过程___________ 。
(5)化合物b2g2与eg2的反应是“呼吸面具”的工作原理,请写出该化学反应方程式_________ 。
(6)下列事实能说明i的非金属性比j的非金属性强的是___________ (填字母)。
A.i的氢化物比j的氢化物稳定
B.i的氢化物酸性比j的氢化物酸性弱
C.i的单质能将j从其钠盐溶液中置换出来

回答下列问题:
(1)以上元素中金属性最强的是
(2)f的最高价氧化物属于酸性氧化物,写出它与氢氧化钠溶液反应的化学方程式
(3)b、d、i形成的简单离子半径由大到小的顺序是
(4)d与h形成的化合物中化学键类型为
(5)化合物b2g2与eg2的反应是“呼吸面具”的工作原理,请写出该化学反应方程式
(6)下列事实能说明i的非金属性比j的非金属性强的是
A.i的氢化物比j的氢化物稳定
B.i的氢化物酸性比j的氢化物酸性弱
C.i的单质能将j从其钠盐溶液中置换出来
您最近一年使用:0次
2024-02-03更新
|
116次组卷
|
2卷引用:贵州省铜仁市2023-2024学年高一上学期1月期末质量监测化学试题
名校
解题方法
4 . 下列物质中,既存在离子键又存在共价键的是
A. | B. | C. | D. |
您最近一年使用:0次
2024-01-21更新
|
132次组卷
|
2卷引用:四川省广安市华蓥中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
5 . 下列关于化学键的说法正确的是
①形成离子键的阴阳离子间只存在静电吸引力
②共价化合物一定含共价键,也可能含离子键
③离子化合物一定含离子键,也可能含极性键或非极性键
④熔融状态下能导电的化合物一定是离子化合物
⑤第I 族和第VII
族和第VII 族原子化合时,一定生成离子键
族原子化合时,一定生成离子键
⑥化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程
①形成离子键的阴阳离子间只存在静电吸引力
②共价化合物一定含共价键,也可能含离子键
③离子化合物一定含离子键,也可能含极性键或非极性键
④熔融状态下能导电的化合物一定是离子化合物
⑤第I
 族和第VII
族和第VII 族原子化合时,一定生成离子键
族原子化合时,一定生成离子键⑥化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程
| A.③④⑥ | B.③⑥ | C.①③⑤ | D.③④⑤ |
您最近一年使用:0次
2024-02-13更新
|
298次组卷
|
2卷引用:天津市重点校2023-2024学年高一上学期期末联考化学试题
名校
解题方法
6 . 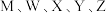 是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
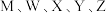 是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
A.原子半径: |
| B.X的氧化物一定属于酸性氧化物 |
| C.在Q的结构中,所有原子最外层均满足8电子稳定结构 |
| D.Y元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键 |
您最近一年使用:0次
2023-12-05更新
|
1971次组卷
|
11卷引用:四川省成都市石室中学2023-2024学年高三上学期期末考试理综试题-高中化学
四川省成都市石室中学2023-2024学年高三上学期期末考试理综试题-高中化学吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷宁夏石嘴山市第三中学2023-2024学年高三上学期第四次月考理科综合试卷江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期第四次月考理综试题湖南省永州市第一中学2023-2024学年高二上学期12月月考化学试题福建省泉州市培元中学2023-2024学年高三上学期12月月考化学试题(已下线)选择题11-16(已下线)专题04 物质结构与性质-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题陕西省西安中学2023-2024学年高三下学期模拟预测(五)理综试题-高中化学
名校
7 . 有关化学键的说法错误的是
| A.存在离子键的物质一定是离子化合物 |
| B.化学键是相邻原子或离子之间的强烈的相互作用,该作用只表现为吸引力 |
| C.存在共价键的物质可能为单质,可能是共价化合物,也可能是离子化合物 |
| D.化学键的强度远大于分子间作用力,一般而言化学键强度也强于氢键 |
您最近一年使用:0次
2023-10-04更新
|
225次组卷
|
2卷引用:新疆喀什地区十四校2023-2024学年高一上学期期末质量检测化学试卷
解题方法
8 . 下列反应中,即有离子键,又有共价键的是
| A.HCl | B.KCl | C.CaCl2 | D.NH4Cl |
您最近一年使用:0次
2023-10-03更新
|
248次组卷
|
2卷引用:新疆兵团第三师图木舒克市鸿德实验学校2022-2023学年高一下学期期末考试化学试题
名校
解题方法
9 . 下列说法不正确的是
| A.离子化合物和金属单质的构成粒子中均含有阳离子 |
| B.离子键和金属键本质上都是静电作用,都没有方向性和饱和性 |
| C.熔点:MgO>NaCl>Hg>HBr |
| D.NaHSO4在水溶液中和熔融状态下都能导电,电离方程式相同 |
您最近一年使用:0次
2023-12-30更新
|
253次组卷
|
3卷引用:北京市第一○一中学2021-2022学年高二下学期期末考试化学试卷
10 . 下列有关说法错误的是
A. 晶体中, 晶体中, 和 和 之间通过静电作用形成离子键 之间通过静电作用形成离子键 |
B. 中氢原子与氯原子通过共用电子形成共价键 中氢原子与氯原子通过共用电子形成共价键 |
C.氨气是共价化合物,电子式为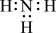 |
D.氯化钠是离子化合物,电子式为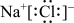 |
您最近一年使用:0次
2023-08-02更新
|
169次组卷
|
2卷引用:山东省威海市2022-2023学年高一下学期期末考试化学试题



