1 . 下列说法正确的是
A. 属于离子化合物 属于离子化合物 |
| B.金属元素与非金属元素形成的化合物一定是离子化合物 |
C. 分子中所有的原子均满足最外层8电子稳定结构 分子中所有的原子均满足最外层8电子稳定结构 |
D. 中阴、阳离子的个数比是1:2,熔化时破坏的是离子键和共价键 中阴、阳离子的个数比是1:2,熔化时破坏的是离子键和共价键 |
您最近一年使用:0次
解题方法
2 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
您最近一年使用:0次
3 . 有关晶体和微粒间作用力的说法不正确的是
| A.干冰是共价分子,其升华破坏了共价键 |
| B.冰是分子晶体,加热气化过程中不破坏化学键 |
| C.氯化钠是离子晶体,加热气化过程中破坏了离子键 |
| D.二氧化硅属于共价化合物,其熔化破坏了共价键 |
您最近一年使用:0次
解题方法
4 . 下列有关说法正确的是
A. 极易溶于水,是因为 极易溶于水,是因为 与水分子间存在氢键,氢键属于化学键 与水分子间存在氢键,氢键属于化学键 |
| B.金属元素与非金属元素之间只能形成离子键,不能形成共价键 |
C. 溶于水可以导电,但 溶于水可以导电,但 属于共价化合物 属于共价化合物 |
D. 反应中,既有离子键的断裂和形成,又有共价键的断裂和形成 反应中,既有离子键的断裂和形成,又有共价键的断裂和形成 |
您最近一年使用:0次
名校
5 . 拉希法制备肼 的主要反应为
的主要反应为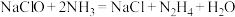 .下列表示反应中相关微粒的化学用语或说法错误的是
.下列表示反应中相关微粒的化学用语或说法错误的是
 的主要反应为
的主要反应为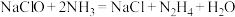 .下列表示反应中相关微粒的化学用语或说法错误的是
.下列表示反应中相关微粒的化学用语或说法错误的是A.中子数为18的氯原子: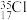 | B. 为离子化合物 为离子化合物 |
C. 的电子式: 的电子式: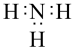 | D. 的结构式: 的结构式: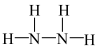 |
您最近一年使用:0次
解题方法
6 . 下列物质中,属于含有极性共价键的离子化合物的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
7 . 自然界中时刻存在着氮气的转化。实现氮气按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图。下列叙述正确的是
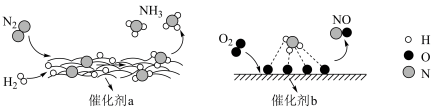
| A.N2→NH3,NH3→NO均属于氮的固定 |
| B.在催化剂a作用下,N2发生了还原反应 |
| C.催化剂a、b表面均发生了极性共价键的断裂 |
| D.生成的NH3为三角锥形 |
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、P、Q是原子序数依次增大的短周期主族元素,其中X的一种核素没有中子,Y的单质是空气的主要成分,Z和Q同主族且Q的原子序数是Z的二倍,在短周期元素中P的金属性最强。回答下列问题:
(1)X、Y、Z三种元素的原子半径从大到小的顺序为_______ (用元素符号表示)。
(2)Y、Z的简单氢化物中较不稳定的是_______ (填化学式),P和Q的最高价氧化物对应水化物的化学方程式为_______ 。
(3)M是由X、Z两种元素组成的含有10个电子的分子,M的电子式为_______ ,M分解反应过程中,反应物中化学键断裂吸收的总能量_______ 生成物中化学键形成放出的能量(填“大于”、“小于”或“等于”)。
(4)已知化合物PX与水反应生成氢气,因此可将其用作野外生存的生氢剂。
①该反应的化学方程式为_______ 。
②该反应中的氧化剂是_______ 还原剂是_______ 。
③反应中涉及到化学键的断裂和形成,其中包括_______ 填序号)。
a.离子键 b.极性共价键 c.非极性共价键 d.氢键
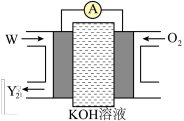
(5)化合物W是由X、Y两种元素组成的含有18个电子的分子,是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料,一种W燃料电池的工作原理如下图所示。放电一段时间,电解质溶液中OH﹣的物质的量浓度_______ (填“增大”“减小”或“不变”),负极反应式为_______ 。
(1)X、Y、Z三种元素的原子半径从大到小的顺序为
(2)Y、Z的简单氢化物中较不稳定的是
(3)M是由X、Z两种元素组成的含有10个电子的分子,M的电子式为
(4)已知化合物PX与水反应生成氢气,因此可将其用作野外生存的生氢剂。
①该反应的化学方程式为
②该反应中的氧化剂是
③反应中涉及到化学键的断裂和形成,其中包括
a.离子键 b.极性共价键 c.非极性共价键 d.氢键
(5)化合物W是由X、Y两种元素组成的含有18个电子的分子,是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料,一种W燃料电池的工作原理如下图所示。放电一段时间,电解质溶液中OH﹣的物质的量浓度
您最近一年使用:0次
9 . 一种以太阳能聚热驱动制备CO和 的过程如图,
的过程如图, 是总反应的催化剂,下列说法正确的是
是总反应的催化剂,下列说法正确的是
 的过程如图,
的过程如图, 是总反应的催化剂,下列说法正确的是
是总反应的催化剂,下列说法正确的是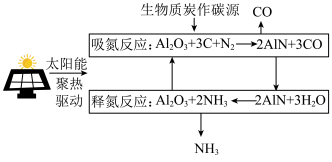
A.CO和 互为同素异形体 互为同素异形体 |
| B.吸氮反应中有非极性共价键的断裂和极性共价键的形成 |
C.释氮反应时,每生成22.4 L ,转移6 mol电子 ,转移6 mol电子 |
| D.CO属于酸性氧化物 |
您最近一年使用:0次
解题方法
10 . NaOH是一种重要的化工原料,工业生产中可利用直流电电解饱和食盐水法来制取:
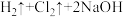 。下列说法正确的是
。下列说法正确的是

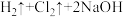 。下列说法正确的是
。下列说法正确的是A.NaCl的电子式为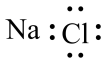 | B.NaOH中含有共价键 |
| C.熔融的NaOH不能导电 | D.该反应的氧化产物为 |
您最近一年使用:0次



